-
下列说法中正确的是
A.所有主族元素的正化合价数,等于它的族序数
B.第ⅦA族元素的原子随核电荷数的增加,得电子能力逐渐减弱
C.第ⅡA族元素的阳离子与同周期稀有气体元素的原子具有相同的核外电子排布
D.前三周期元素中共有非金属元素12种
高二化学选择题中等难度题查看答案及解析
-
根据原子结构及元素周期律的知识,下列推断正确的是
A.
得电子能力相同
B.同主族元素含氧酸的酸性随核电荷数的增加而减弱
C.Cl-、S2-、Ca2+、K+半径逐渐减小
D.核外电子排布相同的微粒化学性质也相同
高二化学选择题中等难度题查看答案及解析
-
下列关于氮族元素的叙述,正确的是( )
A.它们的单质是典型的非金属
B.主要化合价为-3、+5价
C.随着核电荷数的递增,失电子能力逐渐减弱
D.非金属性比相应的同期氧族元素弱高二化学选择题中等难度题查看答案及解析
-
(12分)下图是元素周期表中的一部分。
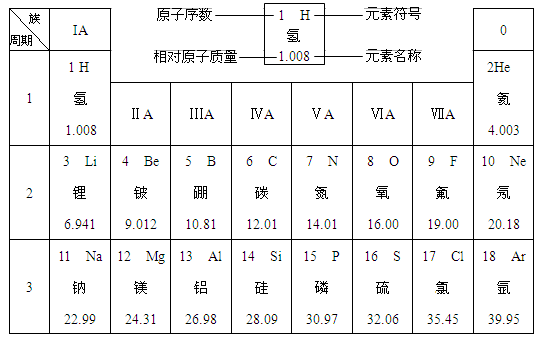
在元素周期表中,同一周期(横行)中的元素,除0族(最右纵行)元素外,从左到右原子序数依次增多,原子半径逐渐减小,在化学反应中,原子失电子能力逐渐减弱,得电子能力逐渐增强。
请回答:
(1)硅的相对原子质量为 ;原子序数为8的元素位于元素周期表的第 周期,元素符号为 ,它属于 (填“金属”或“非金属”)元素。
(2)原子半径:钠 镁(填“>”或“=”或“<”,下同),原子得电子能力:硫 氯。
高二化学填空题中等难度题查看答案及解析
-
下列说法中不正确的是 ( )
A. 同周期元素,随着核电荷数的增加,I1总体上呈现由小到大的变化趋势
B. 电离能越大,表示气态时该原子越易失电子
C. 元素的电负性越大,表示其原子在化合物中吸引电子能力越强
D. 电负性是相对的,所以没有单位
高二化学选择题中等难度题查看答案及解析
-
下列说法中不正确的是 ( )
A.同周期元素,随着核电荷数的增加,I1总体上呈现由小到大的变化趋势
B.电离能越大,表示气态时该原子越易失电子
C.元素的电负性越大,表示其原子在化合物中吸引电子能力越强
D.电负性是相对的,所以没有单位
高二化学单选题中等难度题查看答案及解析
-
下列关于元素周期律和元素周期表的说法错误的是
A. Na、Mg、Al元素的原子核外电子层数随着核电荷数的增加而增加
B. 第2周期元素从Li到F,元素原子得电子能力逐渐增强
C. 同一周期从左到右,随着元素原子序数的递增,其气态氢化物的稳定性增强
D. C、N、O、F的单质与H2化合越来越容易
高二化学选择题简单题查看答案及解析
-
下列有关物质性质的比较正确的是 ( )
①同主族元素的单质从上到下,非金属性减弱,熔点增高
②元素的最高正化合价在数值上等于它所在的族序数
③同周期主族元素的原子半径越小,越难失去电子
④元素的非金属性越强,它的气态氢化物水溶液的酸性越强.
⑤还原性:S2->Se2->Br->Cl-⑥酸性:HClO4>H2SO4>H3PO4>H2SiO3
A.①③ B.②④ C.③⑥ D.⑤⑥
高二化学选择题简单题查看答案及解析
-
根据原子结构及元素周期律的知识,下列推断正确的是
A. 同主族元素含氧酸的酸性随核电荷数的增加而减弱
B. 核外电子排布相同的微粒化学性质也相同
C. Cl-、S2-、Ca2+、K+半径逐渐减小
D.
与
得电子能力相同
高二化学选择题中等难度题查看答案及解析
-
下列说法正确的是
A. 碱金属随原子序数的增大,其熔沸点逐渐降低
B. 卤素单质随原子序数的增大
,其氧化性逐渐增强
C. 在周期表中,族序数都等于该族元素的最外层电子数
D. 非金属性最强的元素,其最高价氧化物对应水化物的酸性最强
高二化学选择题困难题查看答案及解析