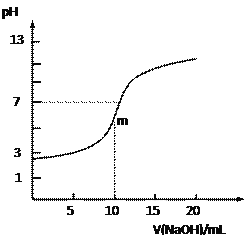
常温下,向10.0mL 0.10 mol·L-1某二元酸H2R溶液中滴加入同物质的量浓度的NaOH溶液,测得溶液的pH随NaOH溶液体积的变化如右图所示。下列说法中正确的是
A. 无法判断H2R是强酸还是弱酸
B. 曲线上m点时溶液中c(Na+)>c(HR-) >c(R2-)>c(H+)
C. HR-的电离能力大于水解能力
D. 溶液中c(Na+)+c(H+)=c(HR-)+c(R2-)+c(OH-)
高三化学单选题中等难度题
常温下,向10.0mL 0.10 mol·L-1某二元酸H2R溶液中滴加入同物质的量浓度的NaOH溶液,测得溶液的pH随NaOH溶液体积的变化如右图所示。下列说法中正确的是

A. 无法判断H2R是强酸还是弱酸
B. 曲线上m点时溶液中c(Na+)>c(HR-) >c(R2-)>c(H+)
C. HR-的电离能力大于水解能力
D. 溶液中c(Na+)+c(H+)=c(HR-)+c(R2-)+c(OH-)
高三化学单选题中等难度题
常温下,向10.0mL 0.10 mol·L-1某二元酸H2R溶液中滴加入同物质的量浓度的NaOH溶液,测得溶液的pH随NaOH溶液体积的变化如右图所示。下列说法中正确的是

A. 无法判断H2R是强酸还是弱酸
B. 曲线上m点时溶液中c(Na+)>c(HR-) >c(R2-)>c(H+)
C. HR-的电离能力大于水解能力
D. 溶液中c(Na+)+c(H+)=c(HR-)+c(R2-)+c(OH-)
高三化学单选题中等难度题查看答案及解析
常温下,向10.0mL 0.10 mol·L-1某二元酸H2R溶液中滴加入同物质的量浓度的NaOH溶液,测得溶液的pH随NaOH溶液体积的变化如右图所示。下列说法中正确的是

A. 无法判断H2R是强酸还是弱酸
B. 曲线上m点时溶液中c(Na+)>c(HR-) >c(R2-)>c(H+)
C. HR-的电离能力大于水解能力
D. 溶液中c(Na+)+c(H+)=c(HR-)+c(R2-)+c(OH-)
高三化学单选题中等难度题查看答案及解析
常温下,向10.0mL0.10mol·L-1某二元酸H2R溶液中滴入同物质的量浓度的NaOH溶液,测得溶液的pH随NaOH溶液体积的变化如图所示。下列说法中正确的是

A. HR-的电离能力大于水解能力
B. 曲线上m点时溶液中c(Na+)>c(HR-)>c(R2-)>c(H+)
C. 无法判断H2R是强酸还是弱酸
D. 溶液中c(Na+)+c(H+)=c(HR-)+c(R2-)+c(OH-)
高三化学单选题中等难度题查看答案及解析
常温下,用 0.10 mol/LKOH 溶液滴定 10.00mL 0.10 mol/L 某二元弱酸H2R 溶液,滴定曲线如图(混合溶液总体积看作混合前两种溶液体积之和),下列关系不正确的是
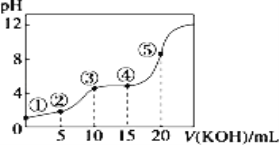
A.点②所示溶液中:c(K+)+c(H+)=c(HR-)+2c(R2-)+c(OH-)
B.点③所示溶液中:c(K+)> c(HR-)> c(R2-)>c(H2R)
C.点④所示溶液中:c(H2R)+ c(HR-)+ c(R2-)=0.04mol·L-1
D.点⑤所示溶液中:c(H+)= c(HR-)+2 c(H2R)+ c(OH-)
高三化学单选题简单题查看答案及解析
常温下,用0.10 mol/LKOH溶液滴定10.00mL 0.10 mol/L某二元弱酸H2R溶液,滴定曲线如图(混合溶液总体积看作混合前两种溶液体积之和),下列关系正确的是
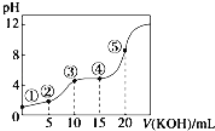
A. 点②所示溶液中:c(K+)+c(H+)=c(HR﹣)+c(R2﹣)+c(OH﹣)
B. 点③所示溶液中:c(K+)>c(HR﹣)>c(H2R)>c(R2﹣)
C. 点④所示溶液中:c(H2R)+c(HR﹣)+c(R2﹣)=0.04 mol.L-1
D. 点⑤所示溶液中:c(H+)=c(HR﹣)+2c(H2R)+c(OH﹣)
高三化学单选题困难题查看答案及解析
常温下,用0.10 mol·L-1KOH溶液滴定10.00mL 0.10mol·L-1某二元弱酸H2R溶液,所得滴定曲线如图所示。下列叙述正确的是
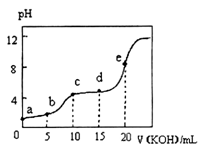
A.a点所示溶液中:<1012
B.c点所示溶液中:c(K+)>c(HR-)>c(H2R)>c(R2-)
C.e点所示溶液中:c(H+)=c(HR-)+2c(H2R)+c(OH-)
D.五个点中d点时c(HR-)最大
高三化学选择题困难题查看答案及解析
室温时,将0.10 mol/L的NaOH溶液滴入20.0 mL未知浓度的某一元酸HA溶液中,溶液pH随加入NaOH溶液体积变化曲线如图。下列有关说法不正确的是
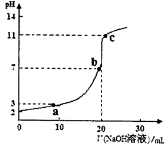
A.该一元酸溶液浓度为0.10mol/L
B.a、b、c点的水溶液导电性依次增强
C.室温时,HA的电离常数Kal×10-5
D.a点和c点所示溶液中H2O的电离程度相同
高三化学选择题困难题查看答案及解析
常温下,向浓度均为0.1 mol•L-1、体积均为100mL的两种一元酸HX、HY的溶液中,分别加入NaOH 固体,lg随加入NaOH的物质的量的变化如图所示(忽略加入NaOH固体导致溶液温度的变化)。下列叙述正确的是.
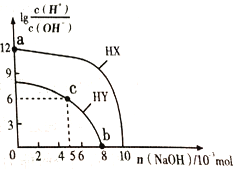
A. HX的酸性弱于HY
B. c点溶液中c(Y-)<c(HY)
C. a点由水电离出的c(H+)=10-12 mol•L-1
D. b点溶液中离子浓度大小关系为c(Y-)+c(HY)=c(Na+)+0.02 mol•L-1
高三化学单选题困难题查看答案及解析
常温下,向浓度均为0.1 mol·L-1、体积均为100 mL的两种一元酸HX、HY的溶液中,分别加入NaOH固体,lg随加入NaOH的物质的量的变化如图所示(忽略加入NaOH固体导致溶液温度与体积的变化)。下列叙述正确的是
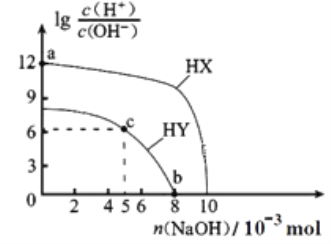
A. a点由水电离出的c(H+)=10-12 mol·L-1
B. b点时酸碱恰好完全中和
C. c点溶液中:c(Y-)>c(HY)
D. HX、HY均为弱酸且酸性HX>HY
高三化学单选题困难题查看答案及解析
室温时,将0.10 mol·L−1 NaOH溶液滴入20.00 mL未知浓度的某一元酸HA溶液中,溶液pH随加入NaOH溶液体积的变化曲线如图所示。当V(NaOH)=20.00 mL,二者恰好完全反应。则下列有关说法不正确的是
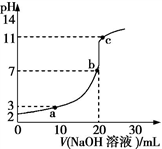
A. 该一元酸溶液浓度为0.10 mol·L−1
B. a、b、c点的水溶液导电性依次增强
C. 室温时,HA的电离常数Ka≈l×10−5
D. a点和c点所示溶液中H2O的电离程度相同
高三化学选择题中等难度题查看答案及解析