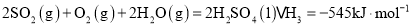-
Na2S粗品含有杂质,其纯化、含量测定方法如下。回答下列问题:
(1)粗品经水浸、过滤、__________________、洗涤、干燥等操作可以除去不溶性杂质,得到较纯的Na2S固体。
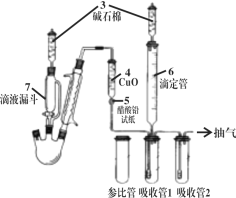
(2)国标中采用如图所示装置测定Na2S样品溶液中Na2CO3的百分含量(实验前,吸收管1、吸收管2、参比管中均装入组成相同的乙醇、丙酮混合溶液,该溶液吸收CO2后,颜色发生改变) 。
(步骤一)标定KOH标准溶液
准确称取w g邻苯二甲酸氢钾(KC8H5O4,摩尔质量为M g/mol)置于锥形瓶中,加入适量蒸馏水、2滴指示剂,用待标定的KOH溶液滴定至终点,消耗v mL KOH溶液。
①标定过程中应该选用的指示剂名称是______,理由是__________;
(已知邻苯二甲酸的电离平衡常数为Ka1=1.1×10-3,Ka2=4.0×10-6)
②KOH溶液的准确浓度为_____mol/L(用含M、v、w的代数式表示)
(步骤二)往三颈烧瓶中先后加入100mL 样品溶液、15 ml过氧化氢溶液(足量),连接好装置,加热并打开抽气装置;
(步骤三)上述反应完成后,从滴液漏斗中慢慢加入足量稀硫酸溶液,充分反应;
(步骤四)用装置6中的KOH标准溶液滴定吸收管1中的溶液至与参比管中溶液相同的颜色,3 min内不变色为终点。
③过氧化氢的作用是______;碱石棉的作用是__________;
④如果抽气速度过快,可能导致测定结果_________(填“偏高”、“偏低”或“无影响”);
⑤若步骤三中出现_______________________(填现象),说明实验失败,必须重新测定。
-
Na2S粗品含有杂质,其纯化、含量测定方法如下。回答下列问题:
(1)粗品经水浸、过滤、__________________、洗涤、干燥等操作可以除去不溶性杂质,得到较纯的Na2S固体。
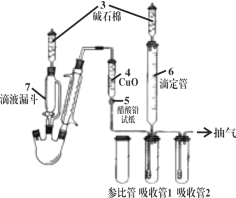
(2)国标中采用如图所示装置测定Na2S样品溶液中Na2CO3的百分含量(实验前,吸收管1、吸收管2、参比管中均装入组成相同的乙醇、丙酮混合溶液,该溶液吸收CO2后,颜色发生改变) 。
(步骤一)标定KOH标准溶液
准确称取w g邻苯二甲酸氢钾(KC8H5O4,摩尔质量为M g/mol)置于锥形瓶中,加入适量蒸馏水、2滴指示剂,用待标定的KOH溶液滴定至终点,消耗v mL KOH溶液。
①标定过程中应该选用的指示剂名称是______,理由是__________;
(已知邻苯二甲酸的电离平衡常数为Ka1=1.1×10-3,Ka2=4.0×10-6)
②KOH溶液的准确浓度为_____mol/L(用含M、v、w的代数式表示)
(步骤二)往三颈烧瓶中先后加入100mL 样品溶液、15 ml过氧化氢溶液(足量),连接好装置,加热并打开抽气装置;
(步骤三)上述反应完成后,从滴液漏斗中慢慢加入足量稀硫酸溶液,充分反应;
(步骤四)用装置6中的KOH标准溶液滴定吸收管1中的溶液至与参比管中溶液相同的颜色,3 min内不变色为终点。
③过氧化氢的作用是______;碱石棉的作用是__________;
④如果抽气速度过快,可能导致测定结果_________(填“偏高”、“偏低”或“无影响”);
⑤若步骤三中出现_______________________(填现象),说明实验失败,必须重新测定。
-
软锰矿是一种常见的锰矿物,主要成分是MnO2,常含有铁、铝元素形成的杂质。工业上,用软锰矿制取高锰酸钾的流程如下(部分条件和产物省略)
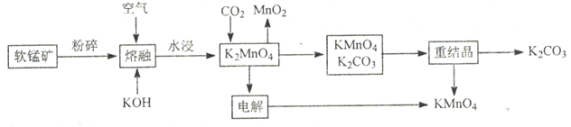
请回答下列问题
(1)在“水浸”过程中,提高K2MnO4浸出率(浸出的K2MnO4质量与“熔块”质量之比)的措施有____________________________________________(至少写出两点)
(2)“熔融”过程中发生的主要反应其化学方程式为_________________________________。
(3)CO2与K2MnO4反应的离子方程式为_________________________________。
(4)KMnO4与K2CO3能用重结晶的方法分离的原理是______________________。
(5)“电解”过程中使用的是惰性电极,则:
①阳极的电极反应方程式为______________________。
②阴极附近溶液的pH将___________(填“增大”、“减小”或“不变”)
(6)可用过氧化氢溶液滴定的方法测定高锰酸钾样品纯度。当达到滴定终点时,溶液中产生的现象为_________________________________。
(7)在上述生产过程中产生的M2+会对环境造成污染。工业上,通过调节pH使废水中的Mn2+形成Mn(OH)2沉淀。当pH=10时,溶液中的c(Mn2+)=___________mol/L(已知:Ksp[Mn(OH)2]=2.0×10-13。相关数据均在常温下测定)
-
以明矾 为原料制备Al、
为原料制备Al、 和
和 的工艺流程如下:
的工艺流程如下:
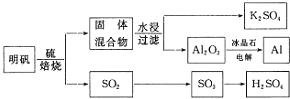
依据上述流程图回答下列问题:
 写出明矾和硫单质混合焙烧发生反应的化学方程式______.
写出明矾和硫单质混合焙烧发生反应的化学方程式______.
 从水浸后的滤液中得到
从水浸后的滤液中得到 晶体的方法是蒸发浓缩、______、过滤,实验室在蒸发浓缩过程中用到的主要仪器有______.
晶体的方法是蒸发浓缩、______、过滤,实验室在蒸发浓缩过程中用到的主要仪器有______.
 电解
电解 时加入冰晶石的作用是______.
时加入冰晶石的作用是______.
 以Al和
以Al和 为电极,NaOH溶液为电解液组成一种新型电池,放电时
为电极,NaOH溶液为电解液组成一种新型电池,放电时 转化为
转化为 ,该电池反应的化学方程式是______.
,该电池反应的化学方程式是______.
 焙烧产生的
焙烧产生的 可用于制硫酸.已知
可用于制硫酸.已知 ,101kPa时:
,101kPa时:


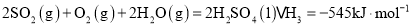
则 和
和 反应的热化学方程式是______.
反应的热化学方程式是______.
 焙烧948吨明矾
焙烧948吨明矾 ,若
,若 的利用率为
的利用率为 ,则可生产多少吨质量分数为
,则可生产多少吨质量分数为 的硫酸?
的硫酸?
-
粗铜中含有少量的锌、铁、银、金等金属和少量矿物杂质(与酸不反应).在实验室条件下以硫酸铜溶液为电解液,用电解的方法对粗铜提纯,并对阳极泥和电解液中金属进行回收和含量测定.
回答以下问题:
步骤一:电解精制:电解过程中,硫酸铜的浓度会______(选填:变大、不变、变小).
步骤二:电解完成后,对电解液进行处理:
(1)阳极泥的综合利用:
稀硝酸处理阳极泥得到硝酸银稀溶液,请写出该步反应的离子方程式:______.
残渣含有极少量的黄金,如何回收金,他们查阅了有关资料,了解到了一些有关金的知识,以下是他们获取的一些信息:
| 序号 | 反应 | 平衡常数 |
| 1 | Au+6HNO3(浓)=Au(NO3)3+3NO2↑+3H2O | <<1 |
| 2 | Au3++4Cl-=AuCl4- | >>1 |
从中可知,金很难与硝酸反应,但却可溶于王水(浓硝酸与盐酸按体积比1:3的混合物),请你简要解释金能够溶于王水的原因:______.
(2)滤液含量的测定:以下是该小组探究滤液的一个实验流程:

则100mL滤液中Cu2+ 的浓度为______mol•L-1,Fe2+的浓度为______mol•L-1.
-
某铝合金中含有合金元素镁、铜、硅,为了测定该合金中铝的含量,设计了如下实验,请回答有关问题:
(1)称取样品ag,称量时应该使用的主要仪器的名称是________。
(2)将样品溶解于足量的稀盐酸,过滤。滤液中主要含有________,滤渣中含有________,溶解、过滤用到的玻璃仪器是________,如果这一实验在月球上完成,它比在地球上做要________(填“容易”或“难”)。
(3)滤液中加过量的氢氧化钠溶液,过滤,有关反应的离子方程式为________。
(4)向步骤(3)的滤液中通入足量的二氧化碳气体,过滤,有关反应的离子方程式为________。
(5)步骤(4)过滤后的滤渣用蒸馏水洗涤数次,烘干并灼烧至恒重,冷却后称重,其质量为b g,原样品中铝的质量分数是________。
(6)若步骤(3)中加入氢氧化钠的量不足,则实验结果________(填“偏高”、“偏低”或“不影响”,下同);若步骤(5)中滤渣没有洗涤,则实验结果________,若滤渣灼烧不充分,则实验结果________。
-
硫酸亚铁晶体(FeSO4·7H2O)在医药上作补血剂。某课外小组的同学欲测定该补血剂中
铁元素的含量。实验步骤如下:
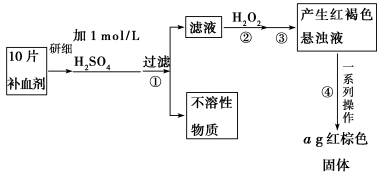
请回答下列问题:
(1)证明步骤①滤液中含有Fe2+的方法是:取样,先滴加KSCN溶液,再滴加________,该过程的现象为________。
(2)步骤②加入过量H2O2的目的是:______________________________________。
(3)步骤③中反应的离子方程式是:_______________________________________。
(4)步骤④中一系列处理的操作步骤:过滤、________、灼烧、________、称量。
(5)若实验中铁无损耗,则每片补血剂中含铁元素的质量为________g。
-
硫酸亚铁晶体(FeSO4·7H2O)在医药上作补血剂。某课外小组的同学欲测定该补血剂中铁元素的含量。实验步骤如下:
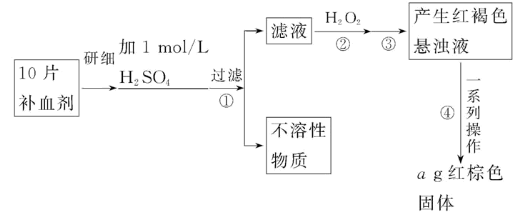
请回答下列问题:
(1)证明步骤①滤液中含有Fe2+的方法是:取样,先滴加KSCN溶液,再滴加_______,该过程的现象为:__________________________________________。
(2)步骤②加入过量H2O2的目的是:____________________________________。
(3)步骤③中反应的离子方程式是:_____________________________________。
(4)步骤④中一系列处理的操作步骤:过滤、_______、灼烧、_______、称量。
(5)若实验中铁无损耗,则每片补血剂中含铁元素的质量为_______g。
-
硫酸亚铁晶体(FeSO4·7H2O)在医药上作补血剂。某课外小组的同学欲测定该补血剂中铁元素的含量。实验步骤如下:
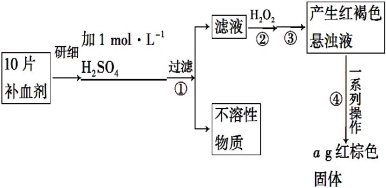
请回答下列问题:
(1)证明步骤①滤液中含有Fe2+的方法是:取样,先滴加KSCN溶液,再滴加 ,该过程的现象为______________________。
(2)步骤②加入过量H2O2的目的是 _______________________。
(3)步骤④中反应的化学方程式是 _______________________。
(4)步骤④中一系列处理的操作步骤:过滤、________、灼烧、 、称量。
-
硫酸亚铁晶体(FeSO4·7H2O)在医药上作补血剂。某课外小组的同学欲测定该补血剂中铁元素的含量。实验步骤如下:
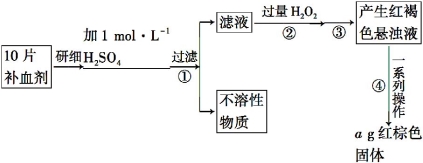
请回答下列问题:
(1)证明步骤①滤液中含有Fe2+的方法是取样,先滴加KSCN溶液,再滴加 ,该过程的现象为________ 。
(2)步骤②加入过量H2O2的目的是________
。
(3)步骤③中反应的离子方程式是________
。
(4)步骤④中一系列处理的操作步骤:过滤、 、灼烧、
、称量。
(5)若实验中铁无损耗,则每片补血剂中含铁元素的质量为 g。