-
以明矾 为原料制备Al、
为原料制备Al、 和
和 的工艺流程如下:
的工艺流程如下:
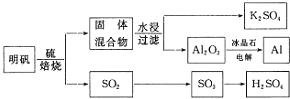
依据上述流程图回答下列问题:
 写出明矾和硫单质混合焙烧发生反应的化学方程式______.
写出明矾和硫单质混合焙烧发生反应的化学方程式______.
 从水浸后的滤液中得到
从水浸后的滤液中得到 晶体的方法是蒸发浓缩、______、过滤,实验室在蒸发浓缩过程中用到的主要仪器有______.
晶体的方法是蒸发浓缩、______、过滤,实验室在蒸发浓缩过程中用到的主要仪器有______.
 电解
电解 时加入冰晶石的作用是______.
时加入冰晶石的作用是______.
 以Al和
以Al和 为电极,NaOH溶液为电解液组成一种新型电池,放电时
为电极,NaOH溶液为电解液组成一种新型电池,放电时 转化为
转化为 ,该电池反应的化学方程式是______.
,该电池反应的化学方程式是______.
 焙烧产生的
焙烧产生的 可用于制硫酸.已知
可用于制硫酸.已知 ,101kPa时:
,101kPa时:


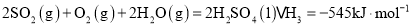
则 和
和 反应的热化学方程式是______.
反应的热化学方程式是______.
 焙烧948吨明矾
焙烧948吨明矾 ,若
,若 的利用率为
的利用率为 ,则可生产多少吨质量分数为
,则可生产多少吨质量分数为 的硫酸?
的硫酸?
-
(12分) 明矾石的主要成分是K2SO4·Al2(SO4)3·2Al 2O3·6H2O,此外还含有少量Fe2O3杂质。利用明矾石制备氢氧化铝的流程如下:
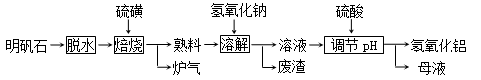
回答下列问题:
(1)“焙烧”过程中发生的反应为2Al2(SO4)3+3S  2Al 2O3 +9SO2 ,其中氧化剂为________________________。
2Al 2O3 +9SO2 ,其中氧化剂为________________________。
(2)“溶解”时反应的离子方程式为________________________。
(3)“调节pH”后过滤、洗涤Al(OH)3沉淀,证明已洗涤干净的实验操作和现象是
________________________。
(4)调节pH时使用的是质量浓度(单位体积溶液所含溶质的质量)为882 g/L 的H2SO4 ,配制1L该溶液,需用量筒量取质量分数为98﹪的硫酸(密度是1.8g/cm3)
________________________mL
(5)“废渣”、“母液”中可回收的物质分别是________________________。
-
(10分) 明矾石的主要成分是K2SO4·Al2(SO4)3·2Al 2O3·6H2O,此外还含有少量Fe2O3杂质。利用明矾石制备氢氧化铝的流程如下:
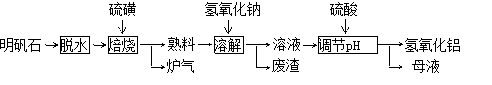
回答下列问题:
(1)“焙烧”过程中发生的反应为2Al2(SO4)3+3S  2Al 2O3 +9SO2 ,其中氧化剂为 。
2Al 2O3 +9SO2 ,其中氧化剂为 。
(2)“溶解”时反应的离子方程式为 。
(3)“调节pH”后过滤、洗涤Al(OH)3沉淀,证明已洗涤干净的实验操作和现象是 。
(4)调节pH时使用的是质量浓度(单位体积溶液所含溶质的质量)为882 g/L 的H2SO4 ,配制1L该溶液,需用量筒量取质量分数为98﹪的硫酸(密度是1.8g/cm3) mL。
(5)“母液”中可回收的物质是 。
-
铝是一种应用广泛的金属,工业上用 和冰晶石(
和冰晶石( )混合熔融电解制得。
)混合熔融电解制得。
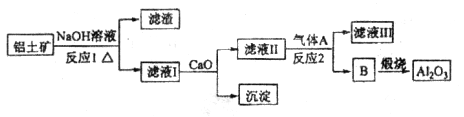
①铝土矿的主要成分是 和
和 等。从铝土矿中提炼
等。从铝土矿中提炼 的流程如下:
的流程如下:
②以萤石( )和纯碱为原料制备冰晶石的流程如下:
)和纯碱为原料制备冰晶石的流程如下:
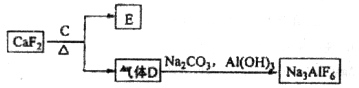
回答下列问题:
(1)写出反应1的化学方程式_________________________、________________________________;
(2)滤液Ⅰ中加入 生成的沉淀是___________,反应2的离子方程式为____ ___________________
生成的沉淀是___________,反应2的离子方程式为____ ___________________
(3)E常用作制作豆腐的添加剂,化合物C是____,写出由D制备冰晶石的化学方程式_______________;
-
铬(Cr)硬度大、抗腐蚀性和耐磨性好,具有广泛的应用前景。一种以铬铁矿(含FeCr2O4及少量Al2O3、SiO2等)为原料制备金属铬的工艺流程如下:
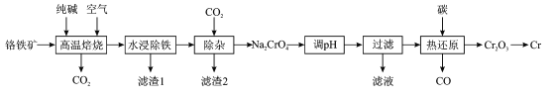
回答下列问题:
(1)“高温焙烧”中主要反应的化学方程式为____。
(2)为提高“水浸”的浸取率,除了适当升高温度,还可采取的措施是____。
(3)“滤渣1”是一种红棕色固体,为检验其中的金属元素,可选择的常用试剂是____。“滤渣2”的主要成分是__________。
(4)“调pH”的目的是____。
(5)“热还原”主要是利用焦炭与重铬酸盐得到Cr2O3和另一种固体产物,该固体产物可返回__________工序循环使用。
(6)可用铝热法还原Cr2O3制备铬单质,铝热反应中镁带的作用是____;还可用惰性电极电解硫酸铬钾[KCr(SO4)2]溶液制备,阴极的电极反应式为____。
-
(10分)以Al(OH)3、H2SO4、工业(NH4)2SO4(含FeSO4)为原料制备透明氧化铝陶瓷的工艺流程如下:
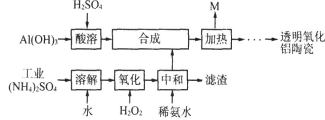
回答下列问题:
(1)写出氧化步骤中发生的主要反应的离子方程式 。
(2)如何检验中和液中的杂质离子已完全除尽? 。
(3)固体NH4Al(SO4)2·12H2O[相对分子质量:453]在加热时,固体残留率随温度的变化如图所示。

633℃时剩余固体的成分化学式为 。
(4)综上分析,流程图中M的主要成分的化学式为 ,M可用一种物质吸收以实现循环利用,该物质的名称是 。
-
明矾石的主要成分是K2SO4·Al2(SO4)3·2Al2O3·6H2O,还含有少量Fe2O3杂质。利用明矾石制备氢氧化铝的流程如下:
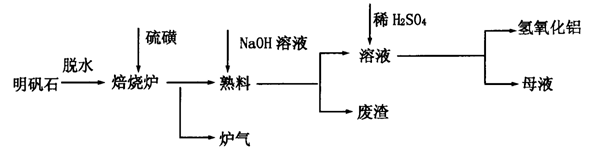
(1)焙烧炉中发生反应的化学方程式为2Al2(SO4)3+3S 2Al2O3+9SO2,该反应的氧化剂是_______。若生成l molAl2O3,则转移的电子数为__________________。
2Al2O3+9SO2,该反应的氧化剂是_______。若生成l molAl2O3,则转移的电子数为__________________。
(2)熟料溶解时,反应的离子方程式为___________________________________________。
(3)母液中溶质主要成分的化学式为_____________________________________________。
(4)将标准状况下1.12L炉气通入100mL 0.5mol·L-1NaOH溶液中,得到一种酸性溶液,则该溶液中各种离子浓度由大到小的排列顺序为____________________________。
(5)检验废渣中主要成分的方法是_____________________________________________________(写出操作步骤、现象及结论)。
-
明矾石的主要成分是K2SO4·Al2(SO4)3·2Al2O3·6H2O,还含有少量Fe2O3杂质。利用明矾石制备氢氧化铝的流程如下:
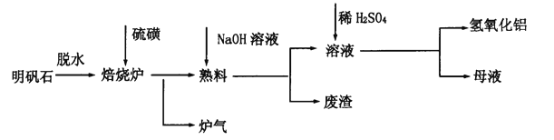
(1)焙烧炉中发生反应的化学方程式为2Al2(SO4)3+3S 2Al2O3+9SO2,该反应的氧化剂是_______。若生成l molAl2O3,则转移的电子数为__________________。
2Al2O3+9SO2,该反应的氧化剂是_______。若生成l molAl2O3,则转移的电子数为__________________。
(2)熟料溶解时,反应的离子方程式为___________________________________________。
(3)母液中溶质主要成分的化学式为_____________________________________________。
(4)将标准状况下1.12L炉气通入100mL 0.5mol·L-1NaOH溶液中,得到一种酸性溶液,则该溶液中各种离子浓度由大到小的排列顺序为____________________________。
(5)检验废渣中主要成分的方法是_____________________________________________________(写出操作步骤、现象及结论)。
-
(9分)硝矾石的主要成分是K2SO4·Al2(SO4)3·2Al2O3·6H2O及少量氧化铁。
利用明矾石制备K2SO4的工艺流程如下所示:
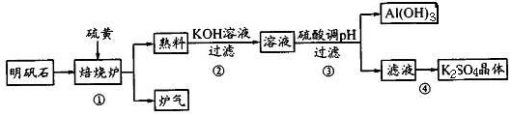
(1)焙烧炉中发生如下反应,请在方程式中表示出电子转移的方向和数目
2Al2(SO4)3+3S 2Al2O3+9SO2↑
2Al2O3+9SO2↑
(2)步骤②涉及Al2O3的离子方程式为____。
(3)步骤③调pH生成AI{OH)。的离子方程式为____;不能用CO2来调pH,理由是
.
(4)步骤④的主要操作步骤是___ _,过滤、洗涤和干燥
(5)炉气回收可做多种用途,请举一例:__ _。
-
硝矾石的主要成分是K2SO4·Al2(SO4)3·2Al2O3·6H2O及少量氧化铁。
利用明矾石制备K2SO4的工艺流程如下所示:
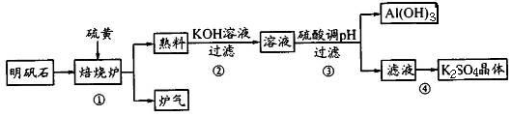
(1)焙烧炉中发生如下反应,请用双线桥法在方程式中表示出电子转移的方向和数目
2Al2(SO4)3+3S 2Al2O3+9SO2↑
2Al2O3+9SO2↑
(2)步骤②涉及Al2O3的离子方程式为 。
(3)步骤③调pH生成AI{OH)。的离子方程式为 ;不能用CO2来调pH,理由是 。
(4)步骤④的主要操作步骤是 ,过滤、洗涤和干燥
为原料制备Al、
和
的工艺流程如下:

写出明矾和硫单质混合焙烧发生反应的化学方程式______.
从水浸后的滤液中得到
晶体的方法是蒸发浓缩、______、过滤,实验室在蒸发浓缩过程中用到的主要仪器有______.
电解
时加入冰晶石的作用是______.
以Al和
为电极,NaOH溶液为电解液组成一种新型电池,放电时
转化为
,该电池反应的化学方程式是______.
焙烧产生的
可用于制硫酸.已知
,101kPa时:
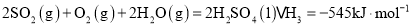
和
反应的热化学方程式是______.
焙烧948吨明矾
,若
的利用率为
,则可生产多少吨质量分数为
的硫酸?










