-
合理应用和处理含氮的化合物,在生产、生活中有重要意义。回答下列问题:
(1)在紫外光照射的条件下,氯气与偏二甲肼[(CH3)2NNH2]可快速反应,偏二甲肼转化为CH3OH和N2,该反应的化学方程式为______________________________。
(2)连二次硝酸(H2N2O2)是一种二元酸,可用于制N2O气体。25℃时,连二次硝酸的电离常数Ka1=6.17×10-8,Ka2=2.88×10-12
①25℃时0.1mol・L-1NaHN2O2溶液中离子浓度由大到小的顺序为____________________________。
②25℃时向0.1 mol・L-1连二次硝酸溶液中逐滴滴入NaOH溶液,当溶液的pH=10时,C(N2O22-)/ C(H2N2O2)=________。
(3)亚硝酰氯可由NO与Cl2反应制得,反应原理为2NO(g)+ Cl2 (g) 2C1NO(g)。按投料比n(NO):n(Cl2) =2:1把NO和Cl2充入一恒压的密闭容器中发生上述反应,NO的平衡转化率与温度T的关系如图所示:
2C1NO(g)。按投料比n(NO):n(Cl2) =2:1把NO和Cl2充入一恒压的密闭容器中发生上述反应,NO的平衡转化率与温度T的关系如图所示:


①该反应的△H_____(填“>”“<”或“=”)0。
②M点时容器内NO的体积分数为____。
③若反应一直保持在P压强条件下进行,则M点的平衡常数Kp=____________,(用含P的表达式表示)。
(4)工业上电解NO制备NH4NO3可以变废为宝,其工作原理如图所示、电解时阳极反应式为___________,为使电解产物全部转化为NH4NO3,需要补充物质A,物质A化学式为__________。
-
中学教材中常见的金属和非金属元素及其化合物在工业和生活中有重要应用,请回答下列问题:
(1)从海水中提溴是将Cl2:通入浓海水中,生成溴单质,而氯气氧化溴离子是在酸性条件下进行的,其目的是避免__________________。
(2)ClO2是高效、低毒的消毒剂,工业上用KClO3与Na2SO3在H2SO4存在下制得ClO2,该反应氧化剂与还原剂物质的量之比为____。
(3)磷的含氧酸有多种形式,如H3 PO4 、H3PO2(次磷酸)、H3PO3(亚磷酸)等。H3PO3与NaOH反应只生成Na2HPO3和NaH2PO3两种盐,写出H3PO3的第二步电离方程式_________________。H3PO3和碘水反应,棕黄色褪去,再滴加AgNO3溶液,有黄色沉淀生成:请写出H3PO3和碘水反应的化学方程式____。
(4)高铁酸钾(K2FeO4)是一种新型高效水处理剂,其中Fe元素的化合价是____:高铁酸钾溶于水放出氧气,能杀菌消毒,生成能吸附水中悬浮物的物质。用一个离子方程式表示高铁酸钾处理水的过程____。
(5)镁一H2O2酸性燃料电池的反应机理为Mg+H2O2 +2H+==Mg2++2H2O,则正极反应式为________。常温下若起始电解质溶液pH =1,则pH =2时溶液中Mg2+浓度为________。已知Ksp[ Mg(OH)2]=5.6×10 -12,当溶液pH =6时,_____(填“有”或“没有”)Mg( OH)2沉淀。
-
中学教材中常见的金属和非金属元素及其化合物在工业和生活中有重要应用,请回答下列问题:
(1)从海水中提溴是将Cl2:通入浓海水中,生成溴单质,而氯气氧化溴离子是在酸性条件下进行的,其目的是避免__________________。
(2)ClO2是高效、低毒的消毒剂,工业上用KClO3与Na2SO3在H2SO4存在下制得ClO2,该反应氧化剂与还原剂物质的量之比为____。
(3)磷的含氧酸有多种形式,如H3 PO4 、H3PO2(次磷酸)、H3PO3(亚磷酸)等。H3PO3与NaOH反应只生成Na2HPO3和NaH2PO3两种盐,写出H3PO3的第二步电离方程式_________________。H3PO3和碘水反应,棕黄色褪去,再滴加AgNO3溶液,有黄色沉淀生成:请写出H3PO3和碘水反应的化学方程式____。
(4)高铁酸钾(K2FeO4)是一种新型高效水处理剂,其中Fe元素的化合价是____:高铁酸钾溶于水放出氧气,能杀菌消毒,生成能吸附水中悬浮物的物质。用一个离子方程式表示高铁酸钾处理水的过程____。
(5)镁一H2O2酸性燃料电池的反应机理为Mg+H2O2 +2H+==Mg2++2H2O,则正极反应式为________。常温下若起始电解质溶液pH =1,则pH =2时溶液中Mg2+浓度为________。已知Ksp[ Mg(OH)2]=5.6×10 -12,当溶液pH =6时,_____(填“有”或“没有”)Mg( OH)2沉淀。
-
碳及其化合物在工农业生产和日常生活中有广泛的应用,对其研究具有重要意义。
回答下列问题:
(1)利用活性炭的___作用可去除水中的悬浮杂质。
(2)炭黑可以活化氧分子得到活化氧(O*),活化氧可以快速将SO2氧化为SO3,其活化过程中的能量变化如图所示:
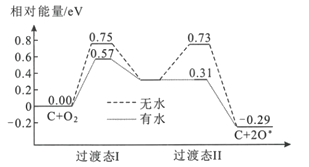
活化过程中有水时的活化能降低了___eV。在酸雨的形成过程中,炭黑起:___作用。
(3)已知:CO(g)+2H2(g) CH3OH(g) ∆H,经测定不同温度下该反应的浓度平衡常数如下:
CH3OH(g) ∆H,经测定不同温度下该反应的浓度平衡常数如下:

①该反应的△H___0(填“>”或“<");250℃时,某时刻测得反应体系中c(CO)=0.4mol·L-1、c(H2)=0.4mol·L-1、c(CH3OH)=0.8mol·L-1,则此时v正__v逆(填“>”、“=”或“<”)。.
②某温度下,在2L刚性容器中,充入0.8molCO和1.6molH2,压强为p,tmin后达到平衡,测得压强为 P。则v(H2)=____mol·L-1·min-1,平衡时的Kp=____。
P。则v(H2)=____mol·L-1·min-1,平衡时的Kp=____。
(4)科研人员设计了甲烷燃料电池电解饱和食盐水装置如图所示,电池的电解质是掺杂了Y2O3与ZrO2的固体,可在高温下传导O2-。
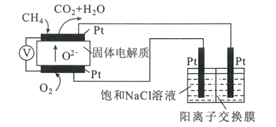
①该电池工作时负极反应方程式为____。
②用该电池电解100mL饱和食盐水,若在两极产生的气体体积分别为V1L、V2L(标准状况),且V1>V2,则电解所得溶液的c(OH-)=____mol·L-1(忽略气体溶解和溶液体积变化)。
-
碳及其化合物在工农业生产和日常生活中有广泛的应用,对其研究具有重要意义。
回答下列问题:
(1)利用活性炭的___作用可去除水中的悬浮杂质。
(2)炭黑可以活化氧分子得到活化氧(O*),活化氧可以快速将SO2氧化为SO3,其活化过程中的能量变化如图所示:
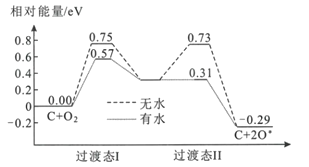
活化过程中有水时的活化能降低了___eV。在酸雨的形成过程中,炭黑起:___作用。
(3)已知:CO(g)+2H2(g) CH3OH(g) ∆H,经测定不同温度下该反应的浓度平衡常数如下:
CH3OH(g) ∆H,经测定不同温度下该反应的浓度平衡常数如下:

①该反应的△H___0(填“>”或“<");250℃时,某时刻测得反应体系中c(CO)=0.4mol·L-1、c(H2)=0.4mol·L-1、c(CH3OH)=0.8mol·L-1,则此时v正__v逆(填“>”、“=”或“<”)。.
②某温度下,在2L刚性容器中,充入0.8molCO和1.6molH2,压强为p,tmin后达到平衡,测得压强为 P。则v(H2)=____mol·L-1·min-1,平衡时的Kp=____。
P。则v(H2)=____mol·L-1·min-1,平衡时的Kp=____。
(4)科研人员设计了甲烷燃料电池电解饱和食盐水装置如图所示,电池的电解质是掺杂了Y2O3与ZrO2的固体,可在高温下传导O2-。
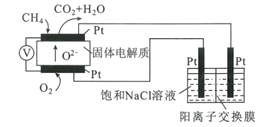
①该电池工作时负极反应方程式为____。
②用该电池电解100mL饱和食盐水,若在两极产生的气体体积分别为V1L、V2L(标准状况),且V1>V2,则电解所得溶液的c(OH-)=____mol·L-1(忽略气体溶解和溶液体积变化)。
-
(15分)合理应用和处理氮的化合物,在生产生活中有重要意义。
(1)尿素[CO(NH2)2]是一种高效化肥,也是一种化工原料。
①以尿素为原料在一定条件下发生反应:CO(NH2)2 (s) + H2O(l) == 2 NH3(g)+CO2(g) △H = +133.6 kJ/mol。该反应的化学平衡常数的表达式K= 。关于该反应的下列说法正确的是 (填序号)。
2 NH3(g)+CO2(g) △H = +133.6 kJ/mol。该反应的化学平衡常数的表达式K= 。关于该反应的下列说法正确的是 (填序号)。
a.从反应开始到平衡时容器中混合气体的平均相对分子质量保持不变
b.在平衡体系中增加水的用量可使该反应的平衡常数增大
c.降低温度使尿素的转化率增大
②尿素在一定条件下可将氮的氧化物还原为氮气。
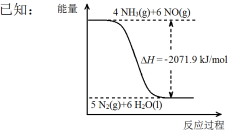
结合①中信息,尿素还原NO(g)的热化学方程式是 。
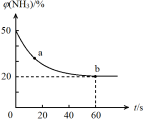
②密闭容器中以等物质的量的NH3和CO2为原料,在120 ℃、催化剂作用下反应生成尿素:CO2(g) +2NH3(g) ==CO (NH2)2 (s) +H2O(g),混合气体中NH3的物质的量百分含量[(NH3)]随时间变化关系如图所示。则a点的正反应速率V(正)(CO2) b点的逆反应速率V(逆)(CO2)(填“>”、“=”或“<”);氨气的平衡转化率是 。
==CO (NH2)2 (s) +H2O(g),混合气体中NH3的物质的量百分含量[(NH3)]随时间变化关系如图所示。则a点的正反应速率V(正)(CO2) b点的逆反应速率V(逆)(CO2)(填“>”、“=”或“<”);氨气的平衡转化率是 。
(2)NO2会污染环境,可用Na2CO3溶液吸收NO2并生成CO2。已知9.2 g NO2和Na2CO3溶液完全反应时转移电子0.1 mol,此反应的离子方程式是 ;恰好反应后,使溶液中的CO2完全逸出,所得溶液呈弱碱性,则溶液中离子浓度大小关系是c(Na+)>______。
-
合理应用和处理氮的化合物,在生产生活中有重要意义。
(1)尿素[CO(NH2)2]是一种高效化肥,也是一种化工原料。
①以尿素为原料在一定条件下发生反应:CO(NH2)2 (s) + H2O(l) 2 NH3(g)+CO2(g) △H=+133.6 kJ/mol。该反应的化学平衡常数的表达式K= 。关于该反应的下列说法正确的是 (填序号)。
2 NH3(g)+CO2(g) △H=+133.6 kJ/mol。该反应的化学平衡常数的表达式K= 。关于该反应的下列说法正确的是 (填序号)。
a. 从反应开始到平衡时容器中混合气体的平均相对分子质量保持不变
b. 在平衡体系中增加水的用量可使该反应的平衡常数增大
c. 降低温度使尿素的转化率增大
②尿素在一定条件下可将氮的氧化物还原为氮气。
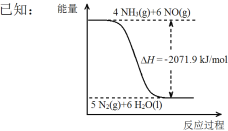
结合①中信息,尿素还原NO(g)的热化学方程式是 。
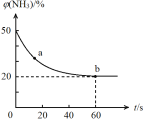
③密闭容器中以等物质的量的NH3和CO2为原料,在120 ℃、催化剂作用下反应生成尿素:CO2(g) +2NH3(g) CO (NH2)2 (s) +H2O(g),混合气体中NH3的物质的量百分含量[φ(NH3)]随时间变化关系如图所示。则a点的正反应速率v正(CO2) b点的逆反应速率v(逆)(CO2)(填“>”、“=”或“<”);氨气的平衡转化率是 。
CO (NH2)2 (s) +H2O(g),混合气体中NH3的物质的量百分含量[φ(NH3)]随时间变化关系如图所示。则a点的正反应速率v正(CO2) b点的逆反应速率v(逆)(CO2)(填“>”、“=”或“<”);氨气的平衡转化率是 。
(2)NO2会污染环境,可用Na2CO3溶液吸收NO2并生成CO2。已知9.2 g NO2和Na2CO3溶液完全反应时转移电子0.1 mol,此反应的离子方程式是 ;恰好反应后,使溶液中的CO2完全逸出,所得溶液呈弱碱性,则溶液中存在的所有离子浓度大小关系是c(Na+)>________。
-
合理应用和处理氮的化合物,在生产生活中有重要意义。
(1)尿素[CO(NH2)2]是一种高效化肥,也是一种化工原料。
①以尿素为原料在一定条件下发生反应:CO(NH2)2 (s) + H2O(l) 2 NH3(g)+CO2(g) △H=+133.6 kJ/mol。该反应的化学平衡常数的表达式K= 。关于该反应的下列说法正确的是 (填序号)。
2 NH3(g)+CO2(g) △H=+133.6 kJ/mol。该反应的化学平衡常数的表达式K= 。关于该反应的下列说法正确的是 (填序号)。
a. 从反应开始到平衡时容器中混合气体的平均相对分子质量保持不变
b. 在平衡体系中增加水的用量可使该反应的平衡常数增大
c. 降低温度使尿素的转化率增大
②尿素在一定条件下可将氮的氧化物还原为氮气。
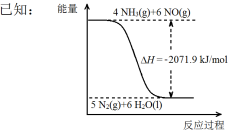

结合①中信息,尿素还原NO(g)的热化学方程式是 。
③密闭容器中以等物质的量的NH3和CO2为原料,在120 ℃、催化剂作用下反应生成尿素:CO2(g) +2NH3(g) CO (NH2)2 (s) +H2O(g),混合气体中NH3的物质的量百分含量[φ(NH3)]随时间变化关系如图所示。则a点的正反应速率v正(CO2) b点的逆反应速率v(逆)(CO2)(填“>”、“=”或“<”);氨气的平衡转化率是 。
CO (NH2)2 (s) +H2O(g),混合气体中NH3的物质的量百分含量[φ(NH3)]随时间变化关系如图所示。则a点的正反应速率v正(CO2) b点的逆反应速率v(逆)(CO2)(填“>”、“=”或“<”);氨气的平衡转化率是 。
(2)NO2会污染环境,可用Na2CO3溶液吸收NO2并生成CO2。已知9.2 g NO2和Na2CO3溶液完全反应时转移电子0.1 mol,此反应的离子方程式是 ;恰好反应后,使溶液中的CO2完全逸出,所得溶液呈弱碱性,则溶液中存在的所有离子浓度大小关系是c(Na+)>________。
-
合理应用和处理氮的化合物,在生产生活中有重要意义。
(1)尿素[CO(NH2)2]是一种高效化肥,也是一种化工原料。
①以尿素为原料在一定条件下发生反应:CO(NH2)2 (s) + H2O(l) 2 NH3(g)+CO2(g) △H=+133.6 kJ/mol。该反应的化学平衡常数的表达式K= 。关于该反应的下列说法正确的是 (填序号)。
2 NH3(g)+CO2(g) △H=+133.6 kJ/mol。该反应的化学平衡常数的表达式K= 。关于该反应的下列说法正确的是 (填序号)。
a. 从反应开始到平衡时容器中混合气体的平均相对分子质量保持不变
b. 在平衡体系中增加水的用量可使该反应的平衡常数增大
c. 降低温度使尿素的转化率增大
②尿素在一定条件下可将氮的氧化物还原为氮气。
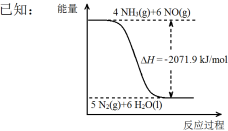
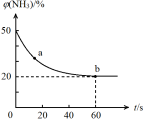
结合①中信息,尿素还原NO(g)的热化学方程式是 。
③密闭容器中以等物质的量的NH3和CO2为原料,在120 ℃、催化剂作用下反应生成尿素:CO2(g) +2NH3(g) CO (NH2)2 (s) +H2O(g),混合气体中NH3的物质的量百分含量[φ(NH3)]随时间变化关系如图所示。则a点的正反应速率v正(CO2) b点的逆反应速率v(逆)(CO2)(填“>”、“=”或“<”);氨气的平衡转化率是 。
CO (NH2)2 (s) +H2O(g),混合气体中NH3的物质的量百分含量[φ(NH3)]随时间变化关系如图所示。则a点的正反应速率v正(CO2) b点的逆反应速率v(逆)(CO2)(填“>”、“=”或“<”);氨气的平衡转化率是 。
(2)NO2会污染环境,可用Na2CO3溶液吸收NO2并生成CO2。已知9.2 g NO2和Na2CO3溶液完全反应时转移电子0.1 mol,此反应的离子方程式是 ;恰好反应后,使溶液中的CO2完全逸出,所得溶液呈弱碱性,则溶液中存在的所有离子浓度大小关系是c(Na+)>________。
-
合理应用和处理元素化合物,在生产生活中有重要意义。尿素[CO(NH2)2]是一种高效化肥,也是一种化工原料。
(1)以尿素为原料在一定条件下发生反应:CO(NH2)2(s)+H2O(l) 2NH3(g)+CO2(g) △H=+133.6 kJ·mol-1。该反应的化学平衡常数的表达式K=_________。
2NH3(g)+CO2(g) △H=+133.6 kJ·mol-1。该反应的化学平衡常数的表达式K=_________。
关于该反应的下列说法正确的是________(填字母序号)。
A.从反应开始到平衡时容器中混合气体的平均相对分子质量保持不变
B.在平衡体系中增加水的用量可使该反应的平衡常数增大
C.当容器中NH3的体积分数不再改变时,反应处于平衡状态
(2)尿素在一定条件下可将氮的氧化物还原为氮气。
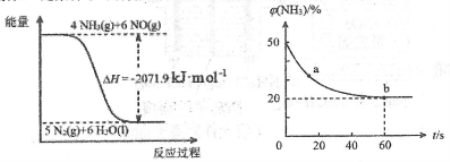
根据图像,结合(1)中信息,尿素还原NO(g)的热化学方程式是_____________________________________。
(3)密闭容器中以等物质的量的NH3和CO2为原料,在120℃、催化剂作用下反应生成尿素:CO2(g)+NH3(g) CO(NH2)2(s)+H2O(g),混合气体中NH3 的物质的量百分含量[φ(NH3)%]随时间变化关系如图所示。则a点的正反应速率V正(CO2)_________b点的逆反应速率V逆(CO2)(填“>”、“=”或“<”);氨气的平衡转化率是___________。
CO(NH2)2(s)+H2O(g),混合气体中NH3 的物质的量百分含量[φ(NH3)%]随时间变化关系如图所示。则a点的正反应速率V正(CO2)_________b点的逆反应速率V逆(CO2)(填“>”、“=”或“<”);氨气的平衡转化率是___________。
2C1NO(g)。按投料比n(NO):n(Cl2) =2:1把NO和Cl2充入一恒压的密闭容器中发生上述反应,NO的平衡转化率与温度T的关系如图所示:
















