-
以硫铁矿 主要成分为
主要成分为 ,还有少量CuS、
,还有少量CuS、 等杂质
等杂质 为原料制备绿矾晶体
为原料制备绿矾晶体 的工艺流程如下:
的工艺流程如下:
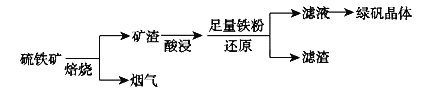
 “酸浸”过程,矿渣中的
“酸浸”过程,矿渣中的 与稀
与稀 反应的离子方程式___________________。
反应的离子方程式___________________。
 烟气中的
烟气中的 会污染环境,可用足量氨水吸收,写出该反应的离子方程式________。
会污染环境,可用足量氨水吸收,写出该反应的离子方程式________。
 滤液中金属阳离子的检验方法________________________________。
滤液中金属阳离子的检验方法________________________________。
 溶液制备绿矾晶体过程中要保持
溶液制备绿矾晶体过程中要保持 过量,理由___________________________。
过量,理由___________________________。 结合化学用语说明原因
结合化学用语说明原因
 燃料细菌脱硫法是用氧化亚铁硫杆菌
燃料细菌脱硫法是用氧化亚铁硫杆菌 对硫铁矿进行催化脱硫,同时得到
对硫铁矿进行催化脱硫,同时得到 溶液。其过程如图所示:
溶液。其过程如图所示:
已知总反应为:
 将过程I离子方程式补充完整
将过程I离子方程式补充完整
____FeS2+_____Fe3++______ _______=7Fe2++________S2O32-+_____ _____
 过程II反应的离子方程式___________________________________。
过程II反应的离子方程式___________________________________。
 绿矾晶体在空气中易被氧化。取
绿矾晶体在空气中易被氧化。取 样品,加水完全溶解,用酸化的
样品,加水完全溶解,用酸化的 溶液滴定至终点,消耗
溶液滴定至终点,消耗 溶液
溶液 。反应原理:
。反应原理: 。则绿矾晶体纯度的计算式为_______________。
。则绿矾晶体纯度的计算式为_______________。 摩尔质量为
摩尔质量为
-
以硫铁矿(主要成分为FeS2,还有少量CuS、SiO2等杂质)为原料制备绿矾晶体(FeSO4·7H2O)的工艺流程如下:

(1)“酸浸”过程,矿渣中的Fe2O3与稀H2SO4反应的离子方程式________。
(2)烟气中的SO2会污染环境,可用足量氨水吸收,写出该反应的离子方程式________。
(3)滤液中金属阳离子的检验方法__________。
(4)FeSO4溶液制备绿矾晶体过程中要保持H2SO4过量,理由____。(结合化学用语说明原因)
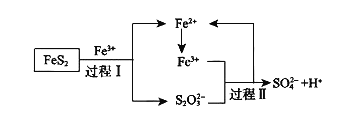
(5)燃料细菌脱硫法是用氧化亚铁硫杆菌(T.f)对硫铁矿进行催化脱硫,同时得到FeSO4溶液。其过程如图所示:
已知总反应为:FeS2+14Fe3++8H2O=2SO42-+15Fe2++16H+
①将过程I离子方程式补充完整
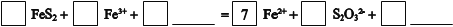 _____
_____
②过程II反应的离子方程式__________。
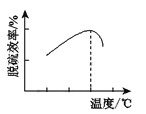
③研究发现,用氧化亚铁硫杆菌(T.f)脱硫,温度过高脱硫效率降低(如图),可能的原因是____。
(6)绿矾晶体在空气中易被氧化。取X g样品,加水完全溶解,用酸化的amol·L-1K2Cr2O7溶液滴定至终点,消耗K2Cr2O7溶液b mL。反应原理:6Fe2++Cr2O72-+14H+ =6Fe3++2Cr3++7H2O。则绿矾晶体纯度的计算式为_____。(FeSO4·7H2O摩尔质量为278 g/mol)
-
以硫铁矿(主要成分为FeS2,还有少量CuS、SiO2等杂质)为原料制备绿矾晶体(FeSO4·7H2O)的工艺流程如下:
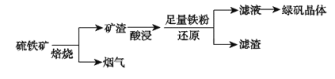
(1)“酸浸”过程,矿渣中的Fe2O3与稀H2SO4反应的离子方程式________。
(2)烟气中的SO2会污染环境,可用足量氨水吸收,写出该反应的离子方程式________。
(3)滤液中金属阳离子的检验方法__________。
(4)FeSO4溶液制备绿矾晶体过程中要保持H2SO4过量,理由________。(结合化学用语说明原因)
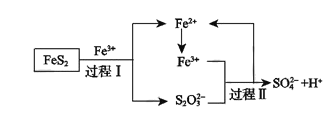
(5)燃料细菌脱硫法是用氧化亚铁硫杆菌(T.f)对硫铁矿进行催化脱硫,同时得到FeSO4溶液。其过程如图所示:
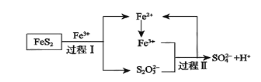
已知总反应为:FeS2+14Fe3++8H2O=2SO42-+15Fe2++16H+
①将过程I离子方程式补充完整______FeS2+______Fe3++_______ ______=7Fe2++______S2O32-+____ ______
②过程II反应的离子方程式________________________________________。
(6)绿矾晶体在空气中易被氧化。取X g样品,加水完全溶解,用酸化的amol·L-1K2Cr2O7溶液滴定至终点,消耗K2Cr2O7溶液b mL。反应原理:6Fe2++Cr2O72-+14H+ =6Fe3++2Cr3++7H2O。则绿矾晶体纯度的计算式为______________。(FeSO4·7H2O摩尔质量为278 g/mol)
-
硫酸亚铁铵 又称莫尔盐,是浅绿色晶体。用硫铁矿
又称莫尔盐,是浅绿色晶体。用硫铁矿 主要含
主要含 、
、 等
等 制备莫尔盐的流程如下:
制备莫尔盐的流程如下:
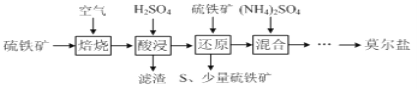
已知:“还原”时, 与
与 不反应,
不反应, 通过反应Ⅰ、Ⅱ被还原,反应Ⅰ如下:
通过反应Ⅰ、Ⅱ被还原,反应Ⅰ如下:
 写出“还原”时
写出“还原”时 与
与 发生还原反应Ⅱ的离子方程式:__________。
发生还原反应Ⅱ的离子方程式:__________。
实验室检验“还原”已完全的方法是__________。
 “还原”前后溶液中部分离子的浓度见下表
“还原”前后溶液中部分离子的浓度见下表 溶液体积变化忽略不计
溶液体积变化忽略不计 ,请计算反应Ⅰ、Ⅱ中被还原的Fe
,请计算反应Ⅰ、Ⅱ中被还原的Fe 的物质的量之比__________。
的物质的量之比__________。
 称取
称取 新制莫尔盐,溶于水配成250mL溶液。取
新制莫尔盐,溶于水配成250mL溶液。取 该溶液加入足量的
该溶液加入足量的 溶液,得到白色沉淀
溶液,得到白色沉淀 ;另取
;另取 该溶液用
该溶液用 酸性溶液滴定,当
酸性溶液滴定,当 恰好完全被还原为
恰好完全被还原为 时,消耗溶液的体积为
时,消耗溶液的体积为 。试确定莫尔盐的化学式
。试确定莫尔盐的化学式 请写出计算过程)________________。
请写出计算过程)________________。
-
实验室以软锰矿(主要成分为MnO2,还有少量FeO、Fe2O3、MgO和Al2O3杂质)为原料制备高锰酸钾的流程如下图:
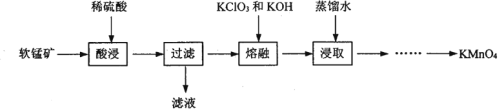
(1) “酸浸”需要加热的目的是__________,此过程中发生反应的离子方程式是______________。(任写一条)
(2) “熔融”过程中,MnO2被KC1O3氧化成K2MnO4。
①该反应的化学方程式为_____________________。
②加入KC1O3应过量的原因除了提高MnO2利用率,还有_________________.
③将适量KClO3和KOH混合均匀后在坩埚内高温反应,应选用坩埚为__________。(选填序号)
a.石英坩埚 b.铁坩埚 c.氧化铝坩埚
(3)己知:①MnO42-只存在于强碱环境(pH>13.5)中,当pH降低时,MnO42-会歧化为MnO4-和MnO2;②饱和碳酸钾溶液的pH约为12.3,饱和碳酸氢钾溶液的pH约为8.8;③相关物质的溶解度曲线如下图。
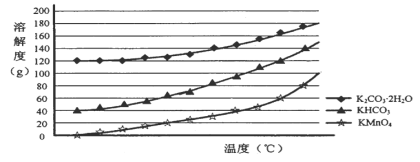
请补充完整由浸取液制备KMnO4晶体的实验方案:向浸取液中缓缓通入CO2,_____________,低温供干得KMnO4晶体。
-
实验室以软锰矿(主要成分为MnO2,还有少量FeO、Fe2O3、MgO和Al2O3杂质)为原料制备高锰酸钾的流程如下图:
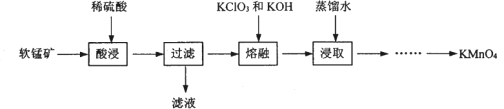
(1) “酸浸”需要加热的目的是__________,此过程中发生反应的离子方程式是______________。(任写一条)
(2) “熔融”过程中,MnO2被KC1O3氧化成K2MnO4。
①该反应的化学方程式为_____________________。
②加入KC1O3应过量的原因除了提高MnO2利用率,还有_________________.
③将适量KClO3和KOH混合均匀后在坩埚内高温反应,应选用坩埚为__________。(选填序号)
a.石英坩埚 b.铁坩埚 c.氧化铝坩埚
(3)己知:①MnO42-只存在于强碱环境(pH>13.5)中,当pH降低时,MnO42-会歧化为MnO4-和MnO2;②饱和碳酸钾溶液的pH约为12.3,饱和碳酸氢钾溶液的pH约为8.8;③相关物质的溶解度曲线如下图。
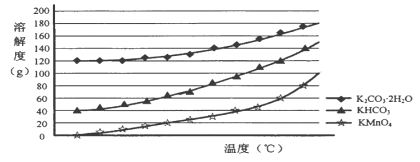
请补充完整由浸取液制备KMnO4晶体的实验方案:向浸取液中缓缓通入CO2,_____________,低温供干得KMnO4晶体。
-
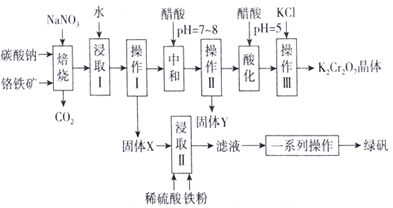
工业上可用铬铁矿(主要成分可表示为FeO·Cr 2O3,还含有Al2O3、MgCO3、SiO2 等杂质)为原料制备重铬酸钾晶体和绿矾的流程如下:
已知:Ⅰ.常见离子沉淀的pH范围
| Fe3+ | Al3+ | Mg2+ | SiO32- | AlO2- |
| 开始沉淀 | 1.9 | 4.2 | 8.1 | 9.5 | 10.2 |
| 沉淀完全 | 3.2 | 5.3 | 9.4 | 8.0 | 8.5 |
Ⅱ.焙烧过程中主要发生反应:2FeO·Cr2O3+4Na2CO3+7NaNO3=4Na2Cr2O4+Fe2O3+ 4CO2 ↑+7NaNO2。
(1)绿矾的化学式为________。
(2)焙烧后的混合物中除含有Na2Cr2O4、NaNO2和过量的Na2CO3、NaNO3外,还含有NaAlO2和Na2SiO3等物质,则焙烧过程中NaAlO2的化学方程式为___________________________。
(3)固体Y的主要成分为________(填写化学式)。
(4)酸化过程中用醋酸调节pH=5的目的为________________________;若pH调节的过低,NO2-可被氧化为NO3-,其离子方程式为_________________________________。
(5)调节pH=5后,加入KCl 控制一定条件,可析出K2Cr2O7晶体,说明溶解度的大小:K2Cr2O7________Na2Cr2O7(填“大于”或“小于”)。
(6)流程中的一系列操作为____________________________________。
-
某工厂用软锰矿(主要成分是MnO2,含少量Al2O3和SiO2)和闪锌矿(主要成分是ZnS,含少量FeS、CuS等杂质)为原料制备MnO2和Zn(干电池原料),其简化流程如下:
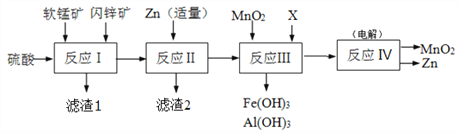
已知:反应Ⅰ中所有金属元素均以离子形式存在。
回答下列问题:
(1)滤渣1中除了SiO2以外,还有一种淡黄色物质,该物质是由MnO2、CuS与硫酸共热时产生的,请写出该反应的离子方程式________________________________。
(2)反应Ⅱ中加入适量金属锌的目的是为了回收某种金属,滤渣2的主要成分是______(填名称)。
(3)反应Ⅲ中MnO2的作用是______,另外一种物质X可以是______。(填字母代号)
a.MgO b.Zn(OH)2 c.Cu2(OH)2CO3 d.MnCO3
(4)反应Ⅳ中电极均是惰性电极,写出阳极电极反应式_______________。本工艺可以循环利用的物质有MnO2、Zn和_____。
(5)已知:H2S的电离常数K1=1.0×10−7,K2=7.0×10−15。0.1 mol/L NaHS的pH___7(填“>”“=”或“<”),理由是________________________________________。
(6)在废水处理领域中常用H2S将Mn2+转化为MnS除去,向含有0.020 mol·L−1 Mn2+废水中通入一定量的H2S气体,调节溶液的pH=a,当HS−浓度为1.0×10−4 mol·L−1时,Mn2+开始沉淀,则a=________。[已知:Ksp(MnS)=1.4×10−15]
-
某工厂用软锰矿(主要成分是MnO2,含少量Al2O3和SiO2)和闪锌矿(主要成分是ZnS,含少量FeS、CuS等杂质)为原料制备MnO2和Zn(干电池原料),其简化流程如下:
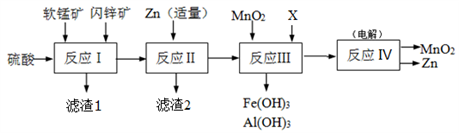
已知:反应Ⅰ中所有金属元素均以离子形式存在。
回答下列问题:
(1)滤渣1中除了SiO2以外,还有一种淡黄色物质,该物质是由MnO2、CuS与硫酸共热时产生的,请写出该反应的离子方程式________________________________。
(2)反应Ⅱ中加入适量金属锌的目的是为了回收某种金属,滤渣2的主要成分是______(填名称)。
(3)反应Ⅲ中MnO2的作用是______,另外一种物质X可以是______。(填字母代号)
a.MgO b.Zn(OH)2 c.Cu2(OH)2CO3 d.MnCO3
(4)反应Ⅳ中电极均是惰性电极,写出阳极电极反应式_______________。本工艺可以循环利用的物质有MnO2、Zn和_____。
(5)已知:H2S的电离常数K1=1.0×10−7,K2=7.0×10−15。0.1 mol/L NaHS的pH___7(填“>”“=”或“<”),理由是________________________________________。
(6)在废水处理领域中常用H2S将Mn2+转化为MnS除去,向含有0.020 mol·L−1 Mn2+废水中通入一定量的H2S气体,调节溶液的pH=a,当HS−浓度为1.0×10−4 mol·L−1时,Mn2+开始沉淀,则a=________。[已知:Ksp(MnS)=1.4×10−15]
-
某工厂用软锰矿(主要成分是MnO2,含少量Al2O3和SiO2)和闪锌矿(主要成分是ZnS,含少量FeS、CuS等杂质)为原料制备MnO2和Zn(干电池原料),其简化流程如下:
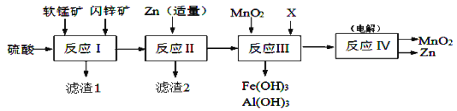
已知:反应Ⅰ中所有金属元素均以离子形式存在。有关常数:Ksp[Al(OH)3]=1.0×10-33、Ksp[Fe(OH)3]=3.0×10-39、Ksp[Mn(OH)2]=2.0×10-13、Ksp[Zn(OH)2]=1.0×10-17、Ksp(MnCO3)=2.0×10-11、Ka1(H2CO3)=4.0×10-7、Ka2(H2CO3)=5.6×10-11。回答下列问题:
(1)滤渣1中除了SiO2以外,还有一种淡黄色物质,该物质是由MnO2、CuS与硫酸共热时产生的,请写出该反应的离子方程式____________________________。
(2)反应Ⅱ中加入适量金属锌的目的是为了回收某种金属,滤渣2的主要成分是___________。
(3)反应Ⅲ中MnO2的作用是_______________________,若反应后溶液中Mn2+、Zn2+均为0.1mol·L-1,需调节溶液pH范围为_______________(溶液中,当一种离子的浓度小于10-6mol/L时可认为已不存在),X可以是_________。(填字母代号)
a.MgO b.Zn(OH)2 c.Cu2(OH)2CO3 d.MnCO3
(4)反应Ⅳ中电极均是惰性电极,写出阳极电极反应式________________________。本工艺可以循环利用的物质有MnO2、Zn和_________。
(5)MnCO3有多种用途。废水处理领域中常用NH4HCO3溶液将Mn2+转化为MnCO3,该反应的离子方程式为______。试通过题述有关数据简要计算说明该反应能进行的原因:____________________________。
主要成分为
,还有少量CuS、
等杂质
为原料制备绿矾晶体
的工艺流程如下:

“酸浸”过程,矿渣中的
与稀
反应的离子方程式___________________。
烟气中的
会污染环境,可用足量氨水吸收,写出该反应的离子方程式________。
滤液中金属阳离子的检验方法________________________________。
溶液制备绿矾晶体过程中要保持
过量,理由___________________________。
结合化学用语说明原因
燃料细菌脱硫法是用氧化亚铁硫杆菌
对硫铁矿进行催化脱硫,同时得到
溶液。其过程如图所示:

将过程I离子方程式补充完整
过程II反应的离子方程式___________________________________。
绿矾晶体在空气中易被氧化。取
样品,加水完全溶解,用酸化的
溶液滴定至终点,消耗
溶液
。反应原理:
。则绿矾晶体纯度的计算式为_______________。
摩尔质量为


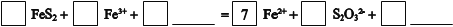 _____
_____










