常温下,将体积均为1 mL、浓度均为0.10 mol/L的XOH和X2CO3溶液分别加水稀释至体积为V mL,pH随lg V的变化情况如图所示,下列叙述中正确的是
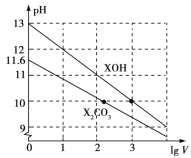
A. XOH是弱碱
B. pH=10的两种溶液中的c(X+):XOH>X2CO3
C. 已知H2CO3的电离平衡常数Ka1远大于Ka2,则Ka2约为1.0×10−10.2
D. 当lg V=2时,若X2CO3溶液的温度升高,溶液碱性增强,则减小
高三化学单选题中等难度题
常温下,将体积均为1 mL、浓度均为0.10 mol/L的XOH和X2CO3溶液分别加水稀释至体积为V mL,pH随lg V的变化情况如图所示,下列叙述中正确的是

A. XOH是弱碱
B. pH=10的两种溶液中的c(X+):XOH>X2CO3
C. 已知H2CO3的电离平衡常数Ka1远大于Ka2,则Ka2约为1.0×10−10.2
D. 当lg V=2时,若X2CO3溶液的温度升高,溶液碱性增强,则减小
高三化学单选题中等难度题
常温下,将体积均为1 mL、浓度均为0.10 mol/L的XOH和X2CO3溶液分别加水稀释至体积为V mL,pH随lg V的变化情况如图所示,下列叙述中正确的是

A. XOH是弱碱
B. pH=10的两种溶液中的c(X+):XOH>X2CO3
C. 已知H2CO3的电离平衡常数Ka1远大于Ka2,则Ka2约为1.0×10−10.2
D. 当lg V=2时,若X2CO3溶液的温度升高,溶液碱性增强,则减小
高三化学单选题中等难度题查看答案及解析
1mL浓度均为0.10mol/L的XOH和X2CO3溶液分别加水稀释(溶液体积为V),溶液pH随lgV的变化情况如图所示,则下列说法正确的是

A. XOH是弱碱
B. pH=10的溶液中c(X+):XOH大于X2CO3
C. 已知H2CO3的电离平衡常数Ka1远远大于Ka2,则Ka2约为1.0×10-10.2
D. 当lgV=2时,升高X2CO3溶液温度,溶液碱性增强且c(HCO3-)/c(CO32-)减小
高三化学单选题困难题查看答案及解析
体积为1ml、浓度均为0.10mol/L的XOH和X2CO3溶液分别加水稀释至体积为V,pH随lgV的变化情况如图所示,下列叙述中正确的是
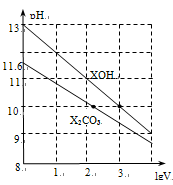
A.XOH是强碱
B.pH=10的两种溶液中的c(X+):XOH大于X2CO3
C.已知H2CO3的电离平衡常数Ka1远远大于Ka2,则Ka2约为1×10-10.2
D.当lgV=2时,若X2CO3溶液升高温度,溶液碱性增强,则c(HCO3-)/c(CO32-)减小
高三化学选择题困难题查看答案及解析
体积为1 mL、浓度均为0.10 mol/L的XOH和X2CO3溶液分别加水稀释至体积为V,pH随lgV的变化情况如图所示,下列叙述中正确的是
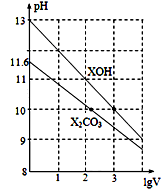
A. XOH是弱碱
B. pH=10的两种溶液中的c(X+):XOH大于X2CO3
C. 已知H2CO3的电离平衡常数Ka1远远大于Ka2,则Ka2约为1.0×10-10.2
D. 当lgV=2时,若X2CO3溶液升高温度,溶液碱性增强,则c(HCO3-)/c(CO32-)减小
高三化学选择题极难题查看答案及解析
体积为1 mL、浓度均为0.10 mol/L的XOH和X2CO3溶液分别加水稀释至体积为V,pH随lgV的变化情况如图所示,下列叙述中正确的是
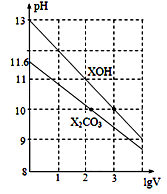
A. XOH是弱碱
B. pH=10的两种溶液中的c(X+):XOH大于X2CO3
C. 已知H2CO3的电离平衡常数Ka1远远大于Ka2,则Ka2约为1.0×10-10.2
D. 当lgV=2时,若X2CO3溶液升高温度,溶液碱性增强,则c(HCO3-)/c(CO32-)减小
高三化学选择题极难题查看答案及解析
体积为1 mL、浓度均为0.10 mol/L的XOH和X2CO3溶液分别加水稀释至体积为V,pH随lgV的变化情况如图所示,下列叙述中正确的是
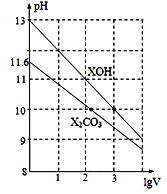
A. XOH是弱碱
B. pH=10的两种溶液中的c(X+):XOH大于X2CO3
C. 已知H2CO3的电离平衡常数Ka1远远大于Ka2,则Ka2约为1.0×10-10.2
D. 当lgV=2时,若X2CO3溶液升高温度,溶液碱性增强,则c(HCO3-)/c(CO32-)减小
高三化学选择题极难题查看答案及解析
常温下体积为1ml、浓度均为0.10mol/L的XOH和X2CO3溶液分别加水稀释至体积为V,pH随lgV的变化情况如图所示,下列叙述中正确的是
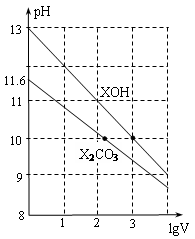
A.pH=10的两种溶液中的c(X+):XOH大于X2CO3
B.已知常温下,0.1 mol·L-1 XHCO3溶液的pH=8.31,则Ka1(H2CO3)·Ka2(H2CO3) >Kw
C.已知H2CO3的电离平衡常数Ka1远远大于Ka2,则Ka2约为1.0×10-10.2
D.当lgV=2时,若X2CO3溶液升高温度,溶液碱性增强,则c(HCO3-)/c(CO32-)减小
高三化学选择题极难题查看答案及解析
体积为1ml、浓度均为0.10mol/L的XOH和X2CO3溶液分别加水稀释至体积为V,pH随lgV的变化情况如图所示,下列叙述中正确的是( )

A.XOH是弱碱
B.pH=10的两种溶液中的c(X+):XOH大于X2CO3
C.已知H2CO3的电离平衡常数Ka1远远大于Ka2,则Ka2约为1.0×10-10.2
D.当lgV=2时,若X2CO3溶液升高温度,溶液碱性增强,则c(HCO3-)/c(CO32-)减小
高三化学选择题极难题查看答案及解析
体积为1ml、浓度均为0.10mol/L的XOH和X2CO3溶液分别加水稀释至体积为V,pH随lgV的变化情况如图所示,下列叙述中正确的是( )
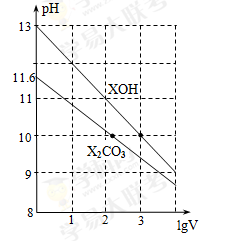
A.XOH是弱碱
B.pH=10的两种溶液中的c(X+):XOH大于X2CO3
C.已知H2CO3的电离平衡常数Ka1远远大于Ka2,则Ka2约为1.0×10-10.2
D.当lgV=2时,若X2CO3溶液升高温度,溶液碱性增强,则c(HCO3-)/c(CO32-)减小
高三化学选择题困难题查看答案及解析
常温下,浓度均为0.10mol/L、体积均为V0的HA和HB溶液,分别加水稀释至体积V,pH随lg的变化如图所示,下列叙述正确的是
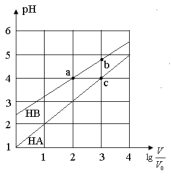
A.相同条件下NaA溶液的pH大于NaB溶液的pH
B.溶液中水的电离程度:a=c>b
C.该温度下HB的电离平衡常数约等于1.11×10-5
D.当lg=3时,若两溶液同时升高温度,则
减小
高三化学选择题中等难度题查看答案及解析