-
SO2在生产、生活中有着广泛的用途。
(l)请你列举一个SO2在生活中的用途 。
(2)SO2在工业上常用于硫酸生产:2SO2(g)+02(g)  2SO3(g),该反应在一定条件下进行时的热效应如图1所示,则其逆反应的活化能为____。
2SO3(g),该反应在一定条件下进行时的热效应如图1所示,则其逆反应的活化能为____。
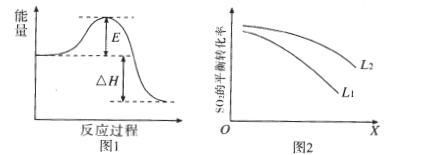
(3)图2中L、X表示物理量温度或压强,依据题中信息可判断:①X表示的物理量是____,理由是____ ;②L1____L2(填“>”,“<”或“:”)。
(4)在容积固定的密闭容器中,起始时充入0.2molSO2和0.1 molO2反应体系起始总压强0.1 MPa。反应在一定的温度下达到平衡时SO2的转化率为90%。该反应的压强平衡常数Kp=____ (用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(5)利用原电池原理,也可用SO2和O2来制备硫酸,该电池用多孔材料作电极。请写出该电池负极的电极反应式 。
-
SO2在生产、生活中有着广泛的用途。
(1)请你列举一个SO2在生活中的用途:______________________。
(2)SO2在工业上常用于硫酸生产:2SO2(g)+O2(g) 2SO3(g),该反应在一定条件下进行时的热效应如图所示,则其逆反应的活化能为__________________。
2SO3(g),该反应在一定条件下进行时的热效应如图所示,则其逆反应的活化能为__________________。
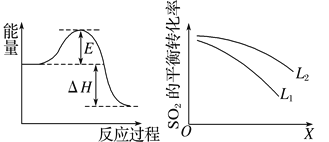
(3)上图中L、X表示物理量温度或压强,依据题中信息可判断:
①X表示的物理量是_________________________,
②L1________(填“>”“<”或“=”)L2。
(4)在容积固定的密闭容器中,起始时充入0.2molSO2和0.1molO2,反应体系起始总压强为0.1MPa。反应在一定的温度下达到平衡时SO2的转化率为90%。该反应的压强平衡常数Kp=__________(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(5)利用原电池原理,也可用SO2和O2来制备硫酸,该电池用多孔材料作电极。请写出该电池负极的电极反应式:__________________________________________。
-
氯气是工业生产中的重要原料,含氯消毒剂在生活中有着广泛的用途。
(1)工业生产通过电解饱和食盐水获取大量氯气,化学方程式为________。
(2)氯气可用于制取84消毒液(有效成分为NaClO),离子方程式为________。
(3)下列措施能增强84消毒液杀菌能力的是________。
A.加入适量醋酸 B.加入适量亚硫酸 C.加入少量NaOH粉末
(4)氯气与氢氧化钠溶液反应,若所得溶液恰好为中性,则溶液中离子浓度关系正确的是________。
A.c(Na+) + c(H+) = c(OH-) + c(Cl-)
B.c(Na+) = c(ClO-) + c(Cl-)
C.c(Na+) = 2c(ClO-) + c(HClO)
(5)84消毒液不能用于消毒钢铁(含Fe、C)制品,易发生电化学腐蚀,钢铁制品表面生成红褐色沉淀。正极反应为________。
-
碳和硅属于同主族元素,在生活生产中有着广泛的用途。
(1)甲烷可用作燃料电池,将两个石墨电极插入KOH溶液中,向两极分别通入CH4和O2,构成甲烷燃料电池,通入CH4的一极,其电极反应式是 ;
CH4催化还原NOX可以消除氮氧化物的污染,有望解决汽车尾气污染问题,反应如下:
CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) △H=-574kJ·mol-1
CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g) △H=-1160kJ·mol-1
则NO2被甲烷还原为N2的热化学方程式为_____________________________________
(2)已知H2CO3 HCO3-+ H+ Ka1(H2CO3)=4.45×10-7
HCO3-+ H+ Ka1(H2CO3)=4.45×10-7
HCO3- CO32-+H+ Ka2(HCO3-)=5.61×10-11
CO32-+H+ Ka2(HCO3-)=5.61×10-11
HA H++A- Ka(HA)=2.95×10-8
H++A- Ka(HA)=2.95×10-8
请依据以上电离平衡常数,写出少量CO2通入到NaA溶液中的离子方程式
___________________________。
(3) 在T温度时,将1.0molCO2和3.0molH2充入2L密闭恒容器中,可发生反应的方程式为CO2 (g) + 3H2(g)  CH3OH(g) + 2H2O(g) 。充分反应达到平衡后,若容器内的压强与起始压强之比为a :1,则CO2转 化率为______,当a=0.875时,该条件下此反应的平衡常数为_______________(用分数表示)。
CH3OH(g) + 2H2O(g) 。充分反应达到平衡后,若容器内的压强与起始压强之比为a :1,则CO2转 化率为______,当a=0.875时,该条件下此反应的平衡常数为_______________(用分数表示)。
(4)氮化硅(Si3N4)是一种新型陶瓷材料,它可由石英(SiO2)与焦炭在高温的氮气流中反应生成,已知该反应的平衡常数表达式K=[c(CO)]6/[c(N2)]2,若已知CO生成速率为v(CO)=6mol·L-1·min-1,则N2消耗速率为v(N2)= ;该反应的化学方程式为________________________________________。
-
【化学选修3:物质结构与性质】铝、铁在生活、生产中有着广泛的用途,请回答下列问题。
(1)Fe2+的最外层电子排布式____________。元素Fe与Mn的第三电离能分别为I3(Fe)、I3(Mn),则I3(Fe)______I3(Mn)(填“>”、“<")。
(2)第四周期中,与Al原子未成对电子数相同的金属元素有____种。气态氯化铝的分子组成为(AlCl3)2,其中Al、Cl均达8e-稳定结构,Al原子的杂化方式为__________。根据等电子原理,AlO2-的空间构型为_____。
(3)Fe(CO)5的熔点为-20℃,沸点为103℃,易溶于乙醚,其晶体类型为______,晶体中σ键和π键的数目之比为______。
(4)科学家们发现某些含铁的物质可催化尿素合成肼(N2H4),沸点:N2H4>C2H6的主要原因为____________。
(5)FeO晶体的晶胞如图所示,己知:FeO晶体的密度为ρg/cm3,NA代表阿伏加德罗常数的值。在该晶胞中,与Fe2+紧邻且等距离的Fe2+数目为_____;Fe2+与O2-最短核间距为______pm(用ρ和NA表示)。

-
化学在生产生活中有着广泛的应用。下列有关说法正确的是
A. SO2溶液用于吸收溴蒸气是因为SO2具有漂白性
B. 小苏打用于焙制糕点是因为小苏打具有碱性
C. SiO2用于生产光导纤维是因为SiO2能与碱反应
D. 波尔多液用作农药是因为铜盐能使蛋白质变性
-
铝、铁在生活、生产中有着广泛的用途,请回答下列问题。
(1)Fe2+的最外层电子排布式____________。元素Fe与Mn的第三电离能分别为I3(Fe)、I3(Mn),则I3(Fe)______I3(Mn)(填“>”、“<")。
(2)第四周期中,与Al原子未成对电子数相同的金属元素有____种。气态氯化铝的分子组成为(AlCl3)2,其中Al、Cl均达8e-稳定结构,Al原子的杂化方式为__________。根据等电子原理,AlO2-的空间构型为_____。
(3)Fe(CO)5的熔点为-20℃,沸点为103℃,易溶于乙醚,其晶体类型为______,晶体中σ键和π键的数目之比为______。
(4)科学家们发现某些含铁的物质可催化尿素合成肼(N2H4),沸点:N2H4>C2H6的主要原因为____________。
(5)FeO晶体的晶胞如图所示,己知:FeO晶体的密度为ρg/cm3,NA代表阿伏加德罗常数的值。在该晶胞中,与Fe2+紧邻且等距离的Fe2+数目为_____;Fe2+与O2-最短核间距为______pm(用ρ和NA表示)。

-
化学在生活中有着广泛的应用,下列对应关系正确的是( )
| 化学性质 | 实际应用 |
| A | SiO2是酸性氧化物 | 生产光导纤维 |
| B | Fe2(SO2)3易水解 | 脱除天然气中H2S |
| C | 乙烯能发生加聚反应 | 用作水果的催熟剂 |
| D | NH3具有还原性 | 将柴油车尾气中NO转化为N2 |
A.A B.B C.C D.D
-
KMnO4在生产和生活中有着广泛的用途,某化学小组在实验室制备KMnO4并探究其性质。请回答下列问题:
(一)KMnO4的制备。
步骤Ⅰ.先利用如图甲所示装置由MnO2制备K2MnO4 。
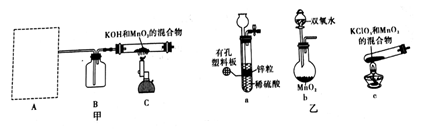
(1)装置A应选用图乙中的______________ (填“a”、“b”或“c”)。
(2)装置B中所盛试剂的名称为_________________。
(3)装置C处制备K2MnO4的化学方程式为________________________。
步骤Ⅱ.由K2MnO4制备KMnO4。已知: K2MnO4易溶于水,水溶液呈墨绿色。
主要过程如下:
①充分反应后,将装置C处所得固体加水溶解,过滤;
②向①的滤液中通入足量CO2,过滤出生成的MnO2;
③将②的滤液经过一系列实验操作从而获得KMnO4晶体。
(4)过程③干燥KMnO4时,温度不宜过高的原因是_______________。
(5)过程②向①的滤液中通入足量CO2,可观察到的现象为______________________; 该步反应中氧化剂与还原剂的物质的量之比为____________。
(二)KMnO4的性质。
(6) KMnO4具有强氧化性,某化学学习小组利用2KMnO4+5H2C2O4+3H2SO4 =K2SO4+2MnSO4+10CO2 +8H2O的反应原理,用配制好的0.10mol/LKMnO4溶液来测定 H2C2O4溶液的浓度,酸性KMnO4溶液应放在_______滴定管中(填“酸式”或“碱式”),滴定时所得的实验数据如下表,试计算所测H2C2O4溶液的浓度为_______mol·L-1。
| 实验次数编号 | 待测液体积(mL) | 滴入的标准液体积(mL) |
| 1 | 25.00 | 28.95 |
| 2 | 25.00 | 25.05 |
| 3 | 25.00 | 24.95 |
-
KMnO4在生产和生活中有着广泛用途,某化学小组在实验室制备KMnO4并探究其性质。请回答:
(一) KMnO4的制备,分步骤I、II两步进行。
步骤I.先利用下图所示装置制备K2MnO4
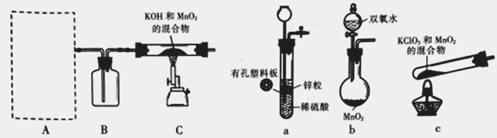
(1)装置A应选用______________(填a、b或c)。
(2)装置B中所盛试剂的名称为_________________。
(3)装置C处反应生成K2MnO4的化学方程式为_____________________。
步骤II.由K2MnO4制备KMnO4。已知: K2MnO4易溶于水,水溶液呈墨绿色。
主要过程如下:
①充分反应后,将装置C处所得固体加水溶解,过滤;
②向滤液中通入足量CO2,过滤出生成的MnO2;
③将滤液蒸发浓缩、降温结晶、过滤、洗涤、干燥,得KMnO4晶体。
(4)过程②向滤液中通入足量CO2,可观察到的现象为____________________;
该步反应中氧化剂与还原剂的物质的量之比为_______________。
(二) KMnO4的性质
巳知: KMnO4具有强氧化性,可与草酸(H2C2O4)反应。
(5)写出KMnO4酸性溶液与草酸反应的离子方程式 _______________________。
(6)基于(5)的反应原理,探究浓度对化学反应速率的影响。
可供选择的试剂有:①0.01 mol·L-1 1 KMnO4酸性溶液;②0.3 mol·L-1 KMnO4酸性溶液;③0.1 mol·L-1 H2C2O4溶液;④0.2 mol·L-1 H2C2O4溶液
所选试剂为______(填序号);简要描述所设计的实验方案______________________________。
2SO3(g),该反应在一定条件下进行时的热效应如图所示,则其逆反应的活化能为__________________。





