-
KMnO4在生产和生活中有着广泛的用途,某化学小组在实验室制备KMnO4并探究其性质。请回答下列问题:
(一)KMnO4的制备。
步骤Ⅰ.先利用如图甲所示装置由MnO2制备K2MnO4 。
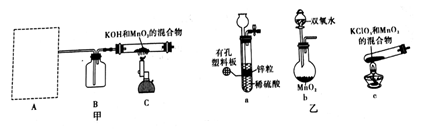
(1)装置A应选用图乙中的______________ (填“a”、“b”或“c”)。
(2)装置B中所盛试剂的名称为_________________。
(3)装置C处制备K2MnO4的化学方程式为________________________。
步骤Ⅱ.由K2MnO4制备KMnO4。已知: K2MnO4易溶于水,水溶液呈墨绿色。
主要过程如下:
①充分反应后,将装置C处所得固体加水溶解,过滤;
②向①的滤液中通入足量CO2,过滤出生成的MnO2;
③将②的滤液经过一系列实验操作从而获得KMnO4晶体。
(4)过程③干燥KMnO4时,温度不宜过高的原因是_______________。
(5)过程②向①的滤液中通入足量CO2,可观察到的现象为______________________; 该步反应中氧化剂与还原剂的物质的量之比为____________。
(二)KMnO4的性质。
(6) KMnO4具有强氧化性,某化学学习小组利用2KMnO4+5H2C2O4+3H2SO4 =K2SO4+2MnSO4+10CO2 +8H2O的反应原理,用配制好的0.10mol/LKMnO4溶液来测定 H2C2O4溶液的浓度,酸性KMnO4溶液应放在_______滴定管中(填“酸式”或“碱式”),滴定时所得的实验数据如下表,试计算所测H2C2O4溶液的浓度为_______mol·L-1。
| 实验次数编号 | 待测液体积(mL) | 滴入的标准液体积(mL) |
| 1 | 25.00 | 28.95 |
| 2 | 25.00 | 25.05 |
| 3 | 25.00 | 24.95 |
-
KMnO4在生产和生活中有着广泛用途,某化学小组在实验室制备KMnO4并探究其性质。请回答:
(一) KMnO4的制备,分步骤I、II两步进行。
步骤I.先利用下图所示装置制备K2MnO4
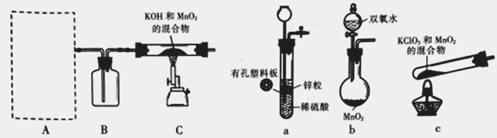
(1)装置A应选用______________(填a、b或c)。
(2)装置B中所盛试剂的名称为_________________。
(3)装置C处反应生成K2MnO4的化学方程式为_____________________。
步骤II.由K2MnO4制备KMnO4。已知: K2MnO4易溶于水,水溶液呈墨绿色。
主要过程如下:
①充分反应后,将装置C处所得固体加水溶解,过滤;
②向滤液中通入足量CO2,过滤出生成的MnO2;
③将滤液蒸发浓缩、降温结晶、过滤、洗涤、干燥,得KMnO4晶体。
(4)过程②向滤液中通入足量CO2,可观察到的现象为____________________;
该步反应中氧化剂与还原剂的物质的量之比为_______________。
(二) KMnO4的性质
巳知: KMnO4具有强氧化性,可与草酸(H2C2O4)反应。
(5)写出KMnO4酸性溶液与草酸反应的离子方程式 _______________________。
(6)基于(5)的反应原理,探究浓度对化学反应速率的影响。
可供选择的试剂有:①0.01 mol·L-1 1 KMnO4酸性溶液;②0.3 mol·L-1 KMnO4酸性溶液;③0.1 mol·L-1 H2C2O4溶液;④0.2 mol·L-1 H2C2O4溶液
所选试剂为______(填序号);简要描述所设计的实验方案______________________________。
-
铁及其化合物在生产和生活中有着广泛的应用。某实验小组设计了如下实验探究
某些含铁化合物的制备、组成、性质等。请按要求回答下列问题:
(1)铁的氯化物的制备与组成:在实验室中,FeCl2可用________和盐酸反应制备,FeCl3可用铁粉和
________反应制备。现有一含有FeCl2和FeCl3的混合物样品,测得n(Fe)∶n(Cl)=1∶2.2,则该样
品中FeCl2和FeC13物质的量之比为__________。
(2)水处理剂和高容量电池材料――高铁酸钾(K2FeO4)的制备与应用:
FeC13与KClO在强碱性条件下反应可制取K2FeO4,其反应的离子方程式为
________________________________________________________________________;
与MnO2-Zn电池类似,K2FeO4-Zn也可以组成碱性电池,其正极电极反应式为
________________________________________________________________________。
(3)光敏材料三草酸合铁酸钾晶体(K3[Fe(C2O4)3]·xH2O)中铁元素含量的测定:
步骤一:称量10.00 g三草酸合铁酸钾晶体,配制成250 mL溶液。
步骤二:取所配溶液25.00 mL于锥形瓶中,加稀H2SO4酸化,滴加KMnO4溶液至草酸根恰好全部氧化成二氧化碳。同时MnO 被还原成Mn2+。向反应后的溶液中加入适量锌粉,至黄色刚好消失,所得溶液收集到锥形瓶中,此时溶液仍呈酸性。
被还原成Mn2+。向反应后的溶液中加入适量锌粉,至黄色刚好消失,所得溶液收集到锥形瓶中,此时溶液仍呈酸性。
步骤三:用0.0200 mol/L KMnO4溶液滴定步骤二所得溶液至终点,消耗KMnO4溶液20.02 mL,滴定中MnO 还原成Mn2+。
还原成Mn2+。
重复步骤二、三操作,步骤三消耗0.0200 mol/L KMnO4溶液19.98 mL。
①步骤一中除量筒、玻璃棒、烧杯外,还需要的玻璃仪器有____________________;步骤三滴定过程中盛装KMn4溶液的仪器名称为___________;滴入最后一滴溶液时,锥形瓶中溶液变为_________色,静置半分钟溶液颜色不再变化,确认为滴定终点。
②步骤二加入锌粉的目的是_______________________________;
写出锌参与反应的离子方程式:____________________________________________。
③实验测得该晶体中铁元素的质量分数为____________。在步骤二中,若加入的KMnO4溶液的量不足,则测得的铁元素含量____________。(填“偏低”“偏高”或“无影响”)
-
肼(N2H4)是一种高能燃料,在生产和研究中用途广泛。化学小组同学在实验室中用过量NH3和NaC1O溶液反应制取N2H4(液)并探究其性质。回答下列问题:
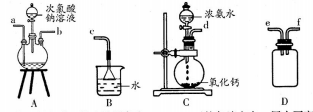
(1)肼的制备
①用上图装置制取肼,其连接顺序为________(按气流方向,用小写字母表示)。
②装置A中发生反应的化学方程式为_________________,装置D的作用是_______________。
(2)探究:N2H4和AgNO3溶液的反应将制得的肼分离提纯后,进行如下实验:
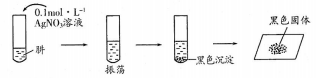
证明黑色沉淀已洗涤干净的操作是__________________________________。
【查阅资料】N2H4水溶液的碱性弱于氨水;N2H4有强还原性。AgOH在溶液中不稳定易分解生成Ag2O;Ag2O和粉末状的Ag均为黑色;Ag2O可溶于氨水。
【提出假设】
假设1:黑色固体可能是Ag;
假设2:黑色固体可能是_____________;
假设3:黑色固体可能是Ag和Ag2O。
【实验验证】该同学基于上述假设,设计如下方案,进行实验,请完成下表中的空白部分。
| 实验编号 | 操作 | 现象 | 实验结论 |
| 1 | 取少量黑色固体于试管,__________ | 黑色固体不溶解 | 假设1成立 |
| 2 | 操作同实验1 | 黑色固体完全溶解 | 假设2成立 |
| 3 | ①取少量黑色固体于试管中,加入适量氨水,振荡,静置,取上层清液于洁净试管中,加入几滴乙醛,水浴加热②取少量黑色固体于试管中,加入足量稀硝酸,振荡 | ①________________ ②________________ | 假设3成立 |
根据实验现象,假设1成立,则N2H4与AgNO3溶液反应的离子方程式为____________。
-
某研究性学习小组欲探究FeSO4·7H2O(绿矾)的主要化学性质和用途。
I.FeSO4·7H2O(绿矾)广泛用于医药和工业领域,以下是FeSO4·7H2O的实验室制备流程图:
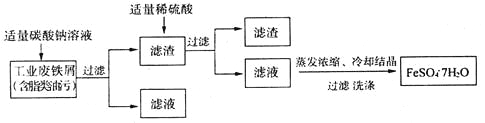
根据题意回答下列问题:
(1)碳酸钠溶液能除去脂类油污是因为_________________(用必要的文字说明);
(2)废铁屑中含有少量的Fe2O3,在制备过程中无需除去,理由是___________________(用必要的离子方程式说明)。
II.为测定某补血剂(有效成分为FeSO4·7H2O)中铁元素含量,设计实验流程如下,回答下列问题:
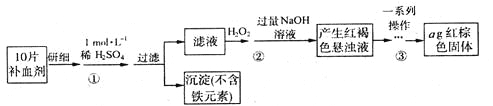
(1)步骤①需要用浓硫酸(质量分数为98.3 %)配制100 mL 1 mol·L-1的稀硫酸,所用的玻璃仪器有量筒、烧杯、玻璃棒、胶头滴管及____________;
(2)步骤③所表示的一系列操作依次是:
a.过滤
b.洗涤
c.__________
d.冷却
e.称量
f.重复c~e直至固体质量不变
操作f的目的是_________________________________________________________;
(3)假设实验过程中铁元素无损耗,则每片补血剂含铁元素为________g(用含n的代数式表示)。
III.利用下图装置探究绿矾的热稳定性
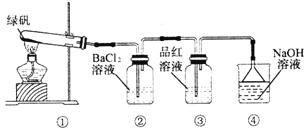
(1)实验过程中,观察到③中品红溶液退色,据此推测FeSO4分解过程中最有可能被氧化的元素是___________,请写出④中反应的离子方程式:____________________;
(2)②中有白色沉淀生成,小组成员经过理论分析并结合(1)中的表述推测,绿矾分解的产物最有可能是下列各项中的______________(填序号字母)。
a.Fe2O3、SO3、H2O
b.Fe2O3、SO2、SO3、H2O
c.FeO、SO2、SO3、H2O
-
SO2在工业生产和食品加工等行业用途广泛。某化学小组对SO2的一些性质和反应进行探究。回答下列问题:
I.为探究SO2和Na2O2的反应产物,进行如下实验。
(1)提出假设。假设一:反应产物为Na2SO3和O2;假设二:反应产物为___(填化学式)。
(2)实验验证。
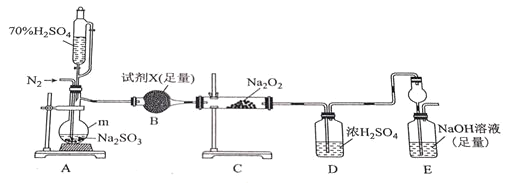
①m的名称为___。
②A中若用稀硫酸代替70%的硫酸,不足之处为___。
③试剂X不宜选择___(填选项字母)。
a.生石灰 b.CaCl2 c.硅胶 d.P2O5
④B的作用___。
II.SO2可以用作葡萄酒的抗氧化剂和防腐剂。该小组同学通过下列操作测定某葡萄酒样品SO2的总含量:量取V1mL样品,加入足量稀H2SO4;将生成的SO2全部蒸出并用足量NaOH溶液吸收;调节溶液的pH后,用cmol/L的标准I 2溶液滴定至终点,消耗标准液的体积为V 2mL。
(3)滴定反应的离子方程式为___;样品中的总含量为___mg/L(用含c,V 1,V 2的代数式表示)。
(4)若用足量稀盐酸代替稀H2SO4,会导致所测SO2的总含量___(填偏高偏低或无影响)。
III.(5)设计实验证明H 2SO3的酸性强于H 2CO3:___。(供选试剂:NaHCO3溶液、CO2、SO2、KMnO4(H+)溶液、NaOH溶液、澄清石灰水)
-
某化学小组为探究草酸的性质并制备草酸钠及其用途,查阅到如下信息:

探究草酸部分性质并制备草酸钠的生产流程如下:
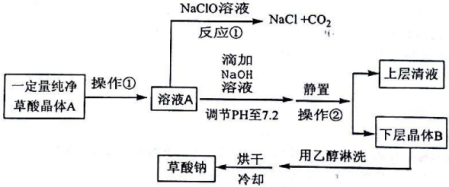
请回答下列问题:
(1)写出反应①的化学方程式__________。表明草酸具有__________性。
(2)向溶液A中加入NaOH溶液,开始滴加速度要尽量快些.其目的是__________。该反应达到终点时的化学方程式为__________。
(3)操作②的名称是__________。用乙醇淋洗晶体B的目的是__________
(4)用0.01000mol/L的高锰酸钾溶液滴定25.00mL某浓度的草酸钠溶液时.需要加入适量的稀硫酸,所发生反应为:5C2O42-+2MnO4-+16H+=2Mn2++10CO2↑+8H2O,若硫酸加入太多,结果会__________:操作中需用__________滴定管(填“酸式”或“碱式”),当达到反应终点时的现象是__________;测得此时消耗上述高锰酸钾溶液20.00mL,则该草酸钠溶液浓度为__________mol/L。
-
氯及其化合物在工农业生产和日常生活中有着广泛的用途。
Ⅰ.实验室用下图所示装置制备KClO溶液,并通过KClO溶液与Fe(NO3)3溶液的反应制备高效水处理剂K2FeO4。已知K2FeO4具有下列性质①可溶于水、微溶于浓KOH溶液,②在0℃~5℃、强碱性溶液中比较稳定。
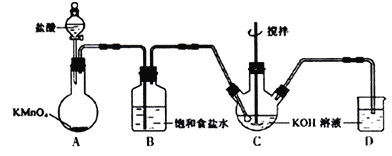
(1)装置A中的玻璃仪器的名称分别是___________。
(2)装置A中KMnO4与盐酸反应生成KCl、MnCl2和Cl2,其离子方程式为_______________________。将制备的Cl2通过装置B可除去___________ (填化学式)。
(3)Cl2和KOH在较高温度下反应生成KClO3。在不改变KOH溶液的浓度和体积的条件下,控制反应在0℃~5℃进行,实验中可采取的措施是___________________。
Ⅱ.某学习小组用下图装置制取并收集ClO2。(已知无水草酸在100℃可以升华)
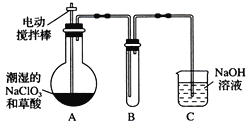
(1)实验时装置A需在60℃~100℃进行的原因是_________________________。
(2) 电动搅拌棒的作用是_______________________。
(3)装置A中反应产物有Na2CO3、ClO2和CO2等,用ClO2处理过的饮用水(pH为5.5~6.5)往往残留少量ClO2和一定量对人体不利的亚氯酸根高子(ClO2-)。
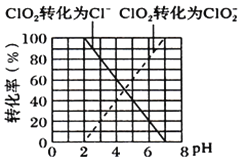
①ClO2被I-还原为ClO2-、Cl-的转化率与溶液pH的关系如图所示
②当pH≤2.0时,写出ClO2被I-还原的离子方程式________________________________。
③当pH 为7.0~8.0时,ClO2的还原产物为___________。
-
(18分)某研究性学习小组欲探究FeSO4·7H2O(绿矾)的主要化学性质和用途。
I.FeSO4·7H2O(绿矾)广泛用于医药和工业领域,以下是FeSO4·7H2O的实验室制备流程图:
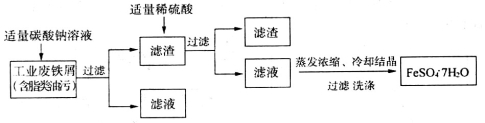
根据题意回答下列问题:
(1)碳酸钠溶液能除去脂类油污是因为_________________(用必要的文字说明);
(2)废铁屑中含有少量的Fe2O3,在制备过程中无需除去,理由是___________________(用必要的离子方程式说明)。
II.为测定某补血剂(有效成分为FeSO4·7H2O)中铁元素含量,设计实验流程如下,回答下列问题:
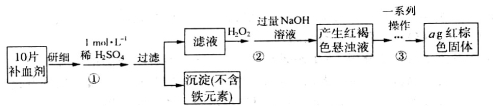
(1)步骤①需要用浓硫酸(质量分数为98.3 %)配制100 mL 1 mol·L-1的稀硫酸,所用的玻璃仪器有量筒、烧杯、玻璃棒、胶头滴管及____________;
(2)步骤③所表示的一系列操作依次是:
a.过滤
b.洗涤
c.__________
d.冷却
e.称量
f.重复c~e直至固体质量不变
操作f的目的是_________________________________________________________;
(3)假设实验过程中铁元素无损耗,则每片补血剂含铁元素为________g(用含n的代数式表示)。
III.利用下图装置探究绿矾的热稳定性
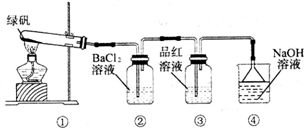
(1)实验过程中,观察到③中品红溶液退色,据此推测FeSO4分解过程中最有可能被氧化的元素是___________,请写出④中反应的离子方程式:____________________;
(2)②中有白色沉淀生成,小组成员经过理论分析并结合(1)中的表述推测,绿矾分解的产物最有可能是下列各项中的______________(填序号字母)。
a.Fe2O3、SO3、H2O
b.Fe2O3、SO2、SO3、H2O
c.FeO、SO2、SO3、H2O
-
【化学—选修3:物质结构与性质】
铁、铝、铜都是日常生活中常见的金属,它们的单质及其化合物在科学研究和工农业生产中具有广泛用途。请回答以下问题:
(1)超细铜粉可用作导电材料、催化剂等,其制备方法如下:

①铜元素位于周期表_________区;Cu+的基态价电子排布图_________;NH4CuSO3中N、S、O三种元素的第一电离能由大到小的顺序为_________(元素符号表示)。
②SO42-中心原子的杂化方式为_________,SO32-的价层电子互斥模型为_________。
(2)请写出向Cu(NH3)4SO4水溶液中通入SO2时发生反应的离子方程式_________。
(3)某学生向CuSO4溶液中加入少量氨水生成蓝色沉淀,继续加入过量氨水沉淀溶解,得到深蓝色透明溶液,最后向该溶液中加入一定量乙醇,析出[Cu(NH3)4]SO4·H2O晶体。
①下列说法正确的是_________。
a.因NH3和H2O都为极性分子,且它们还存在分子内氢键,所以氨气极易溶于水
b.NH3分子和H2O分子,分子空间构型不同,氨气分子的键角小于水分子的键角
c.Cu(NH3)4SO4所含有的化学键有离子键、极性共价键和配位键
d.Cu(NH3)4SO4组成元素中电负性最大的是氮元素
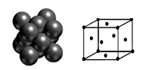
②请解释加入乙醇后析出晶体的原因_________。
(4)下图所示为金属铜的一个晶胞,此晶胞立方体的边长为a pm,Cu的相对原子质量为64,金属铜的密度为ρ g/cm3,则晶胞中铜原子的配位数为_________,用含有a、ρ的代数式表示的阿伏加德罗常数为:_________ mol-1。