-
氯及其化合物在工农业生产和日常生活中有着广泛的用途。
Ⅰ.实验室用下图所示装置制备KClO溶液,并通过KClO溶液与Fe(NO3)3溶液的反应制备高效水处理剂K2FeO4。已知K2FeO4具有下列性质①可溶于水、微溶于浓KOH溶液,②在0℃~5℃、强碱性溶液中比较稳定。
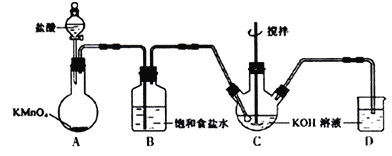
(1)装置A中的玻璃仪器的名称分别是___________。
(2)装置A中KMnO4与盐酸反应生成KCl、MnCl2和Cl2,其离子方程式为_______________________。将制备的Cl2通过装置B可除去___________ (填化学式)。
(3)Cl2和KOH在较高温度下反应生成KClO3。在不改变KOH溶液的浓度和体积的条件下,控制反应在0℃~5℃进行,实验中可采取的措施是___________________。
Ⅱ.某学习小组用下图装置制取并收集ClO2。(已知无水草酸在100℃可以升华)
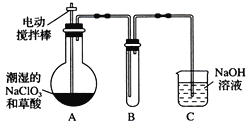
(1)实验时装置A需在60℃~100℃进行的原因是_________________________。
(2) 电动搅拌棒的作用是_______________________。
(3)装置A中反应产物有Na2CO3、ClO2和CO2等,用ClO2处理过的饮用水(pH为5.5~6.5)往往残留少量ClO2和一定量对人体不利的亚氯酸根高子(ClO2-)。
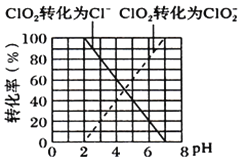
①ClO2被I-还原为ClO2-、Cl-的转化率与溶液pH的关系如图所示
②当pH≤2.0时,写出ClO2被I-还原的离子方程式________________________________。
③当pH 为7.0~8.0时,ClO2的还原产物为___________。
-
溴、碘及其化合物在工农业生产和日常生活中有重要用途。
Ⅰ.氢溴酸在医药和石化工业上有广泛用途,下图是模拟工业制备氢溴酸的流程:
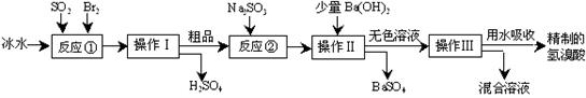
根据上述流程回答下列问题:
(1)反应①中发生反应的离子方程式为 ;使用冰水的目的是
(2)操作Ⅰ的名称是 ;操作Ⅱ的名称是 ;
(3)反应②中加入Na2SO3的目的是 ;但要防止过量,原因是 (用离子方程式表示)
Ⅱ.卤素互化物是指不同卤素原子之间以共价键结合形成的化合物。XX′型卤素互化物与卤素单质结构相似、性质相近, 能与大多数金属反应生成金属卤化物,能与许多非金属单质反应生成相应卤化物,能与水反应等。试回答下列问题:
(4)溴化碘(IBr)与水反应的方程式为IBr +H2O=HBr+HIO下列关于IBr的叙述中不正确的是
A.IBr中溴和碘的化合价均为0价 B.在许多反应中IBr是强氧化剂
C.在IBr与水的反应中,它既是氧化剂又是还原剂 D.与NaOH溶液反应生成NaIO、NaBr和H2O
(5) 在粗碘中含有IBr和ICl,受热时,I2、ICl、IBr均可升华。在粗碘中加入一种物质后,再进行升华,可制得精碘,应加入的物质是
A.H2O B.KI C.Zn D.KCl
-
氢、碳、氮、氧、铁、铜等元素及其化合物在人们的日常生活中有着广泛的用途。回答下列问题:
(1)写出基态铜原子的价电子排布式___。
(2)实验室用KSCN溶液、检验Fe3+。C、N、O的电负性由大到小的顺序为___(用元素符号表示),一定条件下,SCN-与MnO2反应可得到(SCN)2,试写出(SCN)2的结构式___。
(3)FeCl3的熔点为306℃,沸点为315℃FeCl3的晶体类型是__。FeSO4常作补铁剂,SO42-的立体构型是__。
(4)CH3OH分子中O原子的杂化方式为___,键角:H-C-H___H-O-C。(填“<”、“>”、“=”)CH3OH能与H2O以任意比互溶的原因是___。
(5)已知C60分子结构和C60晶胞示意图(如图I、图Ⅱ所示):
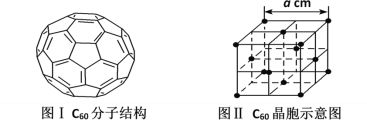
则一个C60分子中含有σ键的个数为__,与每个C60分子距离最近且相等的C60分子有__个,C60晶体的密度的表达式为__g·cm-3。
-
KMnO4在生产和生活中有着广泛用途,某化学小组在实验室制备KMnO4并探究其性质。请回答:
(一) KMnO4的制备,分步骤I、II两步进行。
步骤I.先利用下图所示装置制备K2MnO4
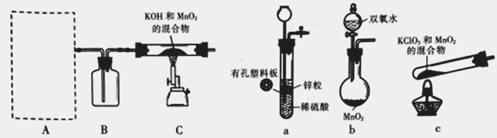
(1)装置A应选用______________(填a、b或c)。
(2)装置B中所盛试剂的名称为_________________。
(3)装置C处反应生成K2MnO4的化学方程式为_____________________。
步骤II.由K2MnO4制备KMnO4。已知: K2MnO4易溶于水,水溶液呈墨绿色。
主要过程如下:
①充分反应后,将装置C处所得固体加水溶解,过滤;
②向滤液中通入足量CO2,过滤出生成的MnO2;
③将滤液蒸发浓缩、降温结晶、过滤、洗涤、干燥,得KMnO4晶体。
(4)过程②向滤液中通入足量CO2,可观察到的现象为____________________;
该步反应中氧化剂与还原剂的物质的量之比为_______________。
(二) KMnO4的性质
巳知: KMnO4具有强氧化性,可与草酸(H2C2O4)反应。
(5)写出KMnO4酸性溶液与草酸反应的离子方程式 _______________________。
(6)基于(5)的反应原理,探究浓度对化学反应速率的影响。
可供选择的试剂有:①0.01 mol·L-1 1 KMnO4酸性溶液;②0.3 mol·L-1 KMnO4酸性溶液;③0.1 mol·L-1 H2C2O4溶液;④0.2 mol·L-1 H2C2O4溶液
所选试剂为______(填序号);简要描述所设计的实验方案______________________________。
-
铁及其化合物在日常生产生活中用途广泛。利用FeSO4制备还原铁粉的工业流程如下:
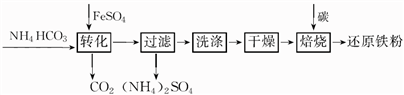
实验室中可用FeSO4(用铁粉和稀硫酸反应制得)和NH4HCO3在如下装置模拟上述流程中的“转化”环节。

(1)装置A的名称是________,装置B中盛放的试剂是________,NH4HCO3盛放在装置________中。
(2)实验过程中,欲将生成的FeSO4溶液和NH4HCO3溶液混合制FeCO3沉淀,操作方法是________________,发生主要反应的离子方程式为_____________________。FeSO4溶液要现用现配制的原因是____________,检验久置的FeSO4是否变质的方法是______________。
(3)干燥过程主要目的是脱去游离水,过程中会有少量FeCO3在空气中被氧化为FeOOH,该反应的化学方程式为____________________________,取干燥后的FeCO3样品12.49 g,与碳混合后焙烧,最终得到还原铁粉6.16 g,计算样品中杂质FeOOH的质量:________g。
-
铝是当前应用最广泛的金属材料之一,铝制品及其化合物在日常生活和工农业生产中也有着重要的用途。回答下列问题:
(1)基态铝原子的核外电子排布式为____________。
(2)根据元素周期律等知识判断,第一电离能Al____________Mg(填写“大于”或“小于”)。
(3)Al2O3是常用的耐火材料,工业上也是用电解Al2O3方法制取金属Al,据此判断Al2O3的晶体类型是____________。
(4)LiAlH4是一种重要的有机合成试剂,AlH4-的立体构型为____________,LiAlH4中Al原子的杂化轨道类型为____________。
(5)金属铝的晶胞结构如图1所示,原子之间相对位置关系的平面图如图2所示。
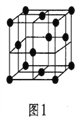
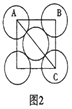
①晶体铝中原子的堆积方式为____________。
②已知铝原子半径为a cm,摩尔质量为Mg·mol-1,阿伏加德罗常数的值为NA,则晶体铝的密度ρ=_______g·cm-3(用含 a、M、NA的代数式来表示)。
-
铜及其化合物在工农业生产和日常生活中有着广泛的用途。请回答下列问题:
(1)基态铜原子的核外电子排布式为___。
(2)NF3可由NH3和F2在Cu催化剂存在下反应直接得到:4NH3+3F2 NF3+3NH4F
NF3+3NH4F
①上述化学方程式中的5种物质所属的晶体类型有__ 填序号
填序号 。
。
a.离子晶体 b.分子晶体 c.原子晶体 d.金属晶体
②F、N、O三种元素的第一电离能由大到小的顺序为__ 用元素符号表示
用元素符号表示
(3)铜晶体铜原子的堆积方式为面心立方最密堆积。每个铜原子周围距离最近的铜原子数目为___。
(4)某X原子的外围电子排布式为3s23p5,铜与X形成化合物的晶胞如图所示(黑点代表铜原子)。
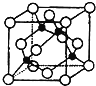
 该晶体的化学式为___。
该晶体的化学式为___。
②已知该晶体的密度为ρg·cm-3,阿伏加德罗常数的数值为NA,则该晶体中晶胞的棱长为__pm(只写计算式 。
。
(5)合成氨工艺的一个重要工序是铜洗,其目的是用铜液 醋酸二氨合铜(I)、氨水
醋酸二氨合铜(I)、氨水 吸收在生产过程中产生的CO和CO2等气体。铜液吸收CO的反应是放热反应,其反应方程式为:Cu(NH3)2Ac+CO+NH3⇌[Cu(NH3)3CO]Ac(Ac表示醋酸根
吸收在生产过程中产生的CO和CO2等气体。铜液吸收CO的反应是放热反应,其反应方程式为:Cu(NH3)2Ac+CO+NH3⇌[Cu(NH3)3CO]Ac(Ac表示醋酸根
①如果要提高上述反应的反应速率,可以采取的措施是___。(选填编号)
a.减压 b.增加NH3的浓度 c.升温 d.及时移走产物
②铜液的组成元素中,短周期元素原子半径从大到小的排列顺序为___。
③NH3的氮原子的杂化类型为___。
-
铜及其化合物在工农业生产和日常生活中有着广泛的用途。请回答下列问题:
(1)基态铜原子的核外电子排布式为___。
(2)NF3可由NH3和F2在Cu催化剂存在下反应直接得到:4NH3+3F2 NF3+3NH4F
NF3+3NH4F
①上述化学方程式中的5种物质所属的晶体类型有__ 填序号
填序号 。
。
a.离子晶体 b.分子晶体 c.原子晶体 d.金属晶体
②F、N、O三种元素的第一电离能由大到小的顺序为__ 用元素符号表示
用元素符号表示
(3)铜晶体铜原子的堆积方式为面心立方最密堆积。每个铜原子周围距离最近的铜原子数目为___。
(4)某X原子的外围电子排布式为3s23p5,铜与X形成化合物的晶胞如图所示(黑点代表铜原子)。

 该晶体的化学式为___。
该晶体的化学式为___。
②已知该晶体的密度为ρg·cm-3,阿伏加德罗常数的数值为NA,则该晶体中晶胞的棱长为__pm(只写计算式 。
。
(5)合成氨工艺的一个重要工序是铜洗,其目的是用铜液 醋酸二氨合铜(I)、氨水
醋酸二氨合铜(I)、氨水 吸收在生产过程中产生的CO和CO2等气体。铜液吸收CO的反应是放热反应,其反应方程式为:Cu(NH3)2Ac+CO+NH3⇌[Cu(NH3)3CO]Ac(Ac表示醋酸根
吸收在生产过程中产生的CO和CO2等气体。铜液吸收CO的反应是放热反应,其反应方程式为:Cu(NH3)2Ac+CO+NH3⇌[Cu(NH3)3CO]Ac(Ac表示醋酸根
①如果要提高上述反应的反应速率,可以采取的措施是___。(选填编号)
a.减压 b.增加NH3的浓度 c.升温 d.及时移走产物
②铜液的组成元素中,短周期元素原子半径从大到小的排列顺序为___。
③NH3的氮原子的杂化类型为___。
-
KMnO4在生产和生活中有着广泛的用途,某化学小组在实验室制备KMnO4并探究其性质。请回答下列问题:
(一)KMnO4的制备。
步骤Ⅰ.先利用如图甲所示装置由MnO2制备K2MnO4 。
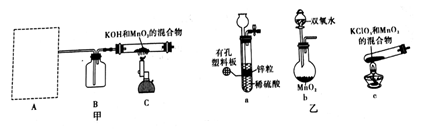
(1)装置A应选用图乙中的______________ (填“a”、“b”或“c”)。
(2)装置B中所盛试剂的名称为_________________。
(3)装置C处制备K2MnO4的化学方程式为________________________。
步骤Ⅱ.由K2MnO4制备KMnO4。已知: K2MnO4易溶于水,水溶液呈墨绿色。
主要过程如下:
①充分反应后,将装置C处所得固体加水溶解,过滤;
②向①的滤液中通入足量CO2,过滤出生成的MnO2;
③将②的滤液经过一系列实验操作从而获得KMnO4晶体。
(4)过程③干燥KMnO4时,温度不宜过高的原因是_______________。
(5)过程②向①的滤液中通入足量CO2,可观察到的现象为______________________; 该步反应中氧化剂与还原剂的物质的量之比为____________。
(二)KMnO4的性质。
(6) KMnO4具有强氧化性,某化学学习小组利用2KMnO4+5H2C2O4+3H2SO4 =K2SO4+2MnSO4+10CO2 +8H2O的反应原理,用配制好的0.10mol/LKMnO4溶液来测定 H2C2O4溶液的浓度,酸性KMnO4溶液应放在_______滴定管中(填“酸式”或“碱式”),滴定时所得的实验数据如下表,试计算所测H2C2O4溶液的浓度为_______mol·L-1。
| 实验次数编号 | 待测液体积(mL) | 滴入的标准液体积(mL) |
| 1 | 25.00 | 28.95 |
| 2 | 25.00 | 25.05 |
| 3 | 25.00 | 24.95 |
-
铁、铜等金属及其化合物在日常生产生活中用途非常广泛。
I.实验室欲制备0.3molCu(NO3)2晶体,甲、乙两同学分别设计实验方案如下:
甲:Cu Cu(NO3)2 乙:Cu
Cu(NO3)2 乙:Cu CuO
CuO Cu(NO3)2
Cu(NO3)2
(1)从绿色化学的角度分析, 同学的方案更合理。
(2)乙同学实验时通入O2的速率不宜过大,为便于观察和控制产生O2的速率,宜选择 装置(填字母序号)。

Ⅱ.某化学实验小组通过实验来探究一包黑色粉是否由Fe3O4、CuO组成,探究过程如下:
(1)提出假设:
假设1.黑色粉末是CuO;
假设2.黑色粉末是Fe3O4;
假设3.黑色粉末是CuO和Fe3O4的混合物。
(2)设计探究实验:
取少量粉末放入足量稀硫酸中,在所得溶液中滴加KSCN试剂。
①若假设1成立,则实验现象是溶液显蓝色。
②若假设2或3成立,则实验现象是 。
为进一步探究,继续向所得溶液加入足量铁粉,若产生 的现象,则假设3成立。
有另一小组同学提出,若混合物中CuO含量较少,可能加入铁粉后实验现象不明显。
查阅资料:Cu2+与足量氨水反应生成深蓝色溶液,Cu2++4NH3•H2O=Cu(NH3)42++4H2O。
为探究是假设2还是假设3成立,另取少量粉末加稀硫酸充分溶解后,再加入足量氨水,若假设2成立,则产生 现象;若假设3成立,则产生 现象。
Ⅲ.由Fe3O4、FeO、CuO、Fe组成的固体混合物,在加热条件下用足量的CO还原,得到金属混合物2.86g,将生成的CO2气体用足量的澄清石灰水吸收后,产生5.00g白色沉淀。固体混合物的质量是 。













