-
I.尿素[CO(NH2)2]是人工合成的第一种有机物。
(1)尿素中所含元素的电负性最大的是________,尿素分子间的氢键可表示为_____。
(2)尿素可用于制有机铁肥,主要代表有[Fe(H2NCONH2)6](NO3)3 。
①与铁同周期且未成对电子数与Fe3+相同的元素是________。
②[Fe(H2NCONH2)6](NO3)3中不存在的化学键____________(填序号)。
A 离子键 B 金属键 C 配位键 D σ键 E π键
③NO3-中N原子杂化后的价电子排布图为_______,NO3-的空间构型为________。
II.Mg2NiH4是一种贮氢的金属氢化物
(3)Mg2NiH4可通过氢化镁和镍单质球磨制成。在Mg2NiH4晶胞中,Ni原子占据如图的顶点和面心,Mg2+处于图八个小立方体的体心。
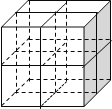
①Mg2NiH4中H的化合价为______。
②Mg2+位于Ni原子形成的___________(填“八面体空隙”或“四面体空隙”)。
③若晶体的密度为dg·cm-3,Mg2NiH4的摩尔质量为Mg·mol-1,则Mg2+和Ni原子的最短距离为___________nm(用含d、M的代数式表示)。
-
N是重要的非金属元素,尿素、羟胺、硝酸、亚硝酸钠均为重要的含氮化合物。
(1)尿素[CO(NH2)2]是人类利用无机物合成的第一种有机物。尿素中元素原子半径最大的原子结构示意图为 ;
(2)羟胺(NH2OH)可看做是氨分子内的1个氢原子被羟基取代的物质,常用作还原剂。
①利用羟胺的还原性,可以除去含Fe2+中的Fe3+,氧化产物是一种性质稳定、无污染的气体,写出反应的离子方程式
②制备NH2OH·HCl(盐酸羟胺)的一种工艺流程如下图所示:
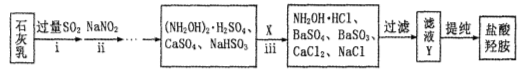
ⅰ步骤中,发生反应的化学方程式为 ;
ⅱ步骤中使用的NaNO2外观酷似食盐,误食会中毒。可用电解法将工业废水中少量的NO2ˉ转化为N2以降低其危害。写出NO2ˉ在酸性条件下转化为氮气的电极反应式为 。
-
尿素[CO(NH2)2]是首个由无机物人工合成的有机物.
(1)工业上尿素由CO2和NH3在一定条件下合成,其反应方程式为______
-
(14分)(2012•重庆)尿素[CO(NH2)2]是首个由无机物人工合成的有机物.
(1)工业上尿素由CO2和NH3在一定条件下合成,其反应方程式为 .
(2)当氨碳比 =4时,CO2的转化率随时间的变化关系如图1所示.
=4时,CO2的转化率随时间的变化关系如图1所示.
①A点的逆反应速率v逆(CO2) B点的正反应速率v正(CO2)(填“大于”“小于”或“等于”).
②NH3的平衡转化率为 .
(3)人工肾脏可采用间接电化学方法除去代谢产物中的尿素,原理如图2所示.
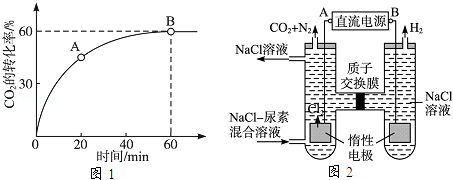
①电源的负极为 (填“A”或“B”).
②阳极室中发生的反应依次为 、 .
③电解结束后,阴极室溶液的pH与电解前相比将 ;若两极共收集到气体13.44L(标准状况),则除去的尿素为 g(忽略气体的溶解).
-
尿素[CO(NH2)2]是首个由无机物人工合成的有机物.
(1)工业上尿素由CO2和NH3在一定条件下合成,其反应方程式为________.
(2)当氨碳比 =4时,CO2的转化率随时间的变化关系如图1所示.
=4时,CO2的转化率随时间的变化关系如图1所示.
①A点的逆反应速率v逆(CO2)________B点的正反应速率v正(CO2)(填“大于”“小于”或“等于”).
②NH3的平衡转化率为________.
(3)人工肾脏可采用间接电化学方法除去代谢产物中的尿素,原理如图2所示.

①电源的负极为________(填“A”或“B”).
②阳极室中发生的反应依次为________、________.
③电解结束后,阴极室溶液的pH与电解前相比将________;若两极共收集到气体13.44L(标准状况),则除去的尿素为________ g(忽略气体的溶解).
-
(16分)尿素[CO(NH2)2]是首个由无机物人工合成的有机物。
⑴工业上尿素由CO2和NH3在一定条件下合成,其反应方程式为________。
⑵当氨碳比 =4时,CO2的转化率随时间的变化关系如右图所示。
=4时,CO2的转化率随时间的变化关系如右图所示。
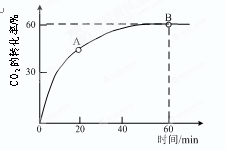
①A点的逆反应速率v逆(CO2)B点的正反应速率v正(CO2)(填 “大于”、“小于”或“等于”)
②NH3的平衡转化率为。
人工肾脏可采用间接电化学方法除去代谢产物中的尿素,原理如右图。
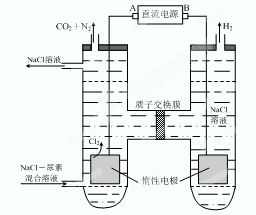
①电源的负极为(填“A”或“B”)。
②阳极室中发生的反应依次为、。
③电解结束后,阴极室溶液的pH与电解前相比将;若两极共收集到气体13.44 L(标准状况),则除去的尿素为g(忽略气体的溶解)。
-
尿素[CO(NH2)2]是首个由无机物人工合成的有机物,工业上尿素是用CO2和NH3在一定条件下合成,其反应方程式为2NH3+CO2 CO(NH3)2+H2O,当氨碳比
CO(NH3)2+H2O,当氨碳比 ,CO2的转化率随时间的变化关系如右图所示,下列说法错误的是
,CO2的转化率随时间的变化关系如右图所示,下列说法错误的是
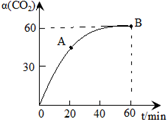
A.该反应在60min时达到平衡状态
B.NH3的平衡转化率为30%
C.增加氨碳比可进一步提高CO2的平衡转化率
D.A点的逆反应速率v逆(CO2)大于B点的正反应速率V正(CO2)
-
尿素是首个由无机物人工合成的有机物,工业上尿素是用CO2和NH3在一定条件下合成,其反应方程式为2NH3+CO2 CO(NH2)2+H2O,当氨碳比
CO(NH2)2+H2O,当氨碳比 ,CO2的转化率随时间的变化关系如右图所示,下列说法错误的是( )
,CO2的转化率随时间的变化关系如右图所示,下列说法错误的是( )

A.该反应在60min时达到平衡状态
B.NH3的平衡转化率为30%
C.增加氨碳比可进一步提高CO2的平衡转化率
D.A点的逆反应速率υ逆(CO2)大于B点的正反应速率υ正(CO2)
-
1828年,德国化学家弗里德里希·维勒首次使用(NH4)2SO4与氰酸钾KCNO人工合成了尿素CO(NH2)2,打破了有机化合物的"生命力"学说。
(1) (NH4)2SO4与KCNO合成尿素反应的化学方程式为____________。
(2)某小组同学在实验室条件下,拟用CO2和NH3,在催化剂的作用下合成尿素。
①用CO2和NH3合成尿素 CO(NH2)2反应的化学方程式为____________。
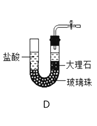
②实验所需的CO2可用多种装置来制备,要想达到“随开随用、随关随停”的目的,下列装置A、B、C、D、E中符和要求的有____________(填字母)。
③若用F装置收集氨气,则气体应由导管口____________(填“a”或“b”)进入。



(3)尿素样品中氮含量可以用甲醛法标定,其原理如下:首先用浓硫酸分解试样,使试液中的胺生成硫酸铵并放出二氧化碳;将过量的硫酸中和后得到中性铵盐,再用甲醛(HCHO)与硫酸铵作用生成六次甲基四铵盐离子(CH2)6N4 H+和硫酸;最后用标准氢氧化钠溶液滴定。
①甲醛与硫酸铵反应的离子方程式为____________;
②滴定选用的指示剂为____________。滴定终点的现象为____________。
③若称取样品m g,溶解后配成250mL溶液。取25.00mL样品溶液于250 mL锥形瓶中,加入10mL w%的甲醛溶液,充分反应后,加入1~2滴指示剂,用浓度为a mol/L的NaOH标准溶液滴定至终点(已知滴定时,1 mol六次甲基四铵盐离子(CH2)6N4H+消耗OH﹣的能力与1mol H+相当)。重复2次,消耗NaOH标准溶液的体积平均值为b mL。则该样品中氮的质量分数为____________。
-
(14分)1773年,伊莱尔·罗埃尔(Hilaire Rouelle)发现尿素。1828年,弗里德里希·维勒首次使用无机物质氰酸钾[KCNO]与硫酸铵人工合成了尿素[CO(NH2)2]。
(1)维勒合成尿素的化学反应方程式为________。
(2)工业上尿素是由CO2和NH3在一定条件下合成,其反应方程式为________当氨碳比 的转化率随时间的变化关系如图1所示。
的转化率随时间的变化关系如图1所示。
①A点速率v逆(CO2)________ 点速率为V正(CO2)(填“大于”、“小于”或“等于”)
点速率为V正(CO2)(填“大于”、“小于”或“等于”)
②NH3的平衡转化率为。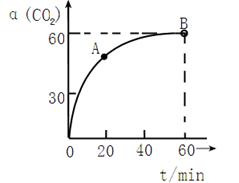
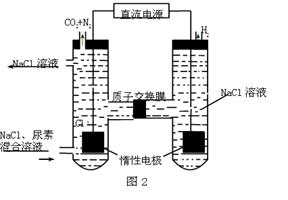
(3)人工肾脏可用间接电化学方法除去代谢产物中的尿素,原理如图2。
①电源的负极为________(填“A”或“B”)。
②阴极室中发生的电极反应式为________
③电解结束后,阴极室溶液的pH与电解前相比将________(填“增大”、“减小”、“不变”)若两极共收集到气体11.2L(标准状况),则除去的尿素为________ g(忽略气体的溶解)。






 CO(NH3)2+H2O,当氨碳比
CO(NH3)2+H2O,当氨碳比






