-
(14分)(2012•重庆)尿素[CO(NH2)2]是首个由无机物人工合成的有机物.
(1)工业上尿素由CO2和NH3在一定条件下合成,其反应方程式为 .
(2)当氨碳比 =4时,CO2的转化率随时间的变化关系如图1所示.
=4时,CO2的转化率随时间的变化关系如图1所示.
①A点的逆反应速率v逆(CO2) B点的正反应速率v正(CO2)(填“大于”“小于”或“等于”).
②NH3的平衡转化率为 .
(3)人工肾脏可采用间接电化学方法除去代谢产物中的尿素,原理如图2所示.
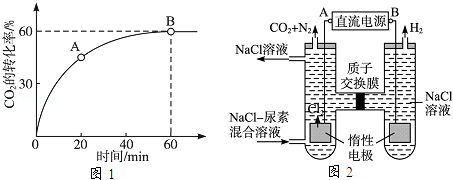
①电源的负极为 (填“A”或“B”).
②阳极室中发生的反应依次为 、 .
③电解结束后,阴极室溶液的pH与电解前相比将 ;若两极共收集到气体13.44L(标准状况),则除去的尿素为 g(忽略气体的溶解).
-
尿素[CO(NH2)2]是首个由无机物人工合成的有机物.
(1)工业上尿素由CO2和NH3在一定条件下合成,其反应方程式为______
-
尿素[CO(NH2)2]是首个由无机物人工合成的有机物,工业上尿素是用CO2和NH3在一定条件下合成,其反应方程式为2NH3+CO2 CO(NH3)2+H2O,当氨碳比
CO(NH3)2+H2O,当氨碳比 ,CO2的转化率随时间的变化关系如右图所示,下列说法错误的是
,CO2的转化率随时间的变化关系如右图所示,下列说法错误的是
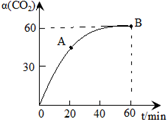
A.该反应在60min时达到平衡状态
B.NH3的平衡转化率为30%
C.增加氨碳比可进一步提高CO2的平衡转化率
D.A点的逆反应速率v逆(CO2)大于B点的正反应速率V正(CO2)
-
尿素[CO(NH2)2]是首个由无机物人工合成的有机物.
(1)工业上尿素由CO2和NH3在一定条件下合成,其反应方程式为________.
(2)当氨碳比 =4时,CO2的转化率随时间的变化关系如图1所示.
=4时,CO2的转化率随时间的变化关系如图1所示.
①A点的逆反应速率v逆(CO2)________B点的正反应速率v正(CO2)(填“大于”“小于”或“等于”).
②NH3的平衡转化率为________.
(3)人工肾脏可采用间接电化学方法除去代谢产物中的尿素,原理如图2所示.

①电源的负极为________(填“A”或“B”).
②阳极室中发生的反应依次为________、________.
③电解结束后,阴极室溶液的pH与电解前相比将________;若两极共收集到气体13.44L(标准状况),则除去的尿素为________ g(忽略气体的溶解).
-
(16分)尿素[CO(NH2)2]是首个由无机物人工合成的有机物。
⑴工业上尿素由CO2和NH3在一定条件下合成,其反应方程式为________。
⑵当氨碳比 =4时,CO2的转化率随时间的变化关系如右图所示。
=4时,CO2的转化率随时间的变化关系如右图所示。
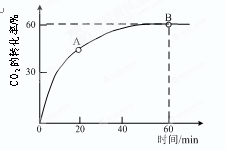
①A点的逆反应速率v逆(CO2)B点的正反应速率v正(CO2)(填 “大于”、“小于”或“等于”)
②NH3的平衡转化率为。
人工肾脏可采用间接电化学方法除去代谢产物中的尿素,原理如右图。
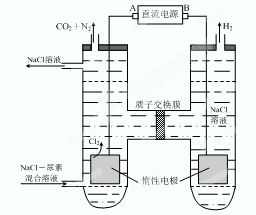
①电源的负极为(填“A”或“B”)。
②阳极室中发生的反应依次为、。
③电解结束后,阴极室溶液的pH与电解前相比将;若两极共收集到气体13.44 L(标准状况),则除去的尿素为g(忽略气体的溶解)。
-
尿素是首个由无机物人工合成的有机物,工业上尿素是用CO2和NH3在一定条件下合成,其反应方程式为2NH3+CO2 CO(NH2)2+H2O,当氨碳比
CO(NH2)2+H2O,当氨碳比 ,CO2的转化率随时间的变化关系如右图所示,下列说法错误的是( )
,CO2的转化率随时间的变化关系如右图所示,下列说法错误的是( )

A.该反应在60min时达到平衡状态
B.NH3的平衡转化率为30%
C.增加氨碳比可进一步提高CO2的平衡转化率
D.A点的逆反应速率υ逆(CO2)大于B点的正反应速率υ正(CO2)
-
尿素[CO(NH2)2] 是首个由无机物合成的有机化合物,通常用作植物的氮肥。合成尿素的主要反应如下:
i. 2NH3(l) + CO2(g) 
 (l)(氨基甲酸铵) △H=-a kJ/mol
(l)(氨基甲酸铵) △H=-a kJ/mol
ii.  (l)
(l) 
 (l) + H2O(l) △H=+b kJ/mol
(l) + H2O(l) △H=+b kJ/mol
iii. 2

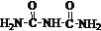 (缩二脲)+NH3 (副反应,程度较小)
(缩二脲)+NH3 (副反应,程度较小)
(1)实验室制取氨气的化学方程式是__________________。
(2)CO(NH2)2中C为+4价,N的化合价_______。
(3)CO2和NH3合成尿素的热化学方程式为___________________________。
(4)工业上提高氨碳比( ),可以提高尿素的产率,结合反应i~iii,解释尿素产率提高的原因______。
),可以提高尿素的产率,结合反应i~iii,解释尿素产率提高的原因______。
(5)某科研小组模拟工业合成尿素,一定条件下,在0.5L的密闭容器中投入4molNH3和1molCO2,测得反应中各组分的物质的量随时间变化如图1所示:
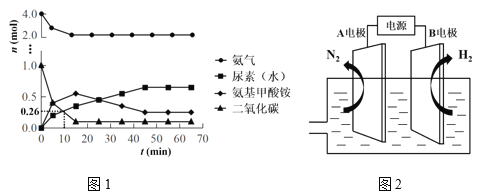
①反应进行到10min时,用CO2表示反应i的速率υ(CO2)=________。
②合成总反应的快慢由慢的一步决定,则合成尿素的总反应的快慢由第______步反应决定(填“i”或“ii”)。
(6)我国研制出非贵金属镍钼基高效电催化剂,实现电解富尿素废水低能耗制H2(装置如图2)。总反应为:CO(NH2)2+H2O 3H2↑+N2↑+CO2↑。
3H2↑+N2↑+CO2↑。
①A电极连接电源的_______极(填“正”或“负”)。
②A电极的电极反应为______。
-
尿素[CO(NH2)2] 是首个由无机物合成的有机化合物,通常用作植物的氮肥。合成尿素的主要反应如下:
i. 2NH3(l) + CO2(g) 
 (l)(氨基甲酸铵) △H=-a kJ/mol
(l)(氨基甲酸铵) △H=-a kJ/mol
ii.  (l)
(l) 
 (l) + H2O(l) △H=+b kJ/mol
(l) + H2O(l) △H=+b kJ/mol
iii. 2

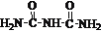 (缩二脲)+NH3 (副反应,程度较小)
(缩二脲)+NH3 (副反应,程度较小)
(1)实验室制取氨气的化学方程式是__________________。
(2)CO(NH2)2中C为+4价,N的化合价_______。
(3)CO2和NH3合成尿素的热化学方程式为___________________________。
(4)工业上提高氨碳比( ),可以提高尿素的产率,结合反应i~iii,解释尿素产率提高的原因______。
),可以提高尿素的产率,结合反应i~iii,解释尿素产率提高的原因______。
(5)某科研小组模拟工业合成尿素,一定条件下,在0.5L的密闭容器中投入4molNH3和1molCO2,测得反应中各组分的物质的量随时间变化如图1所示:
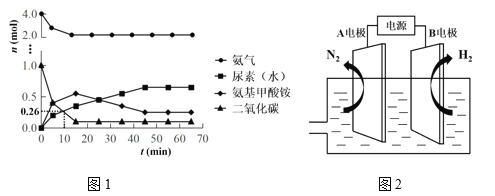
①反应进行到10min时,用CO2表示反应i的速率υ(CO2)=________。
②合成总反应的快慢由慢的一步决定,则合成尿素的总反应的快慢由第______步反应决定(填“i”或“ii”)。
(6)我国研制出非贵金属镍钼基高效电催化剂,实现电解富尿素废水低能耗制H2(装置如图2)。总反应为:CO(NH2)2+H2O 3H2↑+N2↑+CO2↑。
3H2↑+N2↑+CO2↑。
①A电极连接电源的_______极(填“正”或“负”)。
②A电极的电极反应为______。
-
工业生产尿素的原理是以NH3和CO2为原料合成尿素[CO(NH2) 2],反应的化学方程式为 2NH3(g)+ CO2 (g) ⇌ CO(NH2) 2(l)+ H2O(l)+Q(Q>0)。该反应分两步进行:① 2NH3(g)+ CO2 (g) ⇌ NH4COONH2 (s)+ Q1(Q1>0),② NH4COONH2 (s) ⇌ CO(NH2) 2(l)+ H2O(l)+Q2 (Q2<0).
(1)固体CO2称干冰,属于___________晶体。氮原子最外层电子排布式是___________。
(2)氧元素的非金属性比碳强,用原子结构的知识说明理由_________________
(3)下列示意图中,能正确表示合成尿素过程中能量变化的是____________。
A、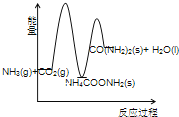 B、
B、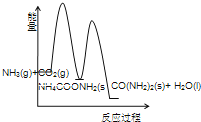
C、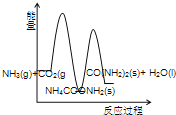 D、
D、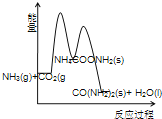
(4)写出合成尿素第一步反应的平衡常数表达式K=_________________________________。
(5)某实验小组模拟工业上合成尿素的条件,在恒定温度下,将氨气和二氧化碳按2:1的物质的量之比充入一体积为10L的密闭容器中(假设容器体积不变,生成物的体积忽略不计),经20min达到平衡,各物质浓度的变化曲线如图所示。
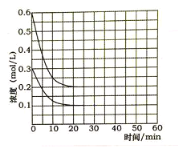
① 在上述条件下,从反应开始至20min时,二氧化碳的平均反应速率为___________。
② 为提高合成尿素的产率,下列可以采取的措施有____________。
a. 缩小反应容器的容积 b. 升高温度
c. 增加反应物的量 d. 使用合适的催化剂
③ 若保持平衡的温度和体积不变,25min 时再向容器中充入2mol氨气和1mol二氧化碳,在40min时重新达到平衡,请在下图中画出25~50min内氨气的浓度变化曲线____________。
-
工业生产尿素的原理是以NH3和CO2为原料合成尿素[CO(NH2) 2],反应的化学方程式为 2NH3(g)+ CO2 (g) ⇌ CO(NH2) 2(l)+ H2O(l)+Q(Q>0)。该反应分两步进行:① 2NH3(g)+ CO2 (g) ⇌ NH4COONH2 (s)+ Q1(Q1>0),② NH4COONH2 (s) ⇌ CO(NH2) 2(l)+ H2O(l)+Q2 (Q2<0).
(1)固体CO2称干冰,属于___________晶体。氮原子最外层电子排布式是___________。
(2)氧元素的非金属性比碳强,用原子结构的知识说明理由_________________
(3)下列示意图中,能正确表示合成尿素过程中能量变化的是____________。
A、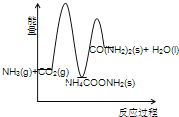 B、
B、
C、 D、
D、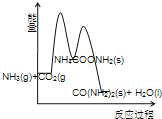
(4)写出合成尿素第一步反应的平衡常数表达式K=_________________________________。
(5)某实验小组模拟工业上合成尿素的条件,在恒定温度下,将氨气和二氧化碳按2:1的物质的量之比充入一体积为10L的密闭容器中(假设容器体积不变,生成物的体积忽略不计),经20min达到平衡,各物质浓度的变化曲线如图所示。
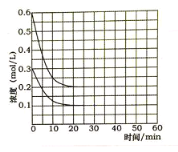
① 在上述条件下,从反应开始至20min时,二氧化碳的平均反应速率为___________。
② 为提高合成尿素的产率,下列可以采取的措施有____________。
a. 缩小反应容器的容积 b. 升高温度
c. 增加反应物的量 d. 使用合适的催化剂
③ 若保持平衡的温度和体积不变,25min 时再向容器中充入2mol氨气和1mol二氧化碳,在40min时重新达到平衡,请在下图中画出25~50min内氨气的浓度变化曲线____________。
=4时,CO2的转化率随时间的变化关系如图1所示.

 CO(NH3)2+H2O,当氨碳比
CO(NH3)2+H2O,当氨碳比




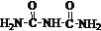 (缩二脲)+NH3 (副反应,程度较小)
(缩二脲)+NH3 (副反应,程度较小)
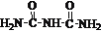 (缩二脲)+NH3 (副反应,程度较小)
(缩二脲)+NH3 (副反应,程度较小)
 B、
B、
 D、
D、

 B、
B、
 D、
D、
