部分短周期元素原子半径的相对大小、最高正价或最低负价随原子序数的变化关系如图所示:

下列说法正确的是
A. 离子半径的大小顺序:e>f>g>h
B. 与x形成简单化合物的沸点:y>z>d
C. x、z、d三种元素形成的化合物可能含有离子键
D. e、f、g、h四种元素对应最高价氧化物的水化物相互之间均能发生反应
高一化学单选题中等难度题
部分短周期元素原子半径的相对大小、最高正价或最低负价随原子序数的变化关系如图所示:

下列说法正确的是
A. 离子半径的大小顺序:e>f>g>h
B. 与x形成简单化合物的沸点:y>z>d
C. x、z、d三种元素形成的化合物可能含有离子键
D. e、f、g、h四种元素对应最高价氧化物的水化物相互之间均能发生反应
高一化学单选题中等难度题
部分短周期元素原子半径的相对大小、最高正价或最低负价随原子序数的变化关系如图所
示:
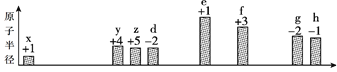
原子序数
下列说法不正确的是( )
A. x、z、d三种元素能形成具有强氧化性的酸
B. 根据g、h的单质与Fe反应的情况,可以判断h的非金属性大于g
C. 工业上通过电解f、h形成的化合物制取f 单质
D. x与其他元素可形成共价化合物或离子化合物
高一化学单选题中等难度题查看答案及解析
部分短周期元素原子半径的相对大小、最高正价或最低负价随原子序数的变化关系如图所示:

下列说法正确的是
A. 离子半径的大小顺序:e>f>g>h
B. 与x形成简单化合物的沸点:y>z>d
C. x、z、d三种元素形成的化合物可能含有离子键
D. e、f、g、h四种元素对应最高价氧化物的水化物相互之间均能发生反应
高一化学单选题中等难度题查看答案及解析
部分短周期元素原子半径的相对大小、最高正价或最低负价随原子序数的变化关系如图:
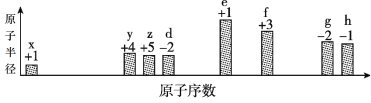
下列说法不正确的是
A.x、z、d三种元素能形成具有强氧化性的酸
B.g、h氧化物对应的水化物都是强酸
C.e最高价氧化物对应的水化物是强碱
D.f的氧化物是两性氧化物
高一化学单选题中等难度题查看答案及解析
随着原子序数的递增,八种短周期元素(用字母x等表示)原子半径的相对大小、最高正价或最低负价的变化如图所示,下列说法正确的是
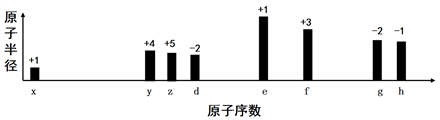
A. z和e的最高价氧化物对应的水化物能相互反应
B. 离子半径:f 3+>e+>d2-
C. g的气态氢化物含有非极性键
D. g的最高价氧化物和水反应生成的化合物是离子化合物
高一化学选择题中等难度题查看答案及解析
随原子序数的递增,八种短周期元素x、y、z、d、e、f、g、h原子半径的相对大小、最高正价或最低负价的变化如图所示。根据判断出的元素回答下列问题:

(1)比较y、g、h最高价氧化物对应水化物的酸性强弱是: > > (用化学式表示)
(2)由表中两种元素的原子按1:1组成的化合物A,A中既含离子键又含非极性共价键,其电子式为 ;
(3)下列元素序号中不是和y同一主族的是 。
a.14 b. 22 c. 50 d. 82
(4)上述元素可组成盐R:zx4f(gd4)2,向盛有10mL 1mol·L﹣1R溶液的烧杯中滴加1mol·L﹣1NaOH溶液,沉淀的物质的量随NaOH溶液体积变化如图所示:
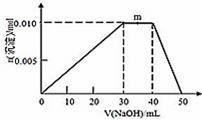
①写出m点反应的离子方程式 。
②若R溶液中改加20mL 1.2 mol·L﹣1 Ba(OH)2溶液,充分反应后,溶液中产生沉淀的物质的量为 mol。
高一化学简答题极难题查看答案及解析
随原子序数递增,八种短周期元素(用字母x等表示)原子半径的相对大小、最高正价或最低负价的变化如下图所示。下列说法错误的是( )
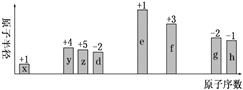
A. zh3中各原子最外层都达到8e-稳定结构
B. y与g可形成化合物yg2,结构式为g=y=g
C. d和f形成的简单离子半径大小关系为:d2- < f3+
D. f 和h 形成的化合物属于离子化合物
高一化学多选题中等难度题查看答案及解析
随原子序数递增,八种短周期元素(用字母x……表示)原子半径的相对大小、最高正价或最低
负价的变化如图所示。
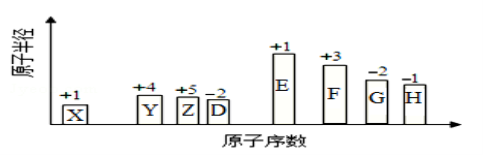
回答下列问题:
(1)H的离子结构示意图为__________________________。
(2)由E和D两元素形成的原子个数比为1∶1的化合物的电子式为______________。
(3)单质G易溶于YG2,则YG2的结构式为_______________。
(4)Z2X4是一种高效清洁的火箭燃料,8g该物质含有的共用电子对数目为_____________。
(5)上述元素可组成盐R:ZX4F(GD4)2。向盛有10mL1mol·L-1R溶液的烧杯中滴加1mol·L-1NaOH溶液,沉淀物质的量随NaOH溶液体积的变化如图所示,则m点对应的离子方程式为_____________。

高一化学简答题困难题查看答案及解析
随原子序数的递增,八种短周期元素(用字母表示)原子半径的相对大小、最高正价或最低负价的变化如下图所示。

请回答下列问题:
(1)f在元素周期表的位置是__________。
(2)比较d、e常见离子的半径的大小(用化学式表示,下同)_________________;比较g、h的最高价氧化物对应的水化物的酸性强弱:________________。
(3)任选上述元素组成一种四原子共价化合物,写出其电子式__________。
(4)上述元素可组成盐R:zx4f(gd4)2,向盛有10 mL 1 mol·L−1 R溶液的烧杯中滴加1 mol·L−1 NaOH溶液,沉淀物质的量随NaOH溶液体积变化示意图如下:
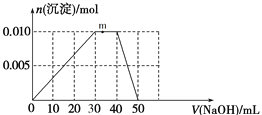
①写出m点反应的离子方程式_____________________________。
②若R溶液改加20 mL1.2 mol·L−1Ba(OH)2溶液,充分反应后,溶液中产生沉淀的物质的量为__________mol。
高一化学综合题中等难度题查看答案及解析
随原子序数的递增,八种短周期元素(用字母x等表示)原子半径的相对大小、最高正价或最低负价的变化如图所示。根据判断出的元素回答问题:


(1)f在元素周期表的位置是____________________________。
(2)比较d、e常见离子的半径大小______>______(用化学式表示,下同);比较g、h的最高价氧化物对应的水化物的酸性强弱___________>____________。
(3)任选上述元素组成一种四原子共价化合物,写出其电子式______________________。
(4)上述元素可组成盐R:zx4f(gd4)2,向盛有10 mL 1 mol·L-1 R溶液的烧杯中滴加1 mol·L-1 NaOH溶液,沉淀物质的量随NaOH溶液体积变化如图所示。
① 写出m段反应的离子方程式_______________________________。
② 若在R溶液中改加20 mL 1.2 mol·L-1 Ba(OH)2溶液,充分反应后,溶液中产生沉淀的物质的量为___________mol。
高一化学填空题极难题查看答案及解析
有8种短周期元素,随着原子序数的递增(横坐标),其原子半径相对大小、最高正价或最低负价的变化情况如图所示。
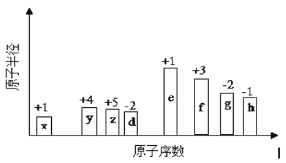
(1)元素h在周期表中的位置是____________。
(2)元素x和y形成的最简单化合物在家庭生活中的用途是____________。
(3)元素e、f最高价氧化物对应水化物的碱性强的是____________。(写化学式)
(4)元素z、x可形成原子个数比为1﹕3的化合物,其电子式为____________。
高一化学推断题简单题查看答案及解析