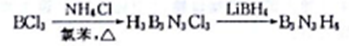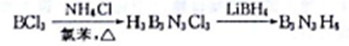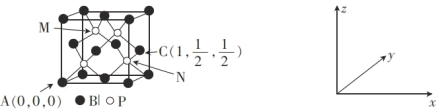-
ⅣA族元素(C、Si、Ge、Sn、Pb)及其化合物在材料等方面有重要用途。回答下列问题:
(1) Pb的价层电子排布图为:____________;
(2)GeC14的中心原子的价层电子对数为____________,分子的立体构型为___________。GeC14可水解生成一种氧化物和一种无氧酸,其化学反应方程式为:________________________________。
(3)四卤化硅 的沸点和二卤化铅
的沸点和二卤化铅 的熔点如下图所示。
的熔点如下图所示。
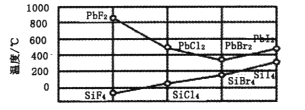
① 的沸点依F、CI、Br、I次序升高的原因是____________。
的沸点依F、CI、Br、I次序升高的原因是____________。
②结合 的沸点和
的沸点和 的熔点的变化规律,可推断:依F、Cl、Br、I次序,
的熔点的变化规律,可推断:依F、Cl、Br、I次序, 中化学键的离子性__________(填“增强”“不变”或“减弱”,下同)、共价性__________。
中化学键的离子性__________(填“增强”“不变”或“减弱”,下同)、共价性__________。
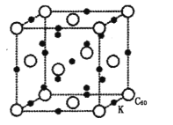
(4)碳的另一种单质 可以与钾形成低温超导化合物,晶胞结构如图所示。此化合物可看成是K填充在
可以与钾形成低温超导化合物,晶胞结构如图所示。此化合物可看成是K填充在 形成的所有四面体间隙和八面体间隙之中,其四面体间隙数目为_________。另有一种碱金属X(相对原子质量为M)与
形成的所有四面体间隙和八面体间隙之中,其四面体间隙数目为_________。另有一种碱金属X(相对原子质量为M)与 可形成类似化合物,但X只填充
可形成类似化合物,但X只填充 形成的八面体间隙的一半,此化合物的化学式为:__________,其晶胞参数为1.4nm,晶体密度为_________
形成的八面体间隙的一半,此化合物的化学式为:__________,其晶胞参数为1.4nm,晶体密度为_________ (用含M和阿伏伽德罗常数的值
(用含M和阿伏伽德罗常数的值 的式子表示)
的式子表示)
-
Ⅰ.硼元素B在化学中有很重要的地位。硼的化合物在农业、医药、玻璃工业等方面用途很广。请回答下列问题:
(1)写出与B元素同主族的Ga元素的基态原子核外电子排布简式 。从原子结构的角度分析,B、N、O元素的第一电离能由大到小的顺序为 。
(2)立方氮化硼可利用人工方法在高温高压条件下合成,属于超硬材料。同数原子晶体的氮化硼(BN)比晶体硅具有更高硬度和耐热性的原因是 。
(3)在BF3分子中中心原子的杂化轨道类型是 ,SiF4微粒的空间构型是 。又知若有d轨道参与杂化,能大大提高中心原子成键能力,试解释为什么BF3、SiF4水解的产物中,除了相应的酸外,前者生成BF4-,后者却是生成SiF62-: 。
Ⅱ.图所示为血红蛋白和肌红蛋白的活性部分---血红素的结构:
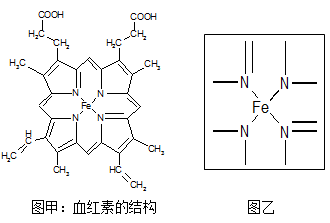
回答下列问题:
(1)根据元素电负性请判断H2N-CHO中碳和氮的化合价分别为 和 。
(2)血红素中两种氮原子的杂化方式分别为 , ;在图乙的方框内用“→”标出亚铁离子的配位键。
-
硼元素在化学中有很重要的地位。硼的化合物在农业、医药等方面用途很广。请回答下列问题:
(1)写出与B元素同主族的Ga元素的基态原子核外电子排布式 。
从原子结构的角度分析,B、N、O元素的第一电离能由大到小的顺序为 。
(2)立方氮化硼可利用人工方法在高温高压条件下合成,属于超硬材料。同属原子晶体的氮化硼(BN)比晶体硅具有更高硬度和耐热性的原因是 。
(3)在BF3分子中中心原子的杂化轨道类型是 ,SiF4粒子的空间构型是 。又知若有d轨道参与杂化,能大大提高中心原子成键能力。试解释为什么BF3、SiF4水解的产物中,除了相应的酸外,前者生成BF后者却是生成 : 。
: 。
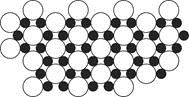
(4)科学家发现硼化镁在39 K时呈超导性,在硼化镁晶体的理想模型中,镁原子和硼原子是分层排布的,一层镁一层硼相间排列。下图是该晶体微观空间中取出的部分原子沿z轴方向的投影,白球是镁原子投影,黑球是硼原子投影,图中的硼原子和镁原子投影在同一平面上。根据图示确定硼化镁的化学式为 。
-
硼元素B在化学中有很重要的地位。硼的化合物在农业、医药、玻璃等方面用途很广。请回答下列问题:
(1)写出与B元素同主族的Ga元素的基态原子核外电子排布式_________________。从原子结构的角度分析,B、N、O元素的第一电离能由大到小的顺序为___________。
(2)立方氮化硼可利用人工方法在高温高压条件下合成,属于超硬材料。同属原子晶体的氮化硼(BN)比晶体硅具有更高硬度和耐热性的原因是_____________________________。
(3)在BF3分子中中心原子的杂化轨道类型是__________,SiF4微粒的空间构型是__________。又知若有d轨道参与杂化,能大大提高中心原子成键能力。试解释为什么BF3、SiF4水解的产物中,除了相应的酸外,前者生成BF4一后者却是生成SiF62—:______________________________________________。
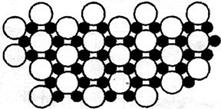
(4)科学家发现硼化镁在39K时呈超导性,在硼化镁晶体的理想模型中,镁原子和硼原子是分层排布的,一层镁一层硼相间排列。下图是该晶体微观空间中取出的部分原子沿Z轴方向的投影,白球是镁原子投影,黑球是硼原子投影,图中的硼原子和镁原子投影在同一平面上。根据图示确定硼化镁的化学式为_______。
-
硼元素在化学中有很重要的地位。硼的化合物在农业、医药等方面用途很广。请回答下列问题:
(1)写出与B元素同主族的Ga元素的基态原子核外电子排布式________________________________________________________________________。
从原子结构的角度分析,B、N、O元素的第一电离能由大到小的顺序为________。
(2)立方氮化硼可利用人工方法在高温高压条件下合成,属于超硬材料。同属原子晶体的氮化硼(BN)比晶体硅具有更高硬度和耐热性的原因是________________________________________________________________________________________________________________________________________________。
(3)在BF3分子中中心原子的杂化轨道类型是________,SiF4粒子的空间构型是________。又知若有d轨道参与杂化,能大大提高中心原子成键能力。试解释为什么BF3、SiF4水解的产物中,除了相应的酸外,前者生成BF4-后者却是生成SiF62-:________________________________________________________________________
________________________________________________________________________。
(4)科学家发现硼化镁在39 K时呈超导性,在硼化镁晶体的理想模型中,镁原子和硼原子是分层排布的,一层镁一层硼相间排列。图是该晶体微观空间中取出的部分原子沿z轴方向的投影,白球是镁原子投影,黑球是硼原子投影,图中的硼原子和镁原子投影在同一平面上。根据图示确定硼化镁的化学式为________。

-
硼及其化合物在材料制造、有机合成等方面用途非常广泛。回答下列问题:
(1)VB2是一种导电陶瓷材料,基态钒原子的价电子排布图为___________
(2)B、C、N、O四种元素第一电离能由小到大的顺序为_______________。
(3)硼的卤化物在工业中有重要作用,硼的四种卤化物的沸点如下表所示:
| 卤化物 | BF3 | BCl3 | BBr3 | BI3 |
| 沸点/K | 172 | 285 | 364 | 483 |
①四种卤化物沸点依次升高的原因是_________________。
②用BF3分子结构解释反应BF3(g)+NH4F(s)=NH4BF4(s)能够发生的原因:_________________。
③制备环硼氨烷的方法如下:

BCl3、LiBH4中硼原子的杂化轨道类型依次为_________________;与B3N3H6互为等电子体的分子的结构简式为___________________。
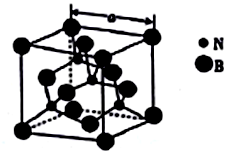
(4)立方氮化硼的晶胞结构与金刚石结构相似(如下图),是超硬材料。
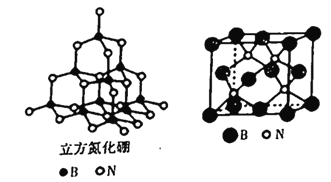
①晶胞中每个氮原子周围与其最近且等距离的硼原子有_____个;
②结构化学上常用原子坐标参数表示晶胞内部各原子的相对位置,立方氮化硼的晶胞中, B原子的坐标参数分别有:B(0,0,0),B( ,0,
,0,  );B(0,
);B(0,  ,
,  )等,则距离上述三个B原子最近且等距离的N原子的坐标参数为___________________。
)等,则距离上述三个B原子最近且等距离的N原子的坐标参数为___________________。
③已知氮化硼晶胞边长为apm,则氮化硼晶体的密度为____g·cm-3(设NA为阿伏加德罗常数值,只要求列算式)。
-
硼及其化合物在材料制造、有机合成等方面用途非常广泛。回答下列问题:
(1) VB2是一种导电陶瓷材料,基态钒原子的价电子排布图为_______。
(2)B、C、N三种元素第一电离能由小到大的顺序为________。
(3)硼的卤化物在工业中有重要作用,硼的四种卤化物的沸点如下表所示。
| BF3 | BCl3 | BBr3 | BI3 |
| 沸点/K | 172 | 285 | 364 | 483 |
①四种卤化物沸点依次升高的原因是__________________。
②用BF3分子结构解释反应BF3(g)+NH4F(s)==NH4[BF4] (s)能够发生的原因:____________。
制备环硼氨烷的方法如下:
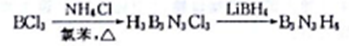
BCl3、LiBH4中硼原子的杂化轨道类型依次为_________;与B3N3H6互为等电子体的分子的结构简式为________________。
(4)立方氮化硼的熔点为3000℃,其晶胞结构如图所示,晶胞参数a=361.5pm。
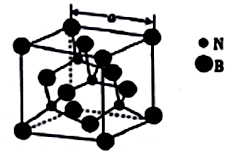
①立方氮化硼的晶体类型为_______________。
②紧邻的两个硼原子间的距离为_______(列出计算式即可) pm。
③立方氮化硼的密度为_____(列出计算式即可)g•㎝-3。
-
硼及其化合物在材料制造、有机合成等方面用途非常广泛。回答下列问题:
(1) VB2是一种导电陶瓷材料,基态钒原子的价电子排布图为_______。
(2)B、C、N三种元素第一电离能由小到大的顺序为________。
(3)硼的卤化物在工业中有重要作用,硼的四种卤化物的沸点如下表所示。
| BF3 | BCl3 | BBr3 | BI3 |
| 沸点/K | 172 | 285 | 364 | 483 |
①四种卤化物沸点依次升高的原因是__________________。
②用BF3分子结构解释反应BF3(g)+NH4F(s)==NH4[BF4] (s)能够发生的原因:____________。
制备环硼氨烷的方法如下:
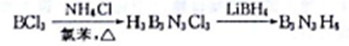
BCl3、LiBH4中硼原子的杂化轨道类型依次为_________;与B3N3H6互为等电子体的分子的结构简式为________________。
(4)立方氮化硼的熔点为3000℃,其晶胞结构如图所示,晶胞参数a=361.5pm。
①立方氮化硼的晶体类型为_______________。
②紧邻的两个硼原子间的距离为_______(列出计算式即可) pm。
③立方氮化硼的密度为_____(列出计算式即可)g•㎝-3。
-
硼及其化合物在新材料、工农业生产等方面用途很广。请回答下列问题:
(1)写出与B元素同主族的Ga元素的基态原子核外电子排布式:________。
(2)立方氮化硼(BN)可利用人工方法在高温高压条件下合成,属于超硬材料。同属原子晶体的氮化硼比晶体硅具有更高的硬度和耐热性的原因是__________。
(3)BF3分子中中心原子的杂化轨道类型是____。又知若有d轨道参与杂化,能大大提高中心原子的成键能力,分析BF3、SiF4水解的产物中, 除了相应的酸外,前者生成BF4-而后者生成SiF62-的原因:_______________。
(4)NaBH4被认为是有机化学中的“万能还原剂”,NaBH4的电子式为_________,其中三种元素的电负性由大到小的顺序是_______________。
(5)自然界中含硼元素的钠盐是一种天然矿藏,其化学式写作 Na2B4O7•10H2O,实际上它的结构单元是由两个H3BO3和两个B(OH)4]-(合而成的双六元环,应该写成 Na2[B4O5(OH)4]•8H2O,其结构如图所示,它的阴离子可形成链状结构,则该晶体中不存在的作用力是______________(填字母)。

A.离子键 B.共价键 C.氢键 D.金属键 E.范德华力
(6)磷化硼(BP)可作为金属表面的保护薄膜,其晶胞如图所示,在BP晶胞中P占据的是硼原子堆积的_____(填“立方体”“正四面体”或“正八面体”)空隙。建立如图所示坐标系,可得晶胞中A、C处原子的分数坐标,则N处的P原子分数坐标为______。若晶胞中硼原子和磷原子之间的最近核间距为a pm,则晶胞边长为____________cm。
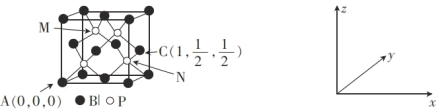
-
硼及其化合物在新材料、工农业生产等方面用途很广。请回答下列问题:
(1)写出与B元素同主族的 元素的基态原子核外电子排布式:____________________。
元素的基态原子核外电子排布式:____________________。
(2)立方氮化硼(BN)可利用人工方法在高温高压条件下合成,属于超硬材料。同属原子晶体的氮化硼比晶体硅具有更高的硬度和耐热性的原因是______________________。
(3) 分子中中心原子的杂化轨道类型是_________________,
分子中中心原子的杂化轨道类型是_________________, 微粒的空间构型是_____________。
微粒的空间构型是_____________。
(4) 被认为是有机化学中的“万能还原剂”,
被认为是有机化学中的“万能还原剂”, 的电子式为_____________,其中三种元素的电负性由大到小的顺序是_____________________。
的电子式为_____________,其中三种元素的电负性由大到小的顺序是_____________________。
(5)自然界中含硼元素的钠盐是一种天然矿藏,其化学式写作 ,实际上它的结构单元是由两个
,实际上它的结构单元是由两个 和两个
和两个 缩合而成的双六元环,应该写成
缩合而成的双六元环,应该写成 ,其结构如图所示,它的阴离子可形成链状结构,则该晶体中不存在的作用力是_______________(填字母)。
,其结构如图所示,它的阴离子可形成链状结构,则该晶体中不存在的作用力是_______________(填字母)。
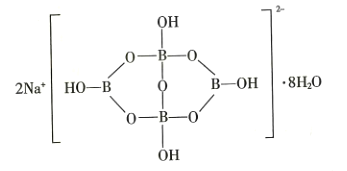
A.离子键 B.共价键 C.氢键 D.金属键 E.范德华力

(6)磷化硼的晶胞如图所示,其化学式为____________,若晶胞中硼原子与磷原子之间的最近核间距为apm,则晶胞边长为____________cm。
的沸点和二卤化铅
的熔点如下图所示。

的沸点依F、CI、Br、I次序升高的原因是____________。
的沸点和
的熔点的变化规律,可推断:依F、Cl、Br、I次序,
中化学键的离子性__________(填“增强”“不变”或“减弱”,下同)、共价性__________。

可以与钾形成低温超导化合物,晶胞结构如图所示。此化合物可看成是K填充在
形成的所有四面体间隙和八面体间隙之中,其四面体间隙数目为_________。另有一种碱金属X(相对原子质量为M)与
可形成类似化合物,但X只填充
形成的八面体间隙的一半,此化合物的化学式为:__________,其晶胞参数为1.4nm,晶体密度为_________
(用含M和阿伏伽德罗常数的值
的式子表示)