-
(加试题)氯化亚铜常用作有机合成工业中的催化剂,为白色晶体,不溶于乙醇,微溶于水,易溶于浓盐酸形成络合离子([CuCl2]-)。受潮露置空气中迅速氧化成碱式盐。实验室用下列流程制备:
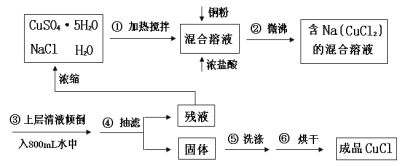
已知:Na[CuCl2](易电离,溶液无色)  NaCl+CuCl↓(白色沉淀)。
NaCl+CuCl↓(白色沉淀)。
请回答以下问题:
(1)写出实验室制取Na[CuCl2]的离子方程式__________
(2)判断步骤②反应完全的现象是____________
(3)步骤③的目的是__________________________________。
(4)步骤④有关抽滤操作,下列说法正确的是_______
A. 选择抽滤主要是为了加快过滤速度,得到较干燥的沉淀
B. 在吸滤瓶和抽气泵之间应连接一个安全瓶,吸滤瓶应与安全瓶的长导管相接
C. 抽滤时不宜过滤胶状沉淀,否则易在滤纸上形成一层密实的沉淀
D. 洗涤沉淀时,应关小水龙头,使洗涤剂缓缓通过沉淀物
(5)定量 称取1.850g CuCl样品(杂质不参与反应),溶于一定量的0.5000mol·L-1FeCl3溶液中,加水稀释至200mL得到溶液,取20.00mL 用0.1000mol·L-1的Ce(SO4)2溶液滴定到终点,消耗18.00mLCe(SO4)2 。
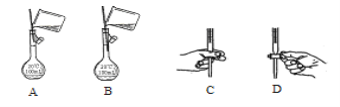
①此实验涉及溶液配制与定量滴定的基本操作中,其中合理的是___________;
②有关反应式:Fe3++CuCl=Fe2++Cu2++Cl- Ce4++Fe2+=Fe3++Ce3+则样品中CuCl的质量分数____________。
-
氯化亚铜(CuCl)常用作有机合成工业中的催化剂,是一种白色粉末;微溶于水、不溶于乙醇及稀硫酸。工业上采用如下工艺流程,从某酸性废液(主要含Cu2+、Fe3+、 H+、Cl-)中制备氯化亚铜。
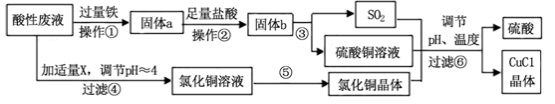
请回答下列问题:
(1)写出步骤①中发生的两个主要反应的离子方程式: 。
(2)步骤②的操作名称是: 。
(3)步骤④中所加物质X为: 。
(4)步骤⑤的操作是: 。
(5)步骤⑥应调节溶液pH呈酸性,且用乙醇洗涤CuCl晶体,目的是: 。
(6)在CuCl的生成过程中,可以循环利用的物质是 ,理论上 (填“是”或“不”)需要补充(不考虑调节等消耗);理由是 。
(7)工业上还可以采用以碳棒为电极电解CuCl2溶液得到CuCl。电解CuCl2溶液,阴极上发生的电极反应式是 。
-
三氯化铬是合成其它铬盐的重要原料,在无机合成和有机合成中有重要的作用,是合成饲料添加剂的主要成份,工业上主要用作媒染剂及催化剂。易溶于水,溶于乙醇,几乎不溶于乙醚,易潮解,易升华。在高温下能被氧气氧化,碱性条件下能被H2O2氧化为Cr(Ⅵ)且2 CrO42- + 2 H+ ⇌ Cr2O72- + H2O。制三氯化铬的流程如下:

(1)三氯化铬碱性条件下被H2O2氧化为Cr(Ⅵ)的离子反应方程式为__ 。
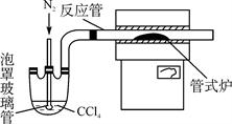
(2)已知CCl4沸点为57.6℃,为保证稳定的CCl4气流,适宜的加热方式是_________________。
(3)用如图装置制备CrCl3时,主要步骤包括:①将产物收集到蒸发皿中;②加热反应管至400℃,开始向三颈烧瓶中通入氮气,继续升温到650℃;③三颈烧瓶中装入150mLCCl4,并加热CCl4,温度控制在50~60℃之间;④反应管出口端出现了CrCl3升华物时,切断加热管式炉的电源;⑤停止加热CCl4,继续通入氮气;⑥检查装置气密性。正确的操作顺序为:⑥→③→__________,步骤②中通如氮气的作用_______________。
(4)已知反应管中发生的主要反应有:Cr2O3+3CCl4→2CrCl3+3COCl2,因光气剧毒,实验需在通风橱中进行,并用乙醇处理COCl2,生成一种含氧酸酯(C5H10O3),用乙醇处理尾气的化学方程式_____ 。
(5)样品中三氯化铬质量分数的测定称取样品0.3300g,加水溶解并定容于250mL容量瓶中。移取25.00mL于碘量瓶(一种带塞的锥形瓶)中,加热至沸后加入1gNa2O2,充分加热煮沸,适当稀释,然后加入过量的2mol/LH2SO4至溶液呈强酸性,此时铬以Cr2O72-存在,再加入1.1gKI,密塞,摇匀,于暗处静置5分钟后,加入1mL指示剂,用0.0250mol/L硫代硫酸钠溶液滴定至终点,平行测定三次,平均消耗标准硫代硫酸钠溶液24.00mL。
已知:Cr2O72-+6I-+14H+=2Cr3++3I2+7H2O,2Na2S2O3+I2=Na2S4O6+2NaI。
①指示剂为___________,滴定终点的现象为________________________________。
②移入碘量瓶的CrCl3溶液需加热煮沸,加入Na2O2后也要加热煮沸,其主要原因是 。
③样品中无水三氯化铬的质量分数为 。(计算结果精确到0.1%)
-
【加试题】常温下碘酸钙[Ca(IO3)2]是一种白色晶体,微溶于水,不溶于乙醇,能溶于盐酸,是目前广泛使用的既能补碘又能补钙的新型食品和词料添加剂。其制备原理如下:
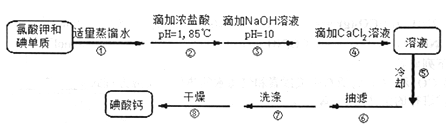
Ⅰ.碘酸钙的制备
(1)某同学设计的实验装置如下图所示(夹持装置已省略),步骤②的加热方式为_________。
(2)步骤⑤冷却热的饱和溶液没有析出晶体,为了得到晶体可以采取的一种措施是________。
(3)步骤⑦洗涤的具体操作是____________。
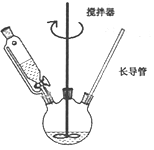
Ⅱ.产品纯度测定
准确称取0.5000 g样品,酸化溶解,定容至250 mL,从中取出25.00 mL试样于锥形瓶中,加入足量的KI充分反应,用0.04000 mol·L-1硫代硫酸钠溶液滴定至终点,重复以上步骤,所测得实验数据如下:
| 1 | 2 | 3 |
| 滴定起始读数/mL | 1.52 | 1.16 | 0.84 |
| 滴定终止读数/mL | 31.50 | 31.18 | 30.84 |
己知:2Na2S2O3 + I2= Na2S4O6 + 2NaI
(4)加入KI时发生反应的离子方程式是_____________。
(5)滴定时所用的指示剂是_________________.
(6)经计算产品的纯度为________________。
-
过渡金属的单质及化合物很多有催化性能,氯化铜、氯化亚铜经常用作有机合成催化剂。实验室中用氯气与粗铜(杂质只有Fe)反应,制备铜的氯化物的流程如下。
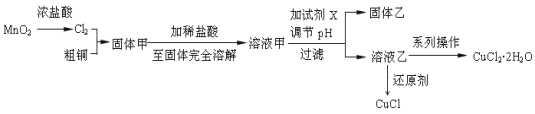
查阅资料:
氯化亚铜:白色微溶于水,在干燥空气中稳定,受潮则易变蓝到棕色,在热水中迅速水解生成氧化铜水合物而呈红色。
氯化铜:从水溶液中结晶时,在26~42℃得到二水物,在15℃以下得到四水物,在15~25.7℃得到三水物,在42℃以上得到一水物,在100℃得到无水物。
(1)现用如图所示的实验仪器及药品制备纯净、干燥的氯气并与粗铜反应(铁架台、铁夹省略)。
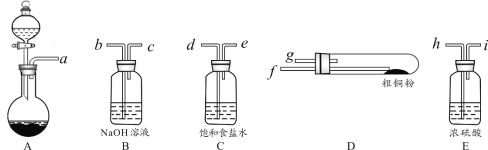
①按气流方向连接各仪器接口顺序是:a→_____、_____→ h 、i →_____、_____→_____。
②本套装置有两个仪器需要加热,加热的顺序为先_____后_____。
(2)分析流程:
①固体甲需要加稀盐酸溶解,其理由是_____;
②溶液甲可加试剂X用于调节pH以除去杂质, X可选用下列试剂中的(填序号)_____。
a.Cu(OH)2 b. NH3·H2O c.CuO d.CuSO4
③完成溶液乙到纯净CuCl2·2H2O晶体的系列操作步骤为:加少量盐酸、蒸发浓缩、___________、____________、洗涤、干燥。
(3)向溶液乙中加入适当的还原剂(如SO2、N2H4、SnCl2等),并微热得到CuCl沉淀,写出向乙溶液加入N2H4(氧化产物为无毒气体)的离子方程式:___________________________。
-
过渡金属的单质及化合物很多有催化性能,氯化铜、氯化亚铜经常用作有机合成催化剂。实验室中用氯气与粗铜(杂质只有Fe)反应,制备铜的氯化物的流程如下。
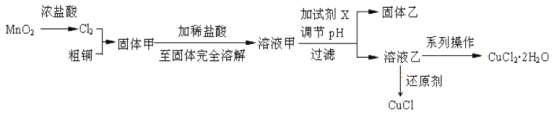
查阅资料:
氯化亚铜:白色微溶于水,在干燥空气中稳定,受潮则易变蓝到棕色,在热水中迅速水解生成氧化铜水合物而呈红色。
氯化铜:从水溶液中结晶时,在26~42℃得到二水物,在15℃以下得到四水物,在15~25.7℃得到三水物,在42℃以上得到一水物,在100℃得到无水物。
(1)现用如图所示的实验仪器及药品制备纯净、干燥的氯气并与粗铜反应(铁架台、铁夹省略)。
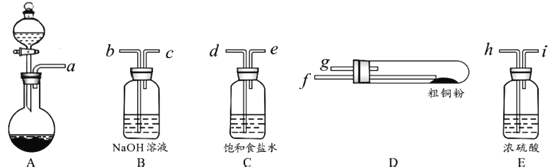
①按气流方向连接各仪器接口顺序是:a→_____、_____→h、i→_____、_____→_____。
②本套装置有两个仪器需要加热,加热的顺序为先_____后_____。
(2)分析流程:
①固体甲需要加稀盐酸溶解,其理由是_____;
②溶液甲可加试剂X用于调节pH以除去杂质,X可选用下列试剂中的(填序号)_____。
a Cu(OH)2 b NH3·H2O c CuO d CuSO4
查阅有关资料得到如下数据,常温下Fe(OH)3的溶度积Ksp=8.0×10-38,Cu(OH)2的溶度积Ksp=3.0×10-20,通常认为残留在溶液中的离子浓度小于1×10-5 mol·L-1时就认为沉淀完全,设溶液中CuSO4的浓度为3.0 mol·L-1,则Cu(OH)2开始沉淀时溶液的pH为________,Fe3+完全沉淀时溶液的pH为________。(提示:lg2=0.3)
③完成溶液乙到纯净CuCl2·2H2O晶体的系列操作步骤为:加少量盐酸、蒸发浓缩、________、_______、洗涤、干燥。
(3)向溶液乙中加入适当的还原剂(如SO2、N2H4、SnCl2等),并微热得到CuCl沉淀,写出向乙溶液加入N2H4(氧化产物为无毒气体)的离子方程式:____________。
-
过氧化钙(CaO2)是一种白色晶体,能潮解,难溶于水,可与水缓慢反应,不溶于乙醇,易与酸反应,常用作杀菌剂、防腐剂等。根据题意,回答相关问题。
I.CaO2晶体的制备:CaO2晶体通常可利用CaCl2在碱性条件下与H2O2反应制得。某化学兴趣小组在实验室制备CaO2的实验方案和装置示意图如下:
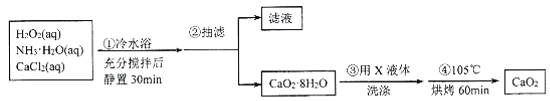
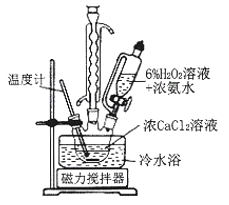
(1)三颈烧瓶中发生的主要反应的化学方程式为___________。
(2)冷水浴的目的是__;步骤③中洗涤CaO2·8H2O的实验操作方法是__
Ⅱ.CaO2含量的测定:测定CaO2样品纯度的方法是:称取0.200g样品于锥形瓶中,加入50mL水和15mL2mol·L-lHCl,振荡使样品溶解生成过氧化氢,再加入几滴MnCl2稀溶液,立即用0.0200mol·L-lKMnO4标准溶液滴定到终点,消耗25.00mL标准液。
(3)上述过程中使用稀盐酸而不使用稀硫酸溶解样品的原因是______;滴定前加入MnCl2稀溶液的作用可能是______。
(4)滴定过程中的离子方程式为____,样品中CaO2的质量分数为____。
(5)实验I制得的晶体样品中CaO2含量偏低的可能原因是:_______。
-
Ⅰ.下图所示的实验,能达到实验目的的是
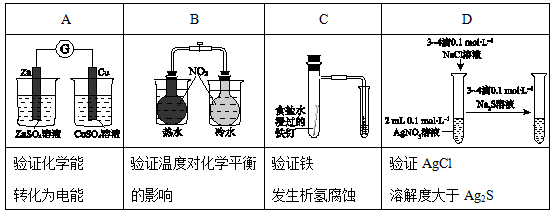
Ⅱ在氯化铜晶体(CuCl2·2H2O)中含有FeCl2杂质,为制得纯净的氯化铜晶体,首先将其溶于水后加少量盐酸配制成水溶液,然后按下图所示的操作步骤进行提纯。
已知:在pH=4~5时,Cu2+、Fe2+不水解,而Fe3+几乎完全水解而沉淀。
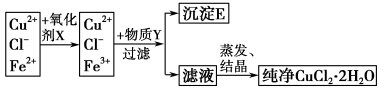
回答下列问题:
(1)下列物质都可以作为氧化剂,其中适合本实验的X是 (填字母)。
A.H2O2 B.KMnO4 C.氯水 D.K2Cr2O7
(2)写出加入氧化剂X后,发生反应的离子方程式(写一个即可) 。
(3)加入Y调节溶液的pH至4~5。物质Y可能是 (填字母)。
A.氨水 B.Cu C.Cu(OH)2 D. CuO
(4)欲将CuCl2·2H2O加热制得无水CuCl2,可在HCl气氛下蒸发,否则得不到纯净CuCl2固体。试用简要的文字和相应化学方程式解释这样操作的原因: 。
-
(14分)氯化铜晶体(CuCl2·xH2O)是重要的化工原料,可用作催化剂、消毒剂等。用孔雀石[主要含Cu2(OH)2CO3,还含少量Fe、Si的化合物]制备氯化铜晶体,方案如下:
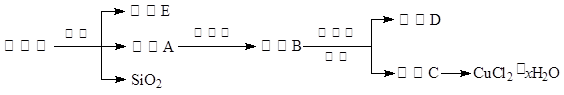
已知:有关金属离子从开始沉淀到沉淀完全时溶液的pH:
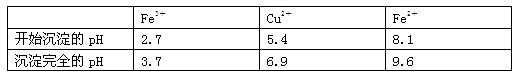
⑴酸溶时,为了提高浸取率可采取的措施有________。(写出一点)
⑵若溶液A含有的金属离子有Cu2+、Fe2+,则试剂①为Cl2,通入Cl2发生反应的离子方程式:________。
⑶加入试剂②的目的是调节pH至a,a的范围是________;
为避免引入杂质离子,试剂②可选用________。
A.氨水 B.氧化铜 C.氢氧化铜 D.氢氧化钠
⑷由溶液C获得CuCl2·xH2O,实验操作依次是加热浓缩、冷却结晶、过滤和洗涤等操作。加热浓缩过程需加入少量盐酸的目的是:________。
⑸工业生产过程会产生含Cu2+的废水,向废水加入碱调节pH=8,沉降后废水中Cu2+浓度为________mol/L。(已知Ksp[Cu(OH)2]=5.6×10-20)
⑹氯化亚铜(CuCl)也是一种重要的化工原料。
制备过程:向CuCl2溶液中通入一定量的SO2,加热一段时间后生成CuCl白色沉淀。写出制备CuCl的离子方程式:________。
-
CuCl2都是重要的化工原料,常用作催化剂、颜料、防腐剂和消毒剂等。已知:CuCl2溶与乙二胺(H2N—CH2—CH2—NH2),可形成配离子 ,该配离子不存在的化学键类型类型有( )
,该配离子不存在的化学键类型类型有( )
A.配位键 B.极性键 C.离子键 D.非极性键

NaCl+CuCl↓(白色沉淀)。














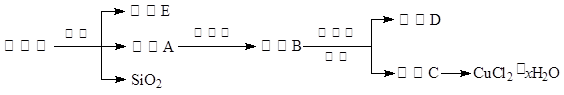

 ,该配离子不存在的化学键类型类型有( )
,该配离子不存在的化学键类型类型有( )