下列依据热化学方程式得出的结论正确的是
A. 已知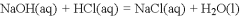
,则
固体与稀盐酸完全反应,放出的热量即为
B. 已知
则
C. 已知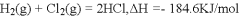 ,则反应物总能量小于生成物总能量
,则反应物总能量小于生成物总能量
D. 已知(白磷,s)=
(红磷,s)
,则白磷比红磷稳定
高一化学单选题简单题
下列依据热化学方程式得出的结论正确的是
A. 已知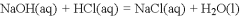
,则
固体与稀盐酸完全反应,放出的热量即为
B. 已知
则
C. 已知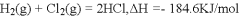 ,则反应物总能量小于生成物总能量
,则反应物总能量小于生成物总能量
D. 已知(白磷,s)=
(红磷,s)
,则白磷比红磷稳定
高一化学单选题简单题
下列依据热化学方程式得出的结论正确的是
A. 已知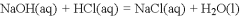
,则
固体与稀盐酸完全反应,放出的热量即为
B. 已知
则
C. 已知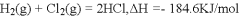 ,则反应物总能量小于生成物总能量
,则反应物总能量小于生成物总能量
D. 已知(白磷,s)=
(红磷,s)
,则白磷比红磷稳定
高一化学单选题简单题查看答案及解析
下列有关热化学方程式的叙述正确的是( )
A.已知C(石墨,s)C(金刚石,s) △H>0,则金刚石比石墨稳定
B.含20.0gNaOH的稀溶液与稀盐酸完全中和,放出28.7kJ的热量,则该反应的热化学方程式为:NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l) △H=-57.4kJ/mol
C.等质量的硫蒸气和硫固体分别完全燃烧,后者放出的热量多
D.N2(g)+3H2(g)2NH3(g);△H=-akJ·mol-1,则将14gN2(g)和足量H2置于一密闭容器中,充分反应后放出0.5akJ的热量
高一化学单选题中等难度题查看答案及解析
下列叙述不正确的是
A. 化学键的断裂和形成是化学反应中能量变化的根本原因
B. 酸碱中和反应一般是放热反应
C. 等质量的硫蒸气和硫固体分别完全燃烧,前者放出的热量多
D. 因为石墨变成金刚石吸热。所以金刚石比石墨稳定
高一化学单选题简单题查看答案及解析
下列叙述不正确的是
A. 化学键的断裂和化学反应中能量变化的根本原因
B. 凡吸热反应均需在加热条件下才能发生
C. 等质量的硫蒸气和硫固体分别完全燃烧,前者放出的热量多
D. 因为石墨变成金刚石吸热,所以金刚石比石墨稳定
高一化学多选题中等难度题查看答案及解析
下列说法正确的是( )
A. 需要加热的反应一定是吸热反应
B. 放热反应X(s)=Y(s),则X比Y稳定
C. 硫蒸气和硫固体分别完全燃烧,后者放出的热量更多
D. 在一个确定的化学反应关系中,反应物的总能量与生成物的总能量一定不同
高一化学单选题中等难度题查看答案及解析
下列叙述不正确的是
A.化学键的断裂和生成是化学反应中能量变化的根本原因
B.凡吸热反应均需在加热条件下才能发生
C.等质量的硫蒸气和硫固体分别完全燃烧,前者放出的热量多
D.因为石墨变成金刚石吸热,所以石墨比金刚石稳定
高一化学单选题简单题查看答案及解析
下列说法或表示方法中,正确的是( )
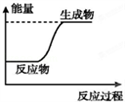
A. 等质量的硫蒸气和硫固体分别完全燃烧,前者放出的热量少
B. 如图可表示C和H2O(g)反应过程中的能量变化
C. 吸热反应一定要加热,才能进行
D. 已知中和热为57.3 kJ·mol-1,则浓硫酸与NaOH溶液反应生成 1mol H2O时, 共放出57.3 kJ的能量
高一化学选择题中等难度题查看答案及解析
为了说明影响化学反应快慢的因素,甲、乙、丙、丁四位同学分别设计了如下四个实验,你认为结论不正确的是
A. 甲将镁条放入过量的稀盐酸,反应速率逐渐加快,原因是该反应放出热量
B. 乙在实验室用锌和稀硫酸反应制取氢气时,向稀硫酸中滴入少量硫酸铜溶液,可以加快反应速率
C. 丙利用两支试管中分别加入相同质量的氯酸钾,其中一支试管中再加入少量二氧化锰,同时加热,产生氧气的快慢相同
D. 相同条件下等质量的块状和粉末状大理石与相同浓度盐酸反应时,粉末状的反应速率快
高一化学单选题中等难度题查看答案及解析
已知一定条件下气体完全燃烧生成气态
和气态
,放出802.3kJ热量,则表示该反应的热化学方程式正确的是( )
A.
B.
C.
D.
高一化学单选题简单题查看答案及解析
下列有关热化学方程式的叙述中,正确的是( )
A、含20.0gNaOH的稀溶液与稀盐酸完全中和,放出28.7kJ的热量,则表示该反应中和热的热化学方程式为NaOH (aq) +HCl (aq) =NaCl(aq) +H2O(l)△H=+57.3kJ/mol
B、已知c(石墨,s)=C(金刚石,s) △H >0,则金刚石比石墨稳定
C、己知2H2(g) +O2 (g) =2H2O (g) △H=-453.6kJ/mol ,则氢气的燃烧热为241.8kJ
D、己知C(s)+O2 (g) =CO2(g)△H1;C(s)+O2(g)=CO(g) △H2,则△H 1<△H 2
高一化学选择题中等难度题查看答案及解析