-
在2 L的密闭容器内,500℃时反应2SO2(g)+O2(g)  2SO3(g)ΔH<0体系中,n(SO2)随时间的变化如表:
2SO3(g)ΔH<0体系中,n(SO2)随时间的变化如表:
| 时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
| n(SO2)(mol) | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
(1)写出该反应的平衡常数表达式:K=______________________。
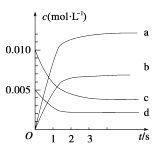
(2)下图表示SO3的变化的曲线是__________。用O2表示从0~2s内该反应的平均速率v=______________。
(3)能说明该反应已达到平衡状态的是________。
a.v(SO3)=2v(O2) b.容器内压强保持不变
c.v逆(SO2)=2v正(O2) d.容器内密度保持不变
(4)为使该反应的反应速率增大,且平衡向正反应方向移动的是________。
a.及时分离出SO3气体 b.适当升高温度 c.增大O2的浓度 d.选择高效催化剂
(5)若在容积均为2 L的密闭容器内,500℃时按不同方式投入反应物,发生反应2SO2(g)+O2(g) 2SO3(g)ΔH=-QkJ·mol-1(Q>0),保持恒温恒容。初始投料与各容器达到平衡时的有关数据如下:
2SO3(g)ΔH=-QkJ·mol-1(Q>0),保持恒温恒容。初始投料与各容器达到平衡时的有关数据如下:
| 实验 | 甲 | 乙 | 丙 |
| 初始投料 | 2molSO2、 1molO2 | 2molSO3 | 4molSO2、 2molO2 |
| 平衡时n(SO3) | 0.5mol | n2 | n3 |
| 反应的能量变化 | 放出Q1kJ | 吸收Q2kJ | 放出Q3kJ |
| 体系的压强 | p1 | p2 | p3 |
| 反应物的转化率 | α1 | α2 | α3 |
三个容器中的反应分别达平衡时下列各组数据关系正确的是____(填字母)。
A.α1+α2=1 B. Q1+Q2=Q C. α3<α1 D. p3<2p1=2p2 E. n2<n3<1.0mol F. Q3=2Q1
(6)在一定条件下进行反应2SO2(g)+O2(g)  2SO3(g),如图所示。
2SO3(g),如图所示。

相同温度下,在甲、乙两容器中各投入2molSO2、1molO2,甲、乙两容器的初始体积均为1L,甲、乙容器达到平衡所用时间:甲____(填“>”、“<”或“=”,下同)乙,平衡时SO2的转化率:甲____乙。
-
在密闭容器中进行反应:2SO2(g)+O2(g) 2SO3(g)( 正反应放热),如图是某次实验的化学反应速率随时间变化的图像,推断在t1时刻突然变化的条件可能是( )
2SO3(g)( 正反应放热),如图是某次实验的化学反应速率随时间变化的图像,推断在t1时刻突然变化的条件可能是( )
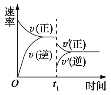
A.降低体系温度 B.减小生成物的浓度
C.催化剂失效 D.增大容器的体积
-
(1)500℃时,在2L密闭容器内发生2SO2(g)+O2(g) 2SO3(g)的反应,其中n(SO2)随时间的变化如下表:
2SO3(g)的反应,其中n(SO2)随时间的变化如下表:
| 时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
| n(SO2)/mol | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
①在第5s时,SO2的转化率为__________________。
②能说明该反应已达到平衡状态的是_________________。
a. v(SO2)=v(O2) b.混合气体中SO2的体积分数保持不变
c.v逆(SO2)=2v正(O2) d.容器内密度保持不变
(2)硅是信息技术的关键材料。
| 化学键 | H-H | Si-Cl | Si-Si | H-Cl |
| E/kJ·mol-1 | 436.0 | 360 | 176 | 431.8 |
用H2还原气态SiCl4制得28g硅的反应热为__________________。
(3)目前,消除氮氧化物污染有多种方法。
用CH4催化还原氮氧化物可以消除氮氧化物的污染。已知:
①CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) ΔH=-574 kJ·mol-1
②CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g) ΔH=-1160 kJ·mol-1
③H2O(g)=H2O(l) ΔH=-44.0 kJ·mol-1
写出CH4(g)与NO2(g)反应生成N2(g)、CO2(g)和H2O(l)的热化学方程式_______。
-
在温度不变的条件下,密闭容器中发生如下反应:2SO2(g)+O2(g) 2SO3(g),下列叙述能够说明反应已经达到平衡状态的是
2SO3(g),下列叙述能够说明反应已经达到平衡状态的是
A.容器中SO2、O2、SO3共存
B.反应容器中压强不随时间变化
C.容器中SO2、O2、SO3的物质的量之比为2∶1∶2
D.SO2与SO3的浓度相等
-
恒温下,物质的量之比为2∶1的SO2和O2的混合气体在容积为2L的恒容密闭容器中发生反应: 2SO2(g)+O2(g) 2SO3(g) (正反应为放热反应),n(SO2)随时间变化关系如下表:
2SO3(g) (正反应为放热反应),n(SO2)随时间变化关系如下表:
| 时间/min | 0 | 1 | 2 | 3 | 4 | 5 |
| n(SO2)/mol | 0.20 | 0.16 | 0.13 | 0.11 | 0.08 | 0.08 |
下列说法正确的是( )
A. 该反应进行到第3分钟时,逆反应速率大于正反应速率
B. 若要提高SO2的转化率,可用空气代替纯氧气并鼓入过量空气
C. 从反应开始到达到平衡,用SO3表示的平均反应速率为0.01 mol/(L·min)
D. 容器内达到平衡状态时的压强与起始时的压强之比为5∶4
-
一密闭体系中发生反应:2SO2(g)+O2(g) 2SO3(g),下图表示该反应的速率(v)在某一时间(t)段内的变化。则下列时间段中,SO3的百分含量最高的是
2SO3(g),下图表示该反应的速率(v)在某一时间(t)段内的变化。则下列时间段中,SO3的百分含量最高的是
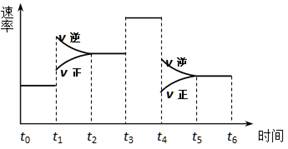
A.t0→t1 B.t2→t3 C.t3→t4 D.t5→t6
-
在一定温度下,固定体积为2L密闭容器中,发生反应:
2SO2(g)+O2(g) 2SO3(g ) ΔH <0,n(SO2)随时间的变化如表:
2SO3(g ) ΔH <0,n(SO2)随时间的变化如表:
| 时间/min | 0 | 1 | 2 | 3 | 4 | 5 |
| n(SO2)/mol | 0.20 | 0.16 | 0.13 | 0.11 | 0.08 | 0.08 |
则下列说法正确的是
A. 当v(SO2)=v(SO3)时,说明该反应已达到平衡状态
B. 用O2表示0~4 min内该反应的平均速率为0.005 mol/(L·min)
C. 平衡时再通入O2,平衡右移,O2转化率减小,SO2转化率增大
D. 若升高温度,则SO2的反应速率会变大,平衡常数K值会增大
-
某恒温固定体积为2 L密闭容器中,发生反应:2SO2(g)+ O2(g)  2SO3(g) ΔH <0,n(SO2)随时间的变化如表:
2SO3(g) ΔH <0,n(SO2)随时间的变化如表:
| 时间/min | 0 | 1 | 2 | 3 | 4 | 5 |
| n(SO2)/mol | 0.20 | 0.16 | 0.13 | 0.11 | 0.08 | 0.08 |
则下列说法正确的是
A. 当容器中气体的密度不变时,说明该反应已达到平衡状态
B. 用O2表示0~4 min内该反应的平均速率为0.005 mol/(L·min)
C. 若升高温度,则SO2的反应速率会变大,平衡常数K值会增大
D. 平衡时再通入18O2,平衡右移,再次平衡时各物质均含有18O,O2的转化率减小
-
某温度下容积固定的密闭容器中进行反应2SO2(g)+O2(g)⇌2SO3(g),下列各选项中,不能表明反应已达平衡的是
A.容器中气体物质的量不随时间而变化 B.反应物的转化率不随时间而变化
C.2v(O2)正=v(SO3)逆 D.容器中气体的密度不随时间而变化
-
可逆反应2SO2(g)+O2(g)  2SO3(g),在体积为2L的密闭容器中进行,如果SO2在某时刻的物质的量为4mol,2min后变为3.6mol,则用O2的浓度变化表示这段时间的反应速率为( )mol·(L·min) -1
2SO3(g),在体积为2L的密闭容器中进行,如果SO2在某时刻的物质的量为4mol,2min后变为3.6mol,则用O2的浓度变化表示这段时间的反应速率为( )mol·(L·min) -1
A.0.05 B. 0.2 C. 0.1 D. 0.4
2SO3(g)ΔH<0体系中,n(SO2)随时间的变化如表:

2SO3(g)ΔH=-QkJ·mol-1(Q>0),保持恒温恒容。初始投料与各容器达到平衡时的有关数据如下:
2SO3(g),如图所示。

