-
现有某铁碳合金,某化学兴趣小组为了测定铁碳合金中铁的质量分数,并探究浓硫酸的还原产物,设计了如图所示的实验装置和实验方案(夹持仪器已省略),请你参与此项活动并回答相应问题:
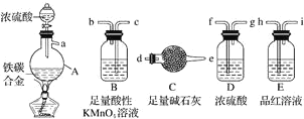
(1)该装置的连接顺序a___(填接口字母),连接好装置后,首先应进行的操作是____。
(2)mg铁碳合金中加入浓H2SO4,点燃酒精灯一段时间后,用滴管吸取A中的溶液滴入到适量水中作为试样,试样中所含金属离子的成分有以下三种可能:A:只含有Fe3+;B:只含有Fe2+;C:____,若为A,则A中反应的化学方程式为___,验证C种可能的实验方法___。
(3)待A中不再逸出气体时,停止加热,拆下C并称重,C增重bg。铁碳合金中铁的质量分数____(写表达式)。
(4)某同学认为利用此装置测得铁的质量分数偏大,请你写出可能的原因:_____。
(5)随着反应的进行,A中还可能发生某些离子反应。写出相应的离子方程式____。
-
现有某铁碳合金,某化学兴趣小组为了测定铁碳合金中铁的质量分数,并探究浓硫酸的还原产物,设计了如图所示的实验装置和实验方案(夹持仪器已省略),请你参与此项活动并回答相应问题:
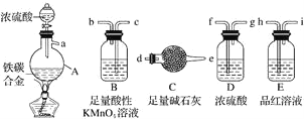
(1)该装置的连接顺序a___(填接口字母),连接好装置后,首先应进行的操作是____。
(2)mg铁碳合金中加入浓H2SO4,点燃酒精灯一段时间后,用滴管吸取A中的溶液滴入到适量水中作为试样,试样中所含金属离子的成分有以下三种可能:A:只含有Fe3+;B:只含有Fe2+;C:____,若为A,则A中反应的化学方程式为___,验证C种可能的实验方法___。
(3)待A中不再逸出气体时,停止加热,拆下C并称重,C增重bg。铁碳合金中铁的质量分数____(写表达式)。
(4)某同学认为利用此装置测得铁的质量分数偏大,请你写出可能的原因:_____。
(5)随着反应的进行,A中还可能发生某些离子反应。写出相应的离子方程式____。
-
现有某铁碳合金,某化学兴趣小组为了测定铁碳合金中铁的质量分数,并探究浓硫酸的某些性质,设计了下图所示的实验装置和实验方案(夹持仪器已省略),请你参与此项活动并回答相应问题(由实验装置引起的实验误差忽略不计)。
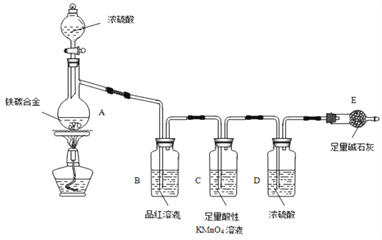
I、探究浓硫酸的某些性质
(1)按图示连接装置,检查装置___________,称量E的质量。
(2)将aɡ铁碳合金样品放入A中,再加入适量的浓硫酸,仪器A的名称为______,未点燃酒精灯前,A、B 均无明显现象,其原因是______________________。
(3)点燃酒精灯一段时间后,A、B中可观察到明显的现象,如A中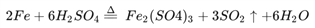 ,写出A中C和浓硫酸发生反应的化学方程式:__________________________,B中的现象是_________________,因此可得到浓硫酸具有_____________性。
,写出A中C和浓硫酸发生反应的化学方程式:__________________________,B中的现象是_________________,因此可得到浓硫酸具有_____________性。
(4)随着反应的进行,浓硫酸浓度逐渐减小变为稀硫酸,A中还可能发生某些离子反应,写出相应的离子方程式:_________________、____________________。
II、测定铁的质量分数
(5)待A中固体完全消失并不再逸出气体时,停止加热,拆下E并称重,E增重bg。铁碳合金中铁的质量分数为___________________(写表达式)。
(6)某同学认为上述方法较复杂,使用如图所示的装置和其他常用的实验仪器测定某些数据即可。为了快速和准确地计算出铁的质量分数,最简便的实验操作是___________(填写代号)。
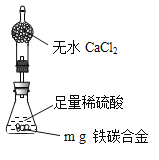
①用排水法测定H2的体积
②反应结束后,过滤、洗涤、干燥、称量残渣的质量
③ 测定反应前后装置和药品的总质量ag
【答案】气密性 蒸馏烧瓶 常温下,铁被浓硫酸钝化 C+2H2SO4(浓) CO2↑+2SO2↑+2H2O 品红溶液逐渐褪色 强氧化 2Fe3++Fe=3Fe2+ Fe+2H+=Fe2++H2↑
CO2↑+2SO2↑+2H2O 品红溶液逐渐褪色 强氧化 2Fe3++Fe=3Fe2+ Fe+2H+=Fe2++H2↑ 
③
【解析】
(1)按图示连接好装置以后,首先检查装置的气密性:(2)根据仪器构造可知仪器A的名称为蒸馏烧瓶;常温下Fe在浓硫酸中钝化,碳不与浓硫酸反应,故无明显现象;(3)浓硫酸具有强氧化性,在加热的条件下碳与浓硫酸反应的方程式为C+2H2SO4(浓) CO2↑+2SO2↑+2H2O;二氧化硫具有漂白性,因此B中的现象是品红溶液逐渐褪色,根据以上分析可知浓硫酸具有强氧化性;(4)硫酸浓度减小后,稀硫酸与铁发生置换反应生成硫酸亚铁和氢气,另外铁还能与硫酸铁反应生成硫酸亚铁,离子方程式分别为Fe+2H+=Fe2++H2↑、2Fe3++Fe=3Fe2+;(5)称取ag铁碳合金,加入过量浓硫酸,加热待A中不再逸出气体时,停止加热,拆下E装置并称重,E增重bg,则生成二氧化碳的质量为bg,根据质量守恒定律,则ag铁碳合金中含碳元素的质量为
CO2↑+2SO2↑+2H2O;二氧化硫具有漂白性,因此B中的现象是品红溶液逐渐褪色,根据以上分析可知浓硫酸具有强氧化性;(4)硫酸浓度减小后,稀硫酸与铁发生置换反应生成硫酸亚铁和氢气,另外铁还能与硫酸铁反应生成硫酸亚铁,离子方程式分别为Fe+2H+=Fe2++H2↑、2Fe3++Fe=3Fe2+;(5)称取ag铁碳合金,加入过量浓硫酸,加热待A中不再逸出气体时,停止加热,拆下E装置并称重,E增重bg,则生成二氧化碳的质量为bg,根据质量守恒定律,则ag铁碳合金中含碳元素的质量为 ,则含铁的质量为
,则含铁的质量为 ,铁的质量分数为
,铁的质量分数为 ;(6)因为铁炭合金中的铁可以与稀硫酸反应生成氢气,瓶总质量的减少量即为氢气的生成量,而铁的质量可以通过氢气的质量求出,答案选③。
;(6)因为铁炭合金中的铁可以与稀硫酸反应生成氢气,瓶总质量的减少量即为氢气的生成量,而铁的质量可以通过氢气的质量求出,答案选③。
【题型】实验题
【结束】
29
现有一种铜粉和铝粉的混合物样品,为测定该样品中铝的含量,称取5.0g此样品置于锥形瓶中,将100mL稀盐酸加入其中恰好完全反应,剩余固体2.3g.
(1)求该混合物中铝的质量分数为多少?
(2)所用盐酸中溶质的物质的量浓度为多少?
-
(20分)现有某铁碳合金,某化学兴趣小组为了测定铁碳合金中铁的质量分数,并探究浓硫酸的某些性质,设计了下图所示的实验装置和实验方案(夹持仪器已省略),请你参与此项活动并回答相应问题(由实验装置引起的实验误差忽略不计)。
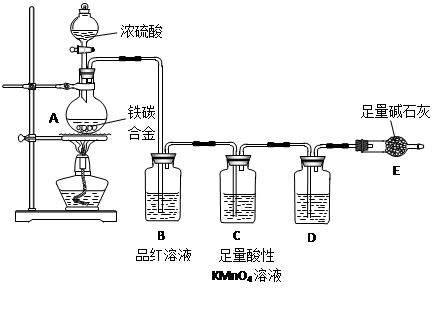
I. 探究浓硫酸的某些性质
(1)按图示的连接装置,检查装置的气密性,称量E的质量;
(2)将m g铁碳合金样品放入A中,再加入适量的浓硫酸;
(3)点燃酒精灯一段时间后,A、B中可观察到明显的现象:
写出A中发生反应的化学方程式___________________________________________(任写一个); B中的现象是________________________________________,由此可得到浓硫酸具有____________性;C中足量的酸性KMnO4溶液所起的作用是________________________;
D中盛放的试剂是_______________。
(4)随着反应的进行,A中还可能发生某些离子反应。写出相应的离子方程式:
___________________________________(任写一个)。
Ⅱ.测定铁的质量分数
(5)待A中不再逸出气体时,停止加热,拆下E并称重,E增重b g,则铁碳合金中铁的质量分数为:___________________________________________(写表达式);
某同学认为:依据此实验测得的数据,计算合金中铁的质量分数可能会偏低,你认为可能的原因是_____________________________________________________________________;
(6)经过大家的讨论,决定采用下列装置和其他常用实验仪器测定某些数据即可,为了快速和准确地计算出铁的质量分数,最简便的实验操作是___________(填写代号)。
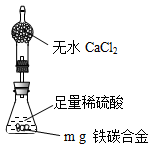
①用排水法测定H2的体积
②反应结束后,过滤、洗涤、干燥、称量残渣的质量
③ 测定反应前后装置和药品的总质量
-
某校化学兴趣小组设计了图示实验装置(图中省略了夹持仪器)来测定某铁碳合金中铁的质量分数.
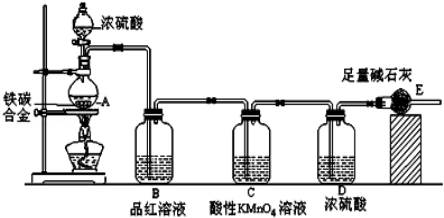
(1)m克铁碳合金中加入过量浓硫酸,未点燃酒精灯前,A、B均无明显现象,其原因是:①常温下碳与浓硫酸不反应;② .
(2)写出加热时A中碳与浓硫酸发生反应的化学方程式: .
(3)B中的现象是: ;C的作用是: .
(4)待A中不再逸出气体时,停止加热,拆下E并称重,E增重bg.则铁碳合金中铁的质量分数为: (写化简后的表达式).
-
某校化学兴趣小组设计了图示实验装置(图中省略了夹持仪器)来测定某铁碳合金中铁的质量分数。
(1)m g铁碳合金中加入过量浓硫酸,未点燃酒精灯前,A、B均无明显现象,其原因是:①常温下碳与浓硫酸不反应;②_____________。
(2)写出加热时A中碳与浓硫酸发生反应的化学方程式____________。
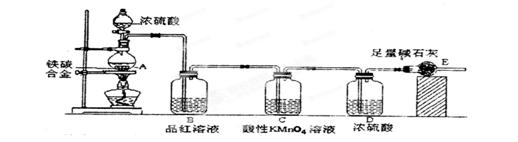
(3)B中的现象是:____________;C的作用是:_______________。
(4)待A中不再逸出气体时,停止加热,拆下E并称重,E增重b g。则铁碳合金中铁的质量分数为_____________。
-
某化学兴趣小组设计了图示实验装置(图中省略了夹持仪器)来测定某铁碳合金中铁的质量分数。
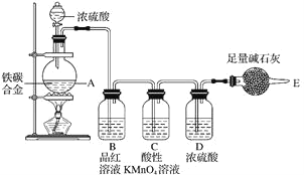
(1)mg铁碳合金中加入过量浓硫酸,未点燃酒精灯前,A、B均无明显现象,其原因是:
①常温下碳与浓硫酸不反应;
②__。
(2)写出加热时A中碳与浓硫酸发生反应的化学方程式__。
(3)B中的现象是__,C的作用是__。
(4)待A中不再逸出气体时,停止加热,拆下E并称重,E增重bg。则铁碳合金中铁的质量分数为__(写表达式)。
(5)甲同学认为利用此装置测得铁的质量分数偏大,请你写出可能的原因:__。
(6)本套装置在设计上存在缺陷,其中导致测得铁的质量分数偏低的是(答一条即可)__。
-
现有铁、碳两种元素组成的合金,某实验小组为了研究该合金的性质并测定该合金中碳的质量分数,设计了如下实验方案和实验装置:
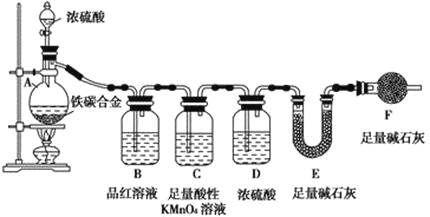
(1)取ag合金粉末放入蒸馏烧瓶,并加入足量浓硫酸,A、B中均无明显现象,原因是________________________________________________。
(2)反应一段时间后,B中的现象为___________________________。
(3)装置C的作用是________________;装置D的作用是___________,F的作用是___________________________________________。
(4)反应结束后,若U形管E增重m g,则合金中碳的质量分数为________。(用含m和a的式子表示)
-
现有某铁碳合金(可看作铁和碳两种单质的混合物),某化学兴趣小组为了测定铁碳合金中碳的质量分数,设计了如图所示的实验装置(夹持仪器已省略)。
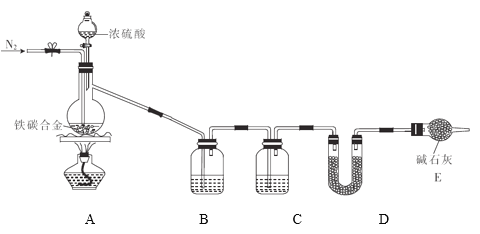
(1)装置A中发生的反应除外 ,还有________________。
,还有________________。
(2)请完成下列表格:
| 装置代号 | B | C | D |
| 所盛试剂 | 酸性 溶液 溶液 | ①________ | ②____________ |
| 装置作用 | ③_____________ | 干燥气体 | ④___________ |
(3)若铁碳合金的质量为5.00g,充分反应后称得D装置增重0.66g,则合金中碳的质量分数为_______,若缺少E装置,则所测碳的质量分数_________(填“偏高”“偏低”或“无影响”)。
-
为测定某生铁(假设仅含Fe和C)粉末状样品中铁的质量分数,某化学研究性学习小组设计有关方案进行如下实验.
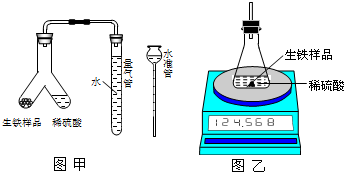
(1)设计如图甲所示装置,生铁和稀硫酸分装在Y型玻璃管中,使生铁样品与稀硫酸反应的操作为______.
实验结束后,读出量气管中的气体体积(换算为标准状况),计算生铁样品中铁的质量分数,测定的结果偏低,可能的原因是______(填字母序号).
A.反应结束并冷却后,未再次调节量气管和水准管中液面相平,即读取气体体积.
B.稀硫酸过量
(2)设计如图乙所示装置,测得反应前后的有关质量如表,则生铁样品中铁的质量分数为______,
根据图中装置判断,若实验中操作没有失误,该实验结果可能______ (填“偏大”、“偏小”或“准
确”).
| 反应前:整套装置+稀硫酸质量/g | 反应前:
生铁样品质量/g | 反应后:整套装置+
锥形瓶中剩余物的质量/g |
| a | m | b |
(3)若取生铁粉末5.72g,在高温下的氧气流中充分反应,得到CO2气体224mL(标准状况).则此生铁粉末中铁和碳的物质的量之比为______.



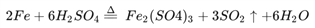 ,写出A中C和浓硫酸发生反应的化学方程式:__________________________,B中的现象是_________________,因此可得到浓硫酸具有_____________性。
,写出A中C和浓硫酸发生反应的化学方程式:__________________________,B中的现象是_________________,因此可得到浓硫酸具有_____________性。







