-
为测定某含有杂质Na2O的Na2O2样品的纯度,3个小组分别设计如下方案。首先准确称量样品m g,然后,按照以下方案进行实验,请你完成相关内容:
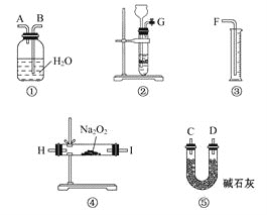
[方案一](1)将样品与水充分反应,使产生的O2通过灼热的铜粉,测得反应后生成氧化铜的质量为n g,通过计算求出试样中Na2O2的含量。Na2O2与水反应的离子方程式是______________;根据所给数据计算出试样中Na2O2含量的代数式为____________。
[方案二]将样品与二氧化碳反应,通过测定反应产生氧气的体积(体积可转化成质量),计算出样品中Na2O2的含量。
(2)上图是完成该实验可能用到的实验装置,根据此实验方案,实验所使用仪器的连接顺序是_______。(填写仪器编号)
(3)装置①⑤的作用分别是:
①___________________;
⑤____________________________。
-
(4分)为测定含有Na2O杂质的Na2O 样品的纯度,甲同学设计以下的方案。
样品的纯度,甲同学设计以下的方案。
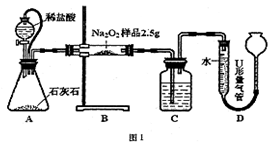
用图所示装置,通过测定Na O2与C0
O2与C0 反应生成0
反应生成0 的体积来测定样品的纯度。
的体积来测定样品的纯度。
(1)C中所盛的药品是____________
(2)A中橡皮管的作用是____________
(3)利用该实验方案所测Na O
O 的纯度明显偏大,其原因可能是__________ (填选项字母)。
的纯度明显偏大,其原因可能是__________ (填选项字母)。
a.装置A、B中的空气对测定结果产生了影响
b.装置C中的空气对测定结果产生了影响
c.读数时U形量气管中的液面左低右高
d.读数时U形量气管中的液面左高右低
(4)该法步骤相对麻烦,请设计一种简便的实验方法完成实验目的,画简图说明即可。
-
现有一定量含有Na2O杂质的Na2O2样品,请设计实验测定该样品的纯度。可供选择的装置如图:
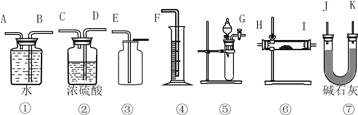
(1)选用上述装置可以组装一套最简单的测定过氧化钠样品纯度的实验装置,选择的仪器组合是____________。
A.①②④⑤ B.①④⑤
C.⑤⑥⑦ D.①③⑤⑦
(2)实验中选用装置的连接顺序是_________________(填各接口的字母,连接胶管省略)。
(3)写出实验中Na2O2发生反应的化学方程式,并用双线桥标注电子转移的方向和数目__________。若开始时测得样品的质量为2.0 g,反应结束后测得气体体积为168mL(标准状况),则Na2O2试样的纯度为_________。
(4)向紫色石蕊试液中加入Na2O2粉末,振荡,正确的叙述是________。
A.最后溶液变蓝 B.溶液先变蓝后褪色
C.溶液仍为紫色 D.因为Na2O2与石蕊发生氧化还原反应而无气泡产生
-
某含有Na2O杂质的Na2O2试样,请设计实验测定该样品的纯度.可供选择的装置:
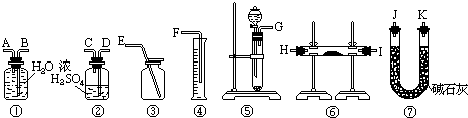
可供选择的药品:CaCO3固体,6mol/L盐酸,蒸馏水
请回答下列问题:
(1)用上述装置可以组装一套最简单的测定过氧化钠样品纯度的实验装置,设计选择的仪器组合是________(填字母).
A.①④⑤B.①②④⑤C.⑤⑥⑦D.①③⑤⑦
(2)实验选择的药品是________,所选用装置的连接顺序应是(填各接口的字母,连接胶管省略)________(填字母)
(3)写出实验中Na2O2和Na2O分别发生反应的离子方程式:
________;________.
(4)用上述实验后所得溶液配制成浓度为1.0mol/L的溶液.
①向400ml该溶液中通入0.3mol CO2,则所得溶液中HCO3-和CO32-的物质的量浓度之比约为________
A.1:3 B.1:2 C.2:1 D.3:1
②将上述溶液蒸发结晶得到Na2CO3和NaHCO3固体混合物,能测定混合物中Na2CO3质量分数的是________.
A.取a克混合物充分加热,在干燥器中冷却至室温,减重b克
B.取a克混合物与足量稀盐酸充分反应,加热、蒸干、灼烧,得b克固体
C.取a克混合物与足量稀硫酸充分反应,逸出气体用碱石灰吸收,增重b克
D.取a克混合物与足量Ba(OH)2溶液充分反应,过滤、洗涤、烘干,得b克固体.
(5)井下采煤个人用的自救器(类似呼吸面具)中盛放的也是过氧化钠,写出体现自救器自救功能的化学反应方程式:________.
-
某化学兴趣小组测定某FeCl3样品(含有少量FeCl2杂质)中铁元素的质量分数,实验时按以下步骤进行:
①称量ag样品,置于烧杯中,
②加入适量的蒸馏水,使样品溶解,然后准确配制成250mL溶液
③准确量取25.00mL步骤②中配得的溶液,置于烧杯中,加入适量的氯水,加热使反应完全
④趁热迅速加入过量氨水,充分搅拌,使沉淀完全
⑤过滤,洗涤沉淀
⑥将沉淀声称到坩埚内加热,搅拌直到固体全部由红褐色变为红棕色后在干燥器中冷却到室温后,称量
⑦…根据上面叙述,回答
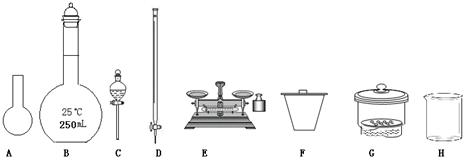
(1)如图所示仪器中,本实验步骤①②中必须用到的仪器是______.
(2)写出步骤③和④中发生反应的离子方程式______
(3)洗涤是洗去附着在沉淀上的______(写离子符号).洗涤沉淀的操作是______检验沉淀已洗净的方法是______
(4)若坩埚质量是W1,坩埚与加热后固体总质量是W2,则样品中铁元素的质量分数为______(列出算式,不需化简)
(5)该兴趣小组中甲学生认为:实验步骤中不加氯水,其余步骤不变,仍可达到实验目的,你认为甲学的观点是否正确______(填“正确”或“错误”)请说明理由(必要时可用化学方程式表示)______.
-
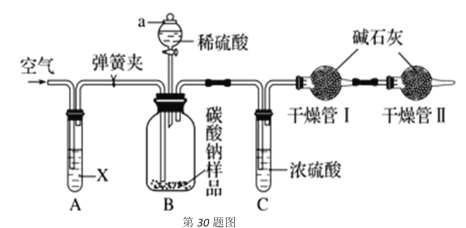
某化学兴趣小组研究混有少量氯化钠杂质的纯碱样品,设计如下装置来测定该纯碱样品的纯度。实验步骤如下:
①组装好仪器并检查气密性;
②用托盘天平称量干燥管Ⅰ的质量为m1;
③称量纯碱样品的质量为n,装入广口瓶B内;
④打开分液漏斗a的旋塞,缓缓滴入稀硫酸,至不再产生气泡为止;
⑤往试管A缓缓鼓入空气数分钟,然后称量干燥管Ⅰ的质量为m2。
请回答:
(1)试剂X是__________,写出广口瓶B中反应的化学方程式__________。
(2)干燥管Ⅱ的作用是__________。
(3)步骤④若滴入稀硫酸过快,会导致测定结果__________(填“偏大”、“偏小”或者“不变”);理由是__________。
(4)根据此实验,计算纯碱样品纯度的为__________(用含m1、m2、n的代数式表示)。
-
某纯碱样品中含有少量氯化钠杂质,现用下图所示装置来测定该纯碱样品的纯度。实验步骤如下:
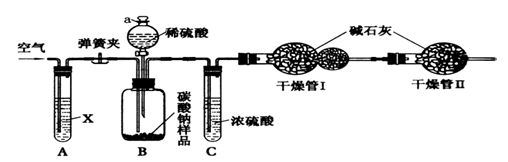
①按图将仪器组装好并检查气密性;②准确称量盛有碱石灰(固体氢氧化钠和生石灰的混合物)的干燥管Ⅰ的质量(设为m1);③准确称量纯碱样品的质量(设为n),放入广口瓶B内;④打开分液漏斗a的旋塞,缓缓滴入稀硫酸,至不再产生气泡为止;⑤往试管A缓缓鼓入空气数分钟,然后称量干燥管Ⅰ的质量(设为m2)。试回答:
(1)实验操作④、⑤都要缓缓鼓地进行,其理由是_____________,如果这两步操作太快,会导致测定结果________(填偏大、偏小或不变)。
(2)鼓入空气的目的是______________;装置A中的试剂X应选用________________,其作用是__________________,
(3)装置C的作用是___________________;干燥管Ⅱ的作用是__________________。
(4)装置A与B之间的弹簧夹在第_________项操作前必须打开,在第_________项操作用其以前必须夹紧。
(5)根据此实验,写出计算纯碱样品纯度的公式:___________________。
-
为测定碳酸钠纯度(只含有少量氯化钠),学生设计了如下两个实验方案。
[方案1]称取 样品,置于小烧杯中,加适量水完全溶解;向小烧杯中加入足量氢氧化钡溶液,过滤,洗涤、干燥沉淀,称量沉淀的质量为19.700克,计算。
样品,置于小烧杯中,加适量水完全溶解;向小烧杯中加入足量氢氧化钡溶液,过滤,洗涤、干燥沉淀,称量沉淀的质量为19.700克,计算。
(1)写出生成沉淀的反应方程式__________________。
(2)过滤操作需要的玻璃仪器__________________。
(3)计算碳酸钠的质量分数为______________(保留两位小数)。
[方案2]用下图装置,排液法测定 的体积,并根据样品质量和
的体积,并根据样品质量和 的体积计算
的体积计算
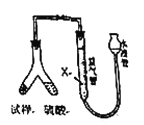
(4)为了减小测定 的体积误差,量气管中加入的液体
的体积误差,量气管中加入的液体 为______(填化学式)。
为______(填化学式)。
(5)通过实验,测得该试样中碳酸钠的质量分数偏高,产生这种现象的原因可能是______。
A.测定气体体积时未冷却至室温
B.气体进入量气管前未用浓硫酸干燥
C. 型管中留有反应生成的气体
型管中留有反应生成的气体
D.反应结束后读数时水准管的水面高于量气管的水面
-
现有一定量含有Na2O杂质的Na2O2试样,用下图所示的实验装置测定Na2O2试样的纯度(通过CO2与样品反应后生成O2的量测定Na2O2的含量)。(可供选用的反应物:CaCO3固体、6 mol·L-1盐酸、6 mol·L-1硫酸和蒸馏水)
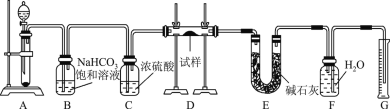
回答下列问题:
(1)实验前必须先_________。
(2)装置A中液体试剂应选用_____。
(3)装置B的作用是_________;装置C的作用是____;装置E中碱石灰的作用是__________。
(4)装置D中发生反应的化学方程式是___________。
(5)若开始时测得样品的质量为2.0 g,反应结束后测得气体体积为224 mL(标准状况),则Na2O2试样的纯度为________。
-
某纯碱样品含有少量 杂质,某兴趣小组用如图所示装置测定纯碱样品中
杂质,某兴趣小组用如图所示装置测定纯碱样品中 的质量分数(铁架台、铁夹等均已略去)。
的质量分数(铁架台、铁夹等均已略去)。
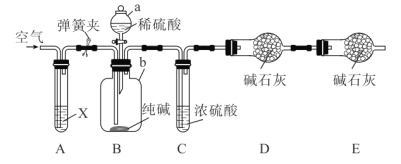
实验步骤如下:
Ⅰ.按图连接装置,并检查气密性;
Ⅱ.准确称量盛有碱石灰的干燥管 的质量为
的质量为 ;
;
Ⅲ.准确称量 纯碱样品放入容器
纯碱样品放入容器 中;
中;
Ⅳ.打开分液漏斗 的旋塞,缓缓滴入稀硫酸,至不再产生气泡为止;
的旋塞,缓缓滴入稀硫酸,至不再产生气泡为止;
Ⅴ.打开弹簧夹,往试管 中缓缓鼓入空气数分钟,最后称得干燥管
中缓缓鼓入空气数分钟,最后称得干燥管 的质量为
的质量为 。
。
请回答下列问题:
(1)检查装置 气密性的方法为____________。
气密性的方法为____________。
(2)装置 中试剂
中试剂 应选择_____,目的是________。
应选择_____,目的是________。
(3)装置 的作用是____,步骤
的作用是____,步骤 中“缓缓鼓入空气数分钟”的目的是____________。
中“缓缓鼓入空气数分钟”的目的是____________。
(4)根据实验中测得的有关数据,计算纯碱样品 的质量分数为___(保留三位有效数字),若没有装置
的质量分数为___(保留三位有效数字),若没有装置 ,会导致测量结果____(填“偏大”“偏小”或“无影响”)。
,会导致测量结果____(填“偏大”“偏小”或“无影响”)。









