-
(16分)(2012•山东)偏二甲肼与N2O4是常用的火箭推进剂,二者发生如下化学反应:
(CH3)2NNH2(l)+2N2O4(l)═2CO2(g)+3N2(g)+4H2O(g) (Ⅰ)
(1)反应(Ⅰ)中氧化剂是 .
(2)火箭残骸中常现红棕色气体,原因为:N2O4(g)⇌2NO2(g) (Ⅱ)
当温度升高时,气体颜色变深,则反应(Ⅱ)为 (填“吸热”或“放热”)反应.
(3)一定温度下,反应(Ⅱ)的焓变为△H.现将1mol N2O4充入一恒压密闭容器中,下列示意图正确且能说明反应达到平衡状态的是 .若在相同温度下,上述反应改在体积为1L的恒容密闭容器中进行,平衡常数 (填“增大”“不变”或“减小”),反应3s后NO2的物质的量为0.6mol,则0~3s内的平均反应速率v(N2O4)= mol/(L•s)﹣1.
(4)NO2可用氨水吸收生成NH4NO3.25℃时,将a mol NH4NO3溶于水,溶液显酸性,原因是 (用离子方程式表示).向该溶液滴加b L 氨水后溶液呈中性,则滴加氨水的过程中水的电离平衡将 (填“正向”“不”或“逆向”)移动,所滴加氨水的浓度为 mol•L﹣1.(NH3•H2O的电离平衡常数取Kb=2×10﹣5 mol•L﹣1)

高三化学填空题中等难度题查看答案及解析
-
(10分)偏二甲肼与N2O4是常用的火箭推进剂,二者发生如下化学反应:
(CH3)2NNH2(l)+2N2O4(l)
2CO2(g)+3N2(g)+4H2O(g) (Ⅰ)
(1)反应(Ⅰ)中氧化剂是 。
(2)火箭残骸中常现红棕色气体,原因为:N2O4(g)
2NO2(g) (Ⅱ)当温度升高时,气体颜色变深,则反应(Ⅱ)为 (填“吸热”或“放热”)反应。
(3)一定温度下,反应(Ⅱ)的焓变为ΔH。现将1 mol N2O4充入一恒压密闭容器中,下列示意图正确且能说明反应达到平衡状态的是 。
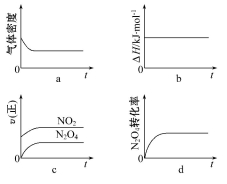
若在相同温度下,上述反应改在体积为1 L的恒容密闭容器中进行,平衡常数 (填“增大”、“不变”或“减小”),反应3 s后NO2的物质的量为0.6 mol,则0 s~3 s内的平均反应速率v(N2O4)= mol·L-1·s-1。
高三化学填空题中等难度题查看答案及解析
-
偏二甲肼与N2O4是常用的火箭推进剂,二者发生如下化学反应:
(CH3)2NNH2(l)+2N2O4(l)═2CO2(g)+3N2(g)+4H2O(g) (Ⅰ)
(1)反应(Ⅰ)中氧化剂是________.
(2)火箭残骸中常现红棕色气体,原因为:N2O4(g)⇌2NO2(g) (Ⅱ)
当温度升高时,气体颜色变深,则反应(Ⅱ)为________(填“吸热”或“放热”)反应.
(3)一定温度下,反应(Ⅱ)的焓变为△H.现将1mol N2O4充入一恒压密闭容器中,下列示意图正确且能说明反应达到平衡状态的是________.若在相同温度下,上述反应改在体积为1L的恒容密闭容器中进行,平衡常数________(填“增大”“不变”或“减小”),反应3s后NO2的物质的量为0.6mol,则0~3s内的平均反应速率v(N2O4)=________ mol/-1.
(4)NO2可用氨水吸收生成NH4NO3.25℃时,将a mol NH4NO3溶于水,溶液显酸性,原因是________(用离子方程式表示).向该溶液滴加b L 氨水后溶液呈中性,则滴加氨水的过程中水的电离平衡将________(填“正向”“不”或“逆向”)移动,所滴加氨水的浓度为________mol•L-1.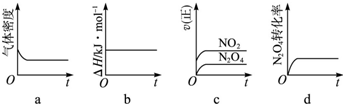
高三化学填空题中等难度题查看答案及解析
-
偏二甲肼与N2O4是常用的火箭推进剂,二者发生如下反应:
(CH3)2NNH2(l)+2N2O4(l)═2CO2(g)+3N2(g)+4H2O(g) (I)
(1)反应(I)中氧化剂是__________。
(2)火箭残骸中常现红棕色气体,原因为:N2O4(g)
2NO2 (g)(II)当温度升高时,气体颜色变深,则反应(II)为________(填“吸热”或“放热”)反应。
(3)一定温度下,反应(Ⅱ)的焓变为△H.现将1molN2O4充入一恒压密闭容器中,下列示意图正确且能说明反应达到平衡状态的是_______;

若在相同温度下,上述反应改在体积为1L的恒容密闭容器中进行,平衡常数______(填“增大”“不变”或“减小”),反应3s后NO2的物质的量为0.6mol,则0~3s内的平均反应速率v(N2O4)= ______mol•L-1•s-1。
高三化学填空题困难题查看答案及解析
-
(14分)偏二甲肼与N2O4 是常用的火箭推进剂,二者发生如下化学反应:
(CH3)2NNH2 ( L )+2N2O4 (L )=2CO2 (g)+3N2(g)+4H2O(g) (Ⅰ)
(1)该反应(Ⅰ)中还原剂是__________。
(2)火箭残骸中常现红棕色气体,原因为:N2O4 (g)
2NO2 (g) (Ⅱ)
一定温度下,反应(Ⅱ)的焓变为ΔH。现将2 mol NO2 充入一恒压密闭容器中,下列示意图正确且能说明反应达到平衡状态的是________.
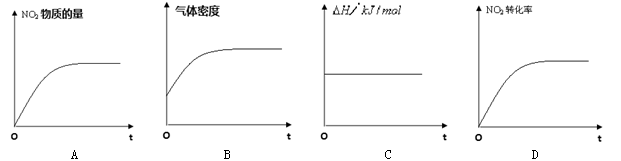
若在相同温度下,上述反应改在体积为3L的恒容密闭容器中进行,平衡常数________(填“增大”“不变”或“减小”),反应4s后N2O4的物质的量为0.9mol,则0~4s内的平均反应速率v(NO2)=_________________。
(3)25℃时,将1mol NH4NO3溶于水,溶液显酸性,原因是_____(用离子方程式表示)。向该溶液滴加50mL氨水后溶液呈中性,则滴加氨水的过程中的水的电离平衡将_______(填“正向”“不”或“逆向”)移动,所滴加氨水的浓度为____mol·L-1。(NH3·H2O的电离平衡常数K=2×10-5 mol·L-1)
高三化学填空题困难题查看答案及解析
-
偏二甲肼与N2O4是常用的火箭推进剂,二者发生如下化学反应:
(Ⅰ)(CH3)2NNH2(l)+2N2O4(l)=2CO2(g)+3N2(g)+4H2O(g)
(Ⅱ)N2O4(g)⇌2NO2(g)
(1)反应(Ⅰ)中氧化剂是___。
(2)当温度升高时,气体颜色变深,则反应(Ⅱ)为___(填“吸热”或“放热”)反应。
(3)若在相同温度下,上述反应改在体积为1L的恒容密闭容器中进行,平衡常数___(填“增大”“不变”或“减小”),反应3s后NO2的物质的量为0.6mol,则0~3s内的平均反应速率v(N2O4)=_______mol⋅L-1⋅s-1。
(4)NO2可用氨水吸收生成NH4NO3。25℃时,将amolNH4NO3溶于水,溶液显酸性,原因是___(用离子方程式表示)。
(5)向该溶液滴加bL氨水后溶液呈中性,则滴加氨水的过程中水的电离平衡将___(填“正向”“不”或“逆向”)移动,所滴加氨水的浓度为___mol·L-1。(NH3·H2O的电离平衡常数取Kb=2×10-5mol·L-1。
高三化学综合题中等难度题查看答案及解析
-
偏二甲肼[(CH3)2N-NH2](N为-2价)与N2O4是常用的火箭推进剂,发生的化学反应如下:(CH3)2N-NH2(l)+2N2O4(l)═2CO2(g)+3N2(g)+4H2O(g)△H<0,下列说法不正确的是( )
A.该反应在任何情况下都能自发进行
B.1mol(CH3)2N-NH2含有11mol共价键
C.反应中,氧化产物为CO2,还原产物为N2
D.反应中,生成1molCO2时,转移8mole-
高三化学单选题中等难度题查看答案及解析
-
运载“神舟八号”飞船的火箭燃料是偏二甲肼[(CH3)2NNH2],燃料和N2O4反应放出巨大的能量,产生大量无毒气体,把飞船送入太空。下列描述不正确的是( )
A.在偏二甲肼与四氧化二氮的反应中,N2O4是氧化剂
B.两物质反应时,生成的无毒气体为CO2、N2、和H2O
C.偏二甲肼中N元素的化合价均为-2价
D.偏二甲肼的同分异构体中,含碳碳单键的化合物只有2种
高三化学选择题简单题查看答案及解析
-
运载火箭常用偏二甲肼(C2H8N2)(其中N的化合价为-3)作燃料和四氧化二氮(N2O4)反应。在火箭升空过程中,燃料发生反应:C2H8N2+2N2O4
2CO2+3N2+4H2O提供能量。下列有关叙述正确的是
A. 该燃料绿色环保,在燃烧过程中不会造成任何环境污染
B. 该反应中N2O4是氧化剂,偏二甲肼是还原剂
C. N2既是氧化产物又是还原产物,CO2既不是氧化产物也不是还原产物
D. 每有0.6 mol N2生成,转移电子数目为2.4NA
高三化学单选题中等难度题查看答案及解析
-
“神舟十号”的运载火箭所用燃料是偏二甲肼(C2H8N2 )( 其中N 的化合价为-3 )和四氧化二氮(N2O4)。在火箭升空过程中,燃料发生反应: C2H8N2 +2N2O4→2CO2+3N2+4H2O 提供能量。下列有关叙述正确的是
A.该燃料无毒,在燃烧过程中不会造成任何环境污染
B.每有0.6molN2生成,转移电子数目为2.4NA
C.该反应中N2O4是氧化剂,偏二甲肼是还原剂
D.N2既是氧化产物又是还原产物,CO2既不是氧化产物也不是还原产物
高三化学单选题困难题查看答案及解析