工业上燃烧硫矿石制取硫酸产生的废气SO2,用电化学原理将SO2转化为重要的化工原料,如图,下列说法正确的是( )

A.电池工作时,消耗O2、SO2物质的量之比为2∶1
B.电子从a极经导线移向b极,再经溶液移向a极
C.电池工作一段时间后电解质溶液的pH增大
D.a为负极,电极反应式为SO2+2H2O-2e-= SO42-+4H+
高二化学单选题中等难度题
工业上燃烧硫矿石制取硫酸产生的废气SO2,用电化学原理将SO2转化为重要的化工原料,如图,下列说法正确的是( )

A.电池工作时,消耗O2、SO2物质的量之比为2∶1
B.电子从a极经导线移向b极,再经溶液移向a极
C.电池工作一段时间后电解质溶液的pH增大
D.a为负极,电极反应式为SO2+2H2O-2e-= SO42-+4H+
高二化学单选题中等难度题
工业上燃烧硫矿石制取硫酸产生的废气SO2,用电化学原理将SO2转化为重要的化工原料,如图,下列说法正确的是( )

A.电池工作时,消耗O2、SO2物质的量之比为2∶1
B.电子从a极经导线移向b极,再经溶液移向a极
C.电池工作一段时间后电解质溶液的pH增大
D.a为负极,电极反应式为SO2+2H2O-2e-= SO42-+4H+
高二化学单选题中等难度题查看答案及解析
工业上燃烧硫矿石制取硫酸产生的废气SO2,用电化学原理将SO2转化为重要的化工原料,如图,下列说法正确的是( )
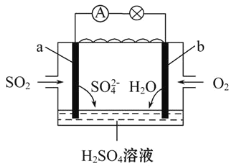
A.电池工作时,消耗O2、SO2物质的量之比为2∶1
B.电子从a极经导线移向b极,再经溶液移向a极
C.电池工作一段时间后电解质溶液的pH增大
D.a为负极,电极反应式为SO2+2H2O-2e-= SO42-+4H+
高二化学单选题中等难度题查看答案及解析
工业生产中产生的废气、废液、废渣直接排放会造成污染,很多都经过吸收转化为化工产品。
I.利用电化学原理吸收工业生产中产生的SO2、NO,同时获得Na2S2O4和NH4NO3产品的工艺流程图如图(Ce为铈元素)。

请回答下列问题:
(1)装置Ⅱ中NO在酸性条件下生成NO2-的离子方程式: 。
(2)装置Ⅲ的作用之一是再生Ce4+,其原理如下图所示:
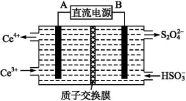
右侧反应室中发生的主要电极反应式为 。
(3)已知进入装置Ⅳ的溶液中NO2-的浓度为0.4 mol·L-1,要使1 m3该溶液中的NO2-完全转化为 NH4NO3,需至少向装置Ⅳ中通入标准状况下的O2的体积为 L。
II.以电石渣[主要成分为Ca(OH)2和CaCO3]为原料制备KClO3的流程如下:

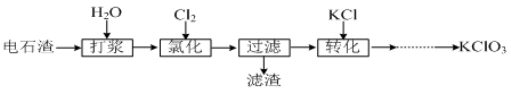
(4)氯化过程控制电石渣过量,在75℃左右进行。氯化时存在Cl2与Ca(OH)2作用生成Ca(ClO)2的反应,Ca(ClO)2进一步转化为Ca(ClO3)2,少量Ca(ClO)2 分解为CaCl2和O2。提高Cl2转化为Ca(ClO3)2的转化率的可行措施有 (填序号)。
A.适当减缓通入Cl2速率 B.充分搅拌浆料 C.加水使Ca(OH)2完全溶解
(5)氯化过程中Cl2 转化为Ca(ClO3)2的总反应方程式为
6Ca(OH)2+6Cl2===Ca(ClO3)2+5CaCl2+6H2O
氯化完成后过滤。滤渣的主要成分为 (填化学式)。
(6)向滤液中加入稍过量KCl固体可将Ca(ClO3)2转化为KClO3,若溶液中KClO3的含量为100g▪L−1,从该溶液中尽可能多地析出KClO3固体的方法是 。

(7)工业上常用磷精矿[Ca5(PO4)3F]和硫酸反应制备磷酸。已知25℃,101kPa时:
CaO(s)+H2SO4(l)=CaSO4(s)+H2O(l) △H=-271kJ/mol
5CaO(s)+H3PO4(l)+HF(g)=Ca5(PO4)3F(s)+5H2O(l) △H=-937kJ/mol
则Ca5(PO4)3F和硫酸反应生成磷酸的热化学方程式是 。
高二化学填空题极难题查看答案及解析
硫酸是重要的化工原料,工业制取硫酸最重要的一步反应为:2SO2(g)+O2(g) 2SO3(g) △H< 0
(1)为提高SO2的转化率,可通入过量O2,用平衡移动原理解释其原因:___________。
(2)某兴趣小组在实验室对该反应进行研究,部分实验数据和图像如下。
反应条件:催化剂、一定温度、容积10 L
| 实验 | 起始物质的量/mol | 平衡时SO3 物质的量/mol | ||
| SO2 | O2 | SO3 | ||
| ⅰ | 0.2 | 0.1 | 0 | 0.12 |
| ⅱ | 0 | 0 | 0.2 | a |
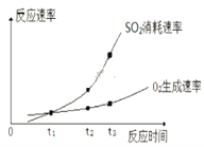
①实验ⅰ中SO2的转化率为______。
②a____0.12(填“>”、“=”或“<”)。
③t1、t2、t3中,达到化学平衡状态的是________。
④ t2到t3的变化是因为改变了一个反应条件,该条件可能是___________。
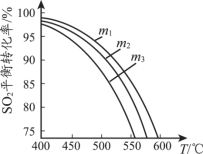
(3)将SO2和O2充入恒压密闭容器中,原料气中SO2 和O2的物质的量之比m(m=n(SO2)/n(O2))不同时,SO2的平衡转化率与温度(T)的关系如下图所示,则m1、m2、m3的大小顺序为_____。
高二化学综合题中等难度题查看答案及解析
高二化学解答题中等难度题查看答案及解析
黄铁矿(主要成分为FeS2)是工业制取硫酸的重要原料,其燃烧产物为SO2和Fe2O3。
(1)已知1g FeS2完全燃烧放出7.1kJ热量,则表示FeS2完全燃烧反应的热化学方程式为:
______________________________________________________________。
(2)将0.050molSO2(g)和0.030molO2(g)放入容积为1L的密闭容器中,反应:2SO2(g)+O2(g)2SO3(g) 在一定条件下达到平衡,测得c(SO3)=0.040mol/L。则该条件下反应的平衡常数K的数值为___________,SO2的平衡转化率为__________。
(3)当该反应处于平衡状态时,欲使平衡向正反应方向移动且反应速率加快,下列措施可行的是________。(填字母)
A.向平衡混合物中充入Ar B.向平衡混合物中充入O2
C.改变反应的催化剂 D.降低反应的温度
(4)反应:2SO2(g)+O2(g)2SO3(g) △H<0 , SO2的转化率在起始温度T1=673K下随反应时间(t)的变化如下图,其他条件不变,仅改变起始温度为T2=723K,请在图中画出温度T2下SO2的转化率随反应时间变化的预期结果示意图。
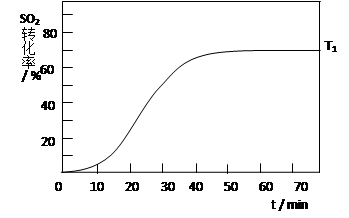
高二化学填空题极难题查看答案及解析
二氧化硫的催化氧化反应:2SO2(g)+O2(g)2SO3(g)是工业制硫酸的重要反应之一。下列说法错误的是
A. 煅烧硫铁矿(主要成分FeS2)可获得SO2,将矿石粉碎成细小颗粒可以提高反应的转化率
B. 已知该催化氧化反应K(300℃)>K(350℃),则该反应正向是放热反应
C. 该反应加入催化剂是为了加快反应速率
D. 保持温度不变,平衡后增大O2的浓度,该反应的平衡常数K不变
高二化学单选题中等难度题查看答案及解析
下图是将SO2转化为重要的化工原料H2SO4的原理示意图,下列说法不正确的是( )
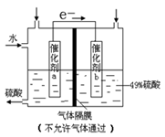
A.该装置将化学能转化为电能
B.催化剂b表面O2发生还原反应,其附近酸性增强
C.催化剂a表面的反应是:SO2+2H2O-2e-=SO42-+4H+
D.若得到的硫酸浓度仍为49%,则理论上参加反应的SO2与加入的H2O的质量比为8:15
高二化学选择题困难题查看答案及解析
下图是将SO2转化为重要的化工原料H2SO4的原理示意图,下列说法不正确的是
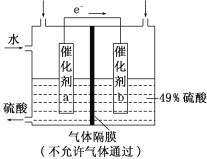
A. 该装置将化学能转化为电能
B. 催化剂b表面O2发生还原反应,其附近酸性增强
C. 催化剂a表面的反应是:SO2+2H2O-2e-===SO42-+4H+
D. 若得到的硫酸浓度仍为49%,则理论上参加反应的SO2与加入的H2O的质量比为8∶15
高二化学单选题困难题查看答案及解析
下图是将SO2转化为重要的化工原料H2SO4的原理示意图,下列说法不正确的是
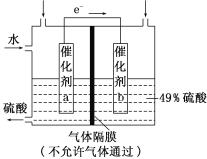
A. 该装置将化学能转化为电能
B. 催化剂b表面O2发生还原反应,其附近酸性增强
C. 催化剂a表面的反应是:SO2+2H2O-2e-===SO42-+4H+
D. 若得到的硫酸浓度仍为49%,则理论上参加反应的SO2与加入的H2O的质量比为8∶15
高二化学单选题困难题查看答案及解析