-
氯气及其化合物在生产和生活中有重要应用,下列关于氯及其化合物的说法正确的是( )
A. NaClO是“84消毒液”的有效成分,其水溶液能使有色布条褪色,反应中NaClO表现还原性
B. Cl2与烧碱溶液反应的实质是Cl2+OH-=Cl-+ClO-+H2O
C. 氯气有毒,在通风橱中制备氯气可以消除氯气的污染
D. 将Cl2通入淀粉-KI溶液,溶液变蓝色
高一化学单选题中等难度题查看答案及解析
-
氯气及其化合物在生产和生活中有重要应用,下列关于氯及其化合物的说法正确的是( )
A.NaClO是“84消毒液”的有效成分,其水溶液能使有色布条褪色,反应中NaClO表现还原性
B.Cl2与烧碱溶液反应的实质是Cl2+OH-=Cl-+ClO-+H2O
C.氯气有毒,在通风橱中制备氯气可以消除氯气的污染
D.将Cl2通入淀粉-KI溶液,溶液变蓝色
高一化学单选题中等难度题查看答案及解析
-
氯气及其化合物在生产和生活中有重要应用,下列关于氯及其化合物的说法正确的是( )
A.NaClO是“84消毒液”的有效成分,其水溶液能使有色布条褪色,反应中NaClO表现还原性
B.Cl2与烧碱溶液反应的实质是Cl2 + OH-=Cl- +ClO- + H2O
C.氯气有毒,在通风橱中制备氯气可以消除氯气的污染
D.将Cl2通入淀粉—KI溶液,溶液变蓝色
高一化学选择题中等难度题查看答案及解析
-
氯气及其化合物在工农业生产和人类生活中都有着重要的应用。
(1)NaClO有较强的氧化性,所以是常用的消毒剂和漂白剂,请写出工业上用氯气和NaOH溶液生产消毒剂NaClO的离子方程式_________________________。
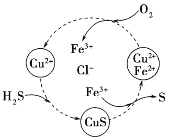
(2)将H2S和空气的混合气体通入FeCl3、FeCl2、CuCl2的混合溶液中反应可以回收S,其物质转化如图所示。该图示的总反应为_________________________。
(3)自来水中的NO3-对人类健康产生危害。为了降低自来水中NO3-的浓度,某研究人员提出在碱性条件下用Al粉还原NO3-,产物是N2。发生的反应可表示如下,请完成方程式的配平。
___Al+___NO3-+___ =___AlO2-+___N2↑+___H2O
高一化学填空题中等难度题查看答案及解析
-
化学与日常生活密切相关,下列有关物质应用的说法正确的是( )
A、玻璃容器可长期盛放各种酸 B、浓氨水可检验氯气管道泄漏
C、浓硫酸可刻蚀石英制艺术品 D、84消毒液的有效成分是NaClO
高一化学选择题简单题查看答案及解析
-
氯气是一种重要的化工原料,氯气及其化合物在自来水的消毒、农药的生产、药物的合成都有着重要的应用。
(1)NaClO中Cl的化合价为____,有较强的___(填氧化、还原)性。
(2)黄色气体ClO2可用于污水杀菌和饮用水净化。
①KClO3与SO2在强酸性溶液中反应可制得ClO2 ,SO2被氧化为SO42-,此反应的离子方程式为____。
②ClO2可将废水中的Mn2+转化为MnO2而除去,本身还原为Cl-,该反应过程中氧化剂与还原剂的物质的量之比为____。
高一化学综合题中等难度题查看答案及解析
-
NaClO2是一种重要的杀菌消毒剂,也常用来漂白织物等,其一种生产工艺如图:
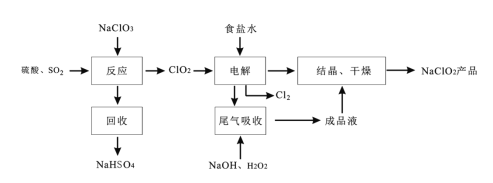
回答下列问题:
(1)NaClO2中Cl的化合价为___;电解产生的Cl2是___色,实验室制备氯气的化学方程式为:____。
(2)写出“反应”步骤中生成ClO2的化学方程式:___。
(3)“电解”所用食盐水由粗盐水精制而成,精制时,为除去Mg2+和Ca2+,要加入的试剂分别为___、___。
高一化学工业流程中等难度题查看答案及解析
-
氯及其化合物在日常生活中有广泛应用。漂白液通常用于家庭和公共场所的消毒,某品牌漂白液的包装说明如下:

(1)该漂白液中,NaClO的物质的量浓度约为___ mol·L-1。
(2)使用NaOH溶液和氯气来制取消毒液,写出该反应的离子方程式___,制取500mL此漂白液,需要5.0mol·L-1的NaOH溶液___mL。
(3)漂白液易吸收空气中的CO2而生成NaHCO3,写出有关的化学方程式___。
高一化学综合题中等难度题查看答案及解析
-
氯气是一种重要的化工原料,在工农业生产生活中有着重要的应用。某化学兴趣小组同学利用以下装置制备氯气并对氯气的性质进行探究:
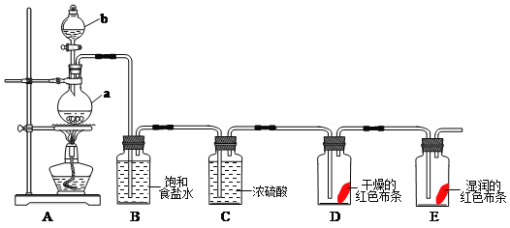
(1)有关氯气、氯水和氯离子的性质,下列说法正确的是_____________
A.氯水的颜色呈浅黄绿色,说明氯水中含有Cl2
B.Cl-和Cl2都具有很强的氧化性
C.新制氯水可以用来杀菌消毒是因为生成强酸 次氯酸
D.将新制氯水滴入AgNO3溶液,会出现白色沉淀
(2)仪器a的名称为___________,装置B中饱和食盐水的作用是_______________。
(3)装置A中发生反应的离子方程式为:____________________________________。
(4)装置D中的实验现象为__________________,装置E中的实验现象为________
(5)整套实验装置存在着明显缺陷,你的改进措施是__________________________。
(6)8.7gMnO2固体与足量浓盐酸充分反应,在标准状况下产生Cl2的体积为_____L;其中被氧化的HCl的物质的量为_______mol。
高一化学实验题简单题查看答案及解析
-
氯气是一种重要的化工原料,氯气及其化合物在自来水的消毒、农药的生产、药物的合成都有着重要的应用。
I.(1)Cl2是一种有毒气体,如果泄漏会造成严重的环境污染。化工厂可用浓氨水来检验Cl2是否泄漏,有关反应的化学方程式为:3Cl2(气)+ 8NH3(气)=6NH4Cl(固)+N2(气)若反应中消耗Cl21.5mol,则被氧化的NH3在标准状况下的体积为__________L,该过程中电子转移的总数为__________________ 个。
(2)黄绿色气体ClO2(其中氯元素价态为+4)可用于污水杀菌和饮用水净化。ClO2可将废水中的Mn2+转化为MnO2而除去,本身还原为Cl-,该反应过程中还原剂与氧化剂的物质的量之比为________。
II.实验室可用如下装置制备氯气并验证氯气的性质置(其中夹持装置已省略)。

已知:装置A是氯气的发生装置,反应的化学方程式为Ca(ClO)2 + 4HCl(浓)═ CaCl2+2Cl2↑+2H2O据此回答下列问题:
(1)装置B中饱和食盐水的作用是_______。
(2)装置C的作用是验证氯气是否具有漂白性,则装置C中Ⅰ、Ⅱ、Ⅲ处依次应放入的物质是:湿润的有色布条、无水氯化钙、干燥的有色布条,请你推测Ⅲ处的现象为:__________。
(3)装置D的作用是___________,则烧杯中的溶液是__________,写出所发生反应的化学方程式_____________________________ 。
高一化学实验题中等难度题查看答案及解析