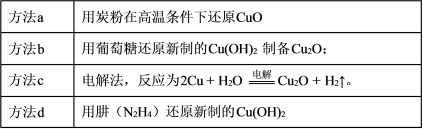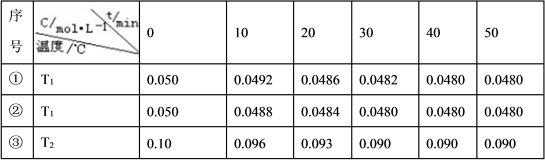-
纳米级 Cu2O 作为一种优良的催化剂而备受关注。
(1)纳米级Cu2O 可以作为催化剂水分解生成氢气。在相同体积的恒容密闭容器中,用两种等质量颗粒大小不同的 Cu2O 进行催化分解水的实验: 2H2O(g) 2H2(g)+O2(g) △H=+484 kJ/mol。水蒸气的浓度( mol/L)随时间变化如下表所示:
2H2(g)+O2(g) △H=+484 kJ/mol。水蒸气的浓度( mol/L)随时间变化如下表所示:
| 序号 | 温度 | 0 | 10 | 20 | 30 | 40 | 50 |
| Ⅰ | T1 | 0.050 | 0.0492 | 0.0486 | 0.0480 | 0.0480 | 0.0480 |
| Ⅱ | T2 | 0.050 | 0.0488 | 0.0484 | 0.0480 | 0.0480 | 0.0480 |
| Ⅲ | T3 | 0.100 | 0.0960 | 0.0930 | 0.0900 | 0.0900 | 0.0900 |
①催化剂的催化效率: 实验Ⅰ______(填“大于”、 “小于”或“等于”)实验Ⅱ。
②实验Ⅲ中 0~10min 内 v(O2)=_____________。
③实验Ⅰ、Ⅱ、Ⅲ的平衡常数分别为 K1、 K2、 K3, 其大小排序为_______。
(2)纳米级 Cu2O 作催化剂还可以实现CH3OH(甲醇)脱氢制取HCHO(甲醛):CH3OH(g) HCHO(g) + H2(g),CH3OH的平衡转化率随温度变化曲线如图:
HCHO(g) + H2(g),CH3OH的平衡转化率随温度变化曲线如图:
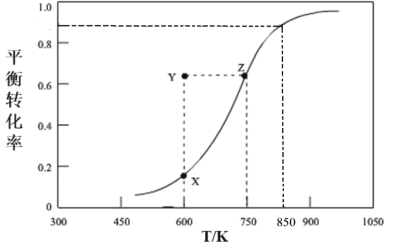
① 600K 时, Y 点甲醇的 v(正)________ v(逆) (填“大于”、“小于”或“等于”)。
②据图回答:工业上利用此反应进行生产时,不能在850K以上生产的理由是_______。
-
铜及其化合物在工农业生产及日常生活中应用非常广泛。回答下列问题:
(1)纳米级Cu2O由于具有优良的催化性能而受到关注,制取Cu2O的两种方法如下表所示。
| 方法I | 用炭粉在高温条件下还原CuO生成Cu2O和CO2 |
| 方法II | 用肼(N2H4)还原新制Cu(OH)2 |
① 方法I中还原剂与氧化剂的物质的量之比为________。
② 方法II发生反应的化学方程式为______________。
(2)氢化亚铜是一种红色同体,可由下列反应制备:
4CuSO4+3H3PO2+6H2O=4CuH↓+4H2SO4+3H3PO4
该反应中每转移3 mol电子,生成CuH的物质的量为___________mol。
(3)氯化铜溶液中各种含铜微粒的分布分数(平衡时某微粒的浓度占各微粒浓度之和的分数)与c(C1-)之间的关系如图所示。
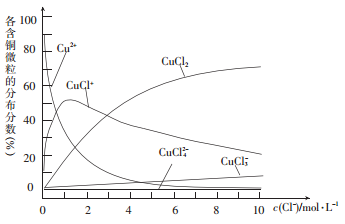
① 当c(C1-)= 9 mol/L时,溶液中3种主要含铜微粒浓度的大小关系为__________。
② 在c(C1-)= l mol /L的氯化铜溶液中,加人AgNO3溶液,CuCl+转化为Cu2+的离子方程式为____________。
(4)已知:Cu(OH)2是二元弱碱,25℃时Ksp[Cu(OH)2]=2.0×10-20。则此温度下在铜盐溶液中Cu2+发生水解反应的平衡常数为______________。
-
氢气是一种清洁能源,氢气的制取是氢能源利用领域的研究热点;氢气也是重要的化工原料。
(1)纳米级的Cu2O可作为太阳光分解水的催化剂.一定温度下,在2L密闭容器中加入纳米级Cu2O并通入0.10mol水蒸气发生反应:
2H2O(g) 2H2(g)+O2(g)△H=+484kJ•mol﹣1,不同时段产生O2的量见下表:
2H2(g)+O2(g)△H=+484kJ•mol﹣1,不同时段产生O2的量见下表:
| 时间/min | 20 | 40 | 60 | 80 |
| n(O2)/mol | 0.0010 | 0.0016 | 0.0020 | 0.0020 |
上述反应过程中能量转化形式为光能转化为 能,达平衡过程中至少需要吸收光能为 kJ(保留三位小数)。
(2)氢气是合成氨工业的原料,合成塔中每产生2mol NH3,放出92.2kJ热量.已知:

则1mol N﹣H键断裂吸收的能量约等于 。
(3)已知:2H2(g)+O2(g)═2H2O(g)△H=﹣483.6kJ/mol
N2(g)+2O2(g)═2NO2(g)△H=+67.7kJ/mol
则H2还原NO2生成水蒸气和氮气反应的热化学方程式是 。
(4)氢镍电池是近年开发出来的可充电电池,它可以取代会产生污染的铜镍电池。氢镍电池的总反应式是 H2+2NiO(OH)  2Ni(OH)2。请由总反应式回答:
2Ni(OH)2。请由总反应式回答:
.电解质溶液应该是 (选填酸溶液、碱溶液),
②.电池放电时,负极反应式为 ,
.外电路中每通过0.2NA个电子时,H2的质量理论上减小 g,
.电池工作时,电子由 极通过外电路流向 极(选填正、负)。
-
氢气是一种清洁能源,氢气的制取是氢能源利用领域的研究热点。
(1)纳米级的Cu2O可作为太阳光分解水的催化剂。一定温度下,在2L密闭容器中加入纳米级Cu2O并通入0.10mol水蒸气发生反应:2H2O(g) 2H2(g)+O2(g)△H = +484kJ·mol—1,不同时段产生O2的量见下表:
2H2(g)+O2(g)△H = +484kJ·mol—1,不同时段产生O2的量见下表:
| 时间/min | 20 | 40 | 60 | 80 |
| n(O2)/mol | 0.0010 | 0.0016 | 0.0020 | 0.0020 |
上述反应过程中能量转化形式为光能转化为 能,达平衡过程中至少需要吸收光能为 kJ。
(2)现有反应:CO(g)+ H2O(g)  CO2(g)+ H2(g) △H<0,在相同温度和相同体积下进行甲、乙、丙、丁四组实验,实验起始时放入容器内各组分的物质的量见下表:
CO2(g)+ H2(g) △H<0,在相同温度和相同体积下进行甲、乙、丙、丁四组实验,实验起始时放入容器内各组分的物质的量见下表:
| 物质的量 | CO | H2 O | CO2 | H2 |
| 甲 | a mol | a mol | 0 mol | 0 mol |
| 乙 | 0mol | 0 mol | 2a mol | a mol |
| 丙 | 0 mol | 0 mol | a mol | a mol |
| 丁 | a mol | a mol | a mol | a mol |
上述四种情况达到平衡后,甲、乙、丙、丁容器中n(CO)的大小顺序为 。
(3)金属钨用途广泛,主要用于制造硬质或耐高温的合金,以及灯泡的灯丝。高温下,在密闭容器中用H2还原WO3得金属钨,总反应为WO3 (s) + 3H2 (g) W (s) + 3H2O (g)。请回答下列问题:
W (s) + 3H2O (g)。请回答下列问题:
①某温度下反应达平衡时,H2与水蒸气的体积比为2:3,则H2的平衡转化率为 。
②上述总反应过程大致分为三个阶段,各阶段主要成分与温度的关系如下表所示:
| 温度 | 25℃ ~ 550℃ ~ 600℃ ~ 700℃ |
| 主要成份 | WO3 W2O5 WO2 W |
假设WO3完全转化为W,则三个阶段消耗H2物质的量之比为 。
③钨丝灯管中的W在使用过程中缓慢挥发,使灯丝变细,加入I2可延长灯管的使用寿命,其工作原理为:W (s) +2I2 (g)  WI4 (g)。下列说法正确的有 (填字母)。
WI4 (g)。下列说法正确的有 (填字母)。
A.灯管内的I2可循环使用
B.WI4在灯丝上分解,产生的W又沉积在灯丝上
C.WI4在灯管壁上分解,使灯管的寿命延长
D.温度升高时,WI4的分解速率加快,W和I2的化合速率减慢
-
(1)纳米级Cu2O由于具有优良的催化性能而受到关注,采用肼(N2H4)燃料电池为电源,用离子交换膜控制电解液中c(OH-)制备纳米Cu2O,其装置如图甲、乙。
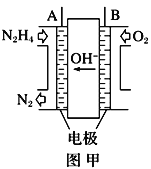
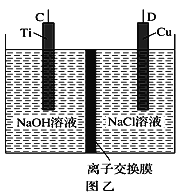
①上述装置中D电极应连接肼燃料电池的____极(填“A”或“B”),该电解池中离子交换膜为_____离子交换膜(填“阴”或“阳”)。
②该电解池的阳极反应式为____________
③当反应生成14.4 g Cu2O时,至少需要肼________ mol。
(2)利用下图丙装置,可以模拟铁的电化学防护。
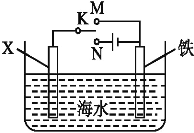
若X为碳棒,为减缓铁的腐蚀,开关K应置于_______处。若X为锌,开关K置于M处,该电化学防护法称为_________。
-
纳米级 Cu2O 由于具有优良的催化性能而受到关注,下表为制取 Cu2O 的四种方法:
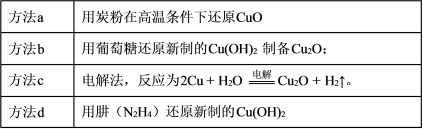
(1)已知:①2Cu(s)+ O2(g)=Cu2O(s);△H = -169kJ·mol-1
O2(g)=Cu2O(s);△H = -169kJ·mol-1
②C(s)+ O2(g)=CO(g);△H = -110.5kJ·mol-1
O2(g)=CO(g);△H = -110.5kJ·mol-1
③ Cu(s)+ O2(g)=CuO(s);△H = -157kJ·mol-1
O2(g)=CuO(s);△H = -157kJ·mol-1
则方法 a 发生的热化学方程式是:__________________________。
(2)方法 c 采用离子交换膜电解法控制电解液中 OH-的浓度而制备纳米 Cu2O,装置如图所示:

上述装置中 A 电极应连_____电极(填“C”或“D”)
②该离子交换膜为_____离子交换膜(填“阴”或“阳”),该电解池的阳极反应式为: _____,钛极附近的 pH 值_____(填“增大”“减小”或“不变”)。
③原电池中 OH-移动方向是向_____(填“左”或“右”)移动,原电池中负极反应式为:_____
(3)在相同的密闭容器中,用以上方法制得的三种 Cu2O 分别进行催化分解水的实验:
2H2O(g)  2H2(g)+O2(g) △H>0。水蒸气的浓度随时间 t 变化如下表所示:
2H2(g)+O2(g) △H>0。水蒸气的浓度随时间 t 变化如下表所示:
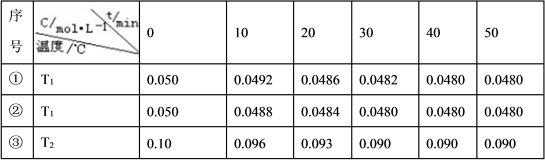
①对比实验的温度:T2_____T1(填“﹥”“﹤”或“﹦”);实验①、②、③的化学平衡常数 K1、K2、K3 的大小关系为:_____
②实验①前 20 min 的平均反应速率 v(O2)=_____
③催化剂的催化效率:实验①_____实验②(填“﹥”或“﹤”)。
-
(1) 纳米级Cu2O由于具有优良的催化性能而受到关注。已知:
2Cu(s)+ O2(g) ="==" Cu2O(s) ΔH=-169kJ·mol-1,
O2(g) ="==" Cu2O(s) ΔH=-169kJ·mol-1,
C(s)+  O2(g) ="==" CO(g) ΔH=-110.5kJ·mol-1,
O2(g) ="==" CO(g) ΔH=-110.5kJ·mol-1,
2Cu(s)+ O2(g)===2 CuO(s) ΔH=-314kJ·mol-1
则工业上用炭粉在高温条件下还原CuO制取Cu2O和CO的热化学方程式为
________。
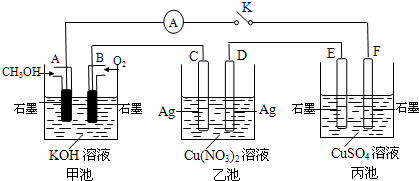
(2)某兴趣小组的同学用下图所示装置研究有关电化学的问题(甲、乙、丙三池中溶质足量),当闭合该装置的电键K时,观察到电流计的指针发生了偏转。
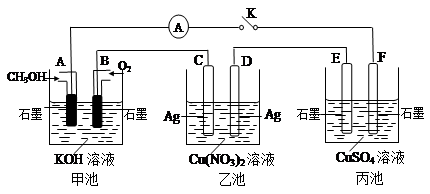
请回答下列问题:
(1)甲池为________(填“原电池”、“电解池”或 “电镀池”),A电极的电极反应式为________。
(2)丙池中F电极为________ (填“正极”、“负极”、“阴极”或“阳极”),该池的总反应方程式为________。
(3)当池中C极质量减轻10.8 g时,甲池中B电极理论上消耗O2的体积为________mL(标准状况)。
(4)一段时间后,断开电键K,下列物质能使乙池恢复到反应前浓度的是________(填选项字母)。
A.Cu B.CuO C.Cu(OH)2 D.Cu2(OH)2CO3
-
纳米级Cu2O由于具有优良的催化性能而受到关注,下表为制取Cu2O的三种方法:

(1)已知:2Cu (s)+½O2(g) =Cu2O(s) △H=-a kJ·mol-1
C (s)+½O2(g) =CO (g) △H=-b kJ·mol-1
Cu (s)+½O2(g) =CuO (s) △H=-c kJ·mol-1
则方法I发生的反应:2CuO(s) +C(s) =Cu2O(s)+CO(g);△H__________kJ·mol-1
(2)工业上很少用方法I制取Cu2O,是由于方法I反应条件不易控制,若控温不当,会降低Cu2O产率,请分析原因:__________________。
(3)方法II为加热条件下用液态肼(N2H4)逐原新制Cu (OH)2来制备纳米级Cu2O,同时放出N2,该制法的化学方程式为____________________。
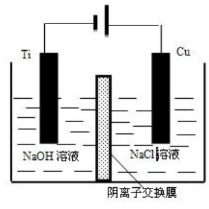
(4)方法III采用离子交换膜控制电解液中OH-的浓度而制备纳米Cu2O,装置如图所示,写出电极反应式并说明该装置制备Cu2O的原理________________________。
(5)在相同的密闭容器中,用以上两种方法制得的Cu2O分别进行催化分解水的实验:
2H2O(g)  2H2(g) + O2(g) △H>O,水蒸气的浓度(mol/L)随时间t(min)变化如下表所示
2H2(g) + O2(g) △H>O,水蒸气的浓度(mol/L)随时间t(min)变化如下表所示
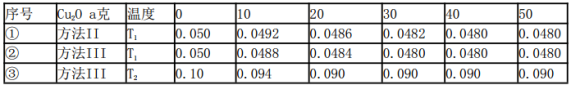
下列叙述正确的是_________(填字母代号).
a.实验的温度:T2<T1
b.实验①前20min的平均反应速率v(O2)=7×10- 5mol/(L·min)
c.实验②比实验①所用的Cu2O催化效率高
d.实验①、②、③的化学平衡常数的关系:K1=K2<K3
-
(1)纳米级Cu2O由于具有优良的催化性能而受到关注.已知:
2Cu(s)+ O2(g)═Cu2O(s)△H=-169kJ•mol-1,
O2(g)═Cu2O(s)△H=-169kJ•mol-1,
C(s)+ O2(g)═CO(g)△H=-110.5kJ•mol-1,
O2(g)═CO(g)△H=-110.5kJ•mol-1,
2Cu(s)+O2(g)═CuO(s)△H=-314kJ•mol-1
则工业上用炭粉在高温条件下还原CuO制取Cu2O和CO的热化学方程式为______.
(2)某兴趣小组的同学用如图所示装置研究有关电化学的问题(甲、乙、丙三池中溶质足量),当闭合该装置的电键K时,观察到电流计的指针发生了偏转.
请回答下列问题:
(1)甲池为______(填“原电池”、“电解池”或“电镀池”),A电极的电极反应式为______.
(2)丙池中F电极为______ (填“正极”、“负极”、“阴极”或“阳极”),该池的总反应方程式为______ 2H2SO4+2Cu+O2↑
-
纳米级Cu2O由于具有优良的催化性能而受到关注,下表为制取Cu2O的两种方法:
| 方法Ⅰ | 用炭粉在高温条件下还原CuO |
| 方法Ⅱ | 电解法的反应为2Cu+H2O  Cu2O+H2↑ Cu2O+H2↑ |
(1)已知:2Cu(s) + 1/2 O2(g) = Cu2O(s) △H = -169KJ/mol
C(s) +1/2 O2(g) = CO(g) △H= -110.5kJ/mol
Cu(s) + 1/2 O2(g) = CuO(s) △H = -157kJ/mol
则方法Ⅰ反应的热化学方程式为______________________ 。
(2)方法Ⅱ采用肼(N2H4)燃料电池为电源,用离子交换膜控制电解液中c(OH-)制备纳米Cu2O,其装置如图甲、乙。
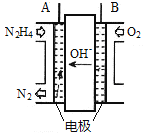
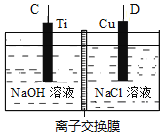
图甲 图乙
①上述装置中D电极应连接肼燃料电池的_______极(填“A”或“B”),该电解池中离子交换膜为______离子交换膜(填“阴”或“阳”)。
②该电解池的阳极反应式为_______________________________,肼燃料电池中A极发生的电极反应为___________________________________。
③当反应生成14.4 g Cu2O时,至少需要肼______mol。
2H2(g)+O2(g) △H=+484 kJ/mol。水蒸气的浓度( mol/L)随时间变化如下表所示:
HCHO(g) + H2(g),CH3OH的平衡转化率随温度变化曲线如图: