-
锡渣主要成分是SnO,还含有少量Fe、Cu、Sb、Pb、As等元素的氧化物.可用下列流程中的方法生产锡酸钠.
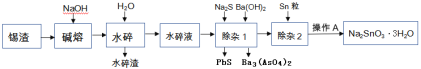
已知: ①砷酸钡难溶于水,Ksp(Ba3(AsO4)2)=10-24
②水碎液中溶质的主要成分为Na2SnO3,Na3AsO4, Na3SbO4,Na2PbO2
(1)碱熔就是在锡渣中加NaOH焙烧,SnO转变为Na2SnO3,则SnO参加反应的化学方程式为____________
(2)除杂1的目的是“除砷和铅”,加入硫化钠所发生反应的离子方程式为____________;若要使0.001mol/L的AsO43-沉淀完全(一般认为离子浓度小于10-6mol/L时即沉淀完全),需等体积加入至少____________mol/L的Ba(OH)2.
(3)除杂2中加入Sn粒的目的是____________
(4)已知Na2SnO3·3H2O可溶于水,难溶于乙醇,加热至140℃时会失去结晶水,所以最后一步从滤液中得到锡酸钠晶体的操作步骤为____________、过滤、用____________洗涤、____________.
(5)水碎渣中的铁元素主要以氧化物形式存在,回收比较容易,而铜冶炼过程中的铜渣中也有铁元素,但主要以硅酸铁的形式存在,回收方法更复杂:需先加CaO作置换剂,发生钙铁置换反应CaO+FeO·SiO2 CaO·SiO2+FeO,在反应过程中,加CaO的同时还需加入还原剂烟煤,则加入还原剂烟煤的作用是____________
CaO·SiO2+FeO,在反应过程中,加CaO的同时还需加入还原剂烟煤,则加入还原剂烟煤的作用是____________
-
锡酸钠晶体(Na2SnO3•3H2O2)在染料工业用作媒染剂。以锡渣废料(主要成分是SnO,还含有少量Fe、Te、Sb、Pb、As等元素的氧化物)为原料,制备锡酸钠晶体的工艺流程图如图:
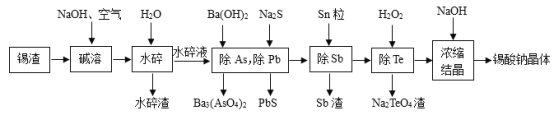
已知:水碎液中溶质的主要成分为Na2SnO3、Na3AsO4、Na3SbO4、Na2PbO2、Na2TeO3。
(1)“碱溶”时,SnO发生反应的化学方程式为___。
(2)工业上制备锡酸钠晶体(Na2SnO3•3H2O)时,会将“水碎渣”再次水洗,其目的是___。
(3) “除Sb”时发生反应的离子方程式为___。
(4) “除Te”过程中氧化剂与还原剂的物质的量之比为___,该过程中反应时间、反应温度对Te的脱除率的影响关系如图,则70℃后随温度升高Te的脱除率下降的原因可能是___;“除Te”的最优反应时间和反应温度分别为___、___。

(5)已知锡酸钠的溶解度一般随着温度的升高而升高,则在“浓缩、结晶”时,加入NaOH的原因是___。
-
锡酸钠(Na2SnO3)主要用作电镀铜锡合金和碱性镀锡的基本原料。锡精矿除含SnO2外,还含有少量WO3、S、As、Fe,一种由锡精矿制备锡酸钠的工艺流程如图:
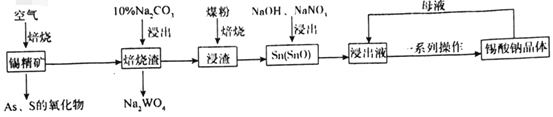
已知:①焙烧后,S、As变为挥发性氧化物而被除去,Fe变为Fe3O4;
②锡酸钠易溶于水,其溶解度随着温度的升高而降低。
请回答下列问题:
(1)Na2SnO3中锡元素的化合价为___,从焙烧渣中除去Fe3O4最简单的方法为___。
(2)WO3与Na2CO3溶液反应生成Na2WO4的化学方程式为___。
(3)加入煤粉焙烧可将SnO2还原为Sn或SnO,Sn或SnO在碱性条件下均能被NaNO3氧化为Na2SnO3,已知NaNO3的还原产物为NH3,则NaNO3氧化Sn的化学方程式为___。
(4)如图为加入NaOH溶液和NaNO3溶液浸出时锡的浸出率与NaOH的质量浓度和反应时间的关系图,则“碱浸”时最适宜条件为___、___。

(5)从浸出液中获得锡酸钠晶体的“一系列操作”具体是指___,将母液返回至浸出液的目的为___。
(6)碱性镀锡以NaOH和Na2SnO3为电解液,以纯锡为阳极材料,待镀金属为阴极材料,镀锡时阳极反应的电极反应式为___。
-
锡酸钠(Na2SnO3·xH2O)主要用作电镀铜锡合金和碱性镀锡的基本原料。锡精矿除含SnO2外,还含有少量WO3、S、As、Fe,—种由锡精矿制备锡酸钠的工艺流程如下:
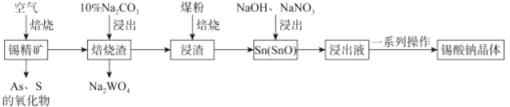
已知:①焙烧后,S、As变为挥发性氧化物而被除去,Fe变为Fe3O4;
②Na2SnO3•xH2O。易溶于水,其在水中的溶解度随着温度的升高而降低。
请回答下列问题:
(1)Sn元素的原子序数为50,其在周期表中的位置为_____________。
(2)从“焙烧渣”中除去Fe3O4最简单的方法为_____________。加入煤粉焙烧可将SnO2还原为Sn或SnO,Sn或SnO。在碱性条件下均能被NaNO3氧化为Na2SnO3,已知NaNO3的还原产物为NH3,则NaNO3氧化Sn的化学方程式为___________________。
(3)如图为加入NaOH溶液和NaNO3溶液浸出时锡的浸出率与NaOH质量浓度和反应温度间的关系图,则“碱浸”的最适宜条件为_____________、___________,
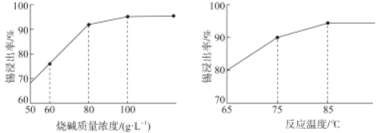
(4)从浸出液中获得锡酸钠晶体的“一系列操作”具体是指___________、洗涤、干燥。
(5)采用热重分析法测定锡酸钠晶体样品所含结晶水数,将样品加热到140℃时,失掉全部结晶水,失重约20.2%。锡酸钠晶体的化学式为__________。
(6)以纯锡为阳极材料,以NaOH和Na2SnO3为电解液,待镀金属为阴极材料,可实现在待镀金属上的持续镀锡,镀锡时阳极的电极反应式为______________。
-
重铬酸钠(Na2Cr2O7·2H2O)是重要的化工原料,在化学工业和制药工业中常用作氧化剂。可用一种铬铁矿(主要成分:FeO·Cr2O3,还含有少量的Al2O3)通过以下流程来制取重铬酸钠。

回答下列问题:
(1)写出Cr元素基态原子的外围电子排布式____。
(2)步骤I中反应的化学方程式为:4FeO·Cr2O3(s)+8Na2CO3(s)+7O2(g)=8Na2CrO4(s)+2Fe2O3(s)+8CO2(g),反应中被氧化的元素是 ,生成2 mol Fe2O3时转移电子的物质的量为 mol。
(3)步骤II中加入NaOH溶液时发生的化学反应方程式为 。
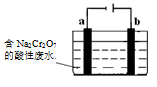
(4)+3、+6价铬都有很强的毒性,+6价铬的毒性更高,可诱发肺癌和鼻咽癌。工业上常用电解法来处理含Cr2O72-的废水,电解装置模拟示意图如右图(电极材料为铁和石墨)。通电后,Cr2O72-在b极附近转变为Cr3+,一段时间后Cr3+最终可在a极附近变成Cr(OH)3沉淀而被除去。a电极的电极材料是____,b电极附近生成Cr3+的反应的离子方程式是____。
将含Cr2O3为50%的铬铁矿30.4 kg,按上述流程制取产品Na2Cr2O7·2H2O,假设整个流程中铬元素的利用率为80%,则最终能制得Na2Cr2O7·2H2O kg。
-
下列说法正确的是( )
A.亚硝酸钠溶液具有防腐作用,可用来浸泡新鲜瓜果
B.我国古代就已采用加热胆矾或绿矾的方法制取硫酸
C.红宝石是含有少量金属氧化物的刚玉,主要成分为二氧化硅
D.Na3AlF6溶液中滴加lmol/L氨水至过量会产生白色沉淀
-
铝是一种重要的金属,在生产、生活中具有许多重要的用图,如图是从铝土矿中制备铝的工艺流程:

已知:
①铝土矿的主要成分是Al2O3,此外还含有少量SiO2、Fe2O3等杂质;
②溶液中的硅酸钠与偏铝酸钠反应,能生成硅铝酸盐沉淀,化学反应方程式为:2Na2SiO3+2NaAlO2+2H2O═Na2Al2Si2O8↓+4NaOH
回答下列问题:
(1)溶解铝土矿时,其成分与NaOH溶液发生反应的离子方程式: .
(2)滤渣A的主要成分为 ;硅酸盐沉淀写成氧化物的形式是 .
(3)在工艺流程第三步中,选用二氧化碳作酸化剂而不使用盐酸的原因是 .
(4)若该工厂用mkg铝土矿共制得nkgAl(假设每步反应进行完全),则铝土矿中Al2O3的质量分数为 .
(5)若将铝用酸溶解,下列试剂中最好选用 (填编号).
A.浓硫酸 B.稀硫酸 C.稀HNO3 D.浓HNO3
(6)电解冶炼铝时用Na3AlF6作助熔剂,Na3AlF6是配合物,其中内界是 ,配位数为 .
-
铜蓝是一种天然含铜矿石,它的主要成分是CuS,同时还含有少量铁的化合物。工业上常以铜蓝为原料生产可用作颜料、木材防腐剂等的化工产品 ,其工艺流程如下:
,其工艺流程如下:

已知: 、
、 、
、 完全沉淀时的pH分别为
完全沉淀时的pH分别为 、
、 、
、 。
。
 与
与 的溶解度曲线如图所示。
的溶解度曲线如图所示。

 “焙烧”时,主反应的产物为等物质的量的两种盐。写出相应的化学反应方程式 _________________________。
“焙烧”时,主反应的产物为等物质的量的两种盐。写出相应的化学反应方程式 _________________________。
 结合题意,试剂A最好选用______
结合题意,试剂A最好选用______ 填编号
填编号



 浓硫酸
浓硫酸
选择该试剂的理由是____________________________。所得滤渣为________________。
 为了获得
为了获得 晶体,对滤液B进行的操作是:蒸发浓缩,趁热过滤,滤液经冷却结晶,过滤得到产品。分析有关物质的溶解度曲线
晶体,对滤液B进行的操作是:蒸发浓缩,趁热过滤,滤液经冷却结晶,过滤得到产品。分析有关物质的溶解度曲线 图
图 ,“趁热过滤”得到的固体是_____________,“冷却结晶”过程中,析出
,“趁热过滤”得到的固体是_____________,“冷却结晶”过程中,析出 晶体的合适温度为___________________。
晶体的合适温度为___________________。
 色光度是产品质量指标之一,合格
色光度是产品质量指标之一,合格  晶体的色光度范围为
晶体的色光度范围为 ,反应过程溶液 pH 对产率、色光度的影响如图2所示,综合考虑制备时应控制 pH 的较合理范围是_______________。
,反应过程溶液 pH 对产率、色光度的影响如图2所示,综合考虑制备时应控制 pH 的较合理范围是_______________。
 已知铜蓝的形成过程如下:
已知铜蓝的形成过程如下: 在自然界中,各种原生铜的矿物经氧化转变为可溶性的
在自然界中,各种原生铜的矿物经氧化转变为可溶性的 溶液,
溶液, 经淋滤作用后溶液向地壳深部渗透,遇到深层的闪锌矿
经淋滤作用后溶液向地壳深部渗透,遇到深层的闪锌矿 或方铅矿
或方铅矿 慢慢转化为铜蓝
慢慢转化为铜蓝 。写出过程
。写出过程 中任意一个反应的离子方程式 ________________。
中任意一个反应的离子方程式 ________________。
-
铝是一种重要的金属,在生产、生活中具有许多重要的用途,下图是从铝土矿中制备铝的工艺流程:

已知:
(1)铝土矿的主要成分是Al2O3,此外还含有少量SiO2、Fe2O3等杂质;
(2)溶液中的硅酸钠与偏铝酸钠反应,能生成硅铝酸盐沉淀,化学反应方程式为:2Na2SiO3+2NaAlO2+2H2O=Na2Al2Si2O8↓+4NaOH
回答下列问题:
(1)写出向铝土矿中加入足量氢氧化钠溶液后,该步操作中发生反应的离子方程式: 。
(2)滤渣A的主要成分为 ;滤渣A的用途是 (只写一种);实验室过滤时使用玻璃棒,其作用是 。
(3)在工艺流程第三步中,选用二氧化碳作酸化剂的原因是 。
(4)若将铝溶解,下列试剂中最好选用 (填编号)。
A.浓硫酸 B.稀硫酸 C.稀硝酸
理由是 。
-
铝是一种重要的金属,在生产、生活中具有许多重要的用途,下图是从铝土矿中制备铝的工艺流程:

已知:(1)铝土矿的主要成分是Al2O3,此外还含有少量SiO2、Fe2O3等杂质;
(2)溶液中的硅酸钠与偏铝酸钠反应,能生成硅铝酸盐沉淀,化学反应方程式为:
2Na2SiO3+2NaAlO2+2H2O = Na2Al2Si2O8↓+4NaOH
回答下列问题:
(1)写出向铝土矿中加入足量氢氧化钠溶液操作中发生反应的离子方程式:____________;__________。
(2)滤渣A的主要成分为_ ;滤渣A的用途是 (只写一种);实验室过滤时使用玻璃棒,其作用是 。
(3)在工艺流程第三步中,选用二氧化碳作酸化剂的原因是: 。
(4)若将铝溶解,下列试剂中最好选用__ ____(填编号)。
A.浓硫酸 B.稀硫酸 C.稀硝酸

CaO·SiO2+FeO,在反应过程中,加CaO的同时还需加入还原剂烟煤,则加入还原剂烟煤的作用是____________












