-
碳和氮的化合物在生产生活中广泛存在。回答下列问题:
(1)三氯化氮(NCl3)是一种黄色、油状、具有刺激性气味的挥发性有毒液体,其原子均满足8e—结构。写出其电子式_____________________。氯碱工业生产时,由于食盐水中通常含有少量NH4Cl,而在阴极区与生成的氯气反应产生少量三氯化氮,该反应的化学方程式为______________。
(2)已知:2CO2(g) + 3NaOH(aq)=NaHCO3(aq)+Na2CO3(aq)+H2O(l) △H=-4a kJ/mol
CO2(g) +2NaOH(aq)=Na2CO3(aq)+H2O(l) △H=-b kJ/mol
该条件下CO2与NaOH溶液反应生成NaHCO3的热化学反应方程式为:____________。
(3)利用CO可以将NO转化为无害的N2,其反应为:2NO(g)+2CO(g) N2(g)+2CO2(g),向容积均为IL的甲、乙、丙三个恒温(反应温度分别为300℃、T℃、300℃)容器中分别加入相同量NO和CO,测得各容器中n(CO)随反应时间t的变化情况如下表所示:
N2(g)+2CO2(g),向容积均为IL的甲、乙、丙三个恒温(反应温度分别为300℃、T℃、300℃)容器中分别加入相同量NO和CO,测得各容器中n(CO)随反应时间t的变化情况如下表所示:
| t/min | 0 | 40 | 80 | 120 | 160 |
| n(CO)(甲容器)/mol | 2.00 | 1.50 | 1.10 | 0.80 | 0.80 |
| n(CO)(乙容器)/mol | 2.00 | 1.45 | 1.00 | 1.00 | 1.00 |
| n(CO)(丙容器)/mol | 1.00 | 0.80 | 0.65 | 0.53 | 0.45 |
①甲容器中,0~40min内用NO的浓度变化表示的平均反应速率v(NO)=_______。
②该反应的△H______0(填“>”或“<”)。
③甲、丙容器达到平衡时,CO的转化率为α(甲)________α(乙)(填“>”,“< ”,“=”)
(4)常温下,在(NH4)2C2O4溶液中,反应NH4++C2O42—+H2O NH3·H2O+HC2O4—的平衡常数K=___。(已知常温下,H2C2O4的电离平衡常数Ka1≈5×10-2,Ka2≈5×10-5 H2O的电离平衡常数Kw=1×10-14 NH3·H2O的电离平衡常数Kb≈2×10-5)
NH3·H2O+HC2O4—的平衡常数K=___。(已知常温下,H2C2O4的电离平衡常数Ka1≈5×10-2,Ka2≈5×10-5 H2O的电离平衡常数Kw=1×10-14 NH3·H2O的电离平衡常数Kb≈2×10-5)
-
三氯化氮(NCl3)是一种淡黄色的油状液体,测得其分子具有三角锥形结构。则下面对于NCl3的描述不正确的是( )
A.它是一种极性分子 B.它的挥发性比NBr3要大
C.它还能再以配位键与Cl-结合 D.已知NBr3对光敏感,所以NCl3对光也敏感
-
三氯化氮(NCl3)是一种淡黄色的油状液体,测得其分子具有三角锥形结构。则下面对于NCl3的描述不正确的是( )
A.它是一种极性分子
B.它的挥发性比PBr3要大
C.它还能再以配位键与Cl-结合
D.已知NBr3对光敏感,所以NCl3对光也敏感
-
三氯化氮(NCl3)是一种淡黄色的油状液体,下面对于NCl3的描述不正确的是( )
A.NCl3为三角锥形 B.NCl3是一种极性分子
C.它还能再以配位键与Cl-结合 D.NCl3的挥发性比PBr3要大
-
三氯化氮(NCl3)是一种淡黄色的油状液体,其分子空间构型与NH3相似。则下面对于NCl3的描述正确的是 ( )
A.是由极性键形成的非极性分子 B.它的挥发性比PBr3要小
C.它还能再以配位键与H+结合 D.Cl—N—Cl的键角是120º
-
三氯化氮(NCl3)是一种淡黄色的油状液体,测得其分子具有三角锥形结构,则下面对于NCl3的描述不正确的是
A.N原子是sp3杂化 B.该分子中的氮原子上有孤对电子
C.它还可以再以配位键与Cl-结合 D.已知NBr3对光敏感,所以NCl3对光也敏感
-
碳和氮的化合物在生产生活中广泛存在。回答下列问题:
(1)催化转化器可使汽车尾气中的主要污染物(CO、NOx、碳氢化合物)进行相互反应,生成无毒物质,减少汽车尾气污染。
已知:N2(g)+O2(g)=2NO(g) △H1=+180.5 kJ/mol;
2C(s)+O2(g)=2CO(g) △H2=-221.0 kJ/mol;
C(s)+O2(g)=CO2(g) △H3=-393.5 kJ/mol
则尾气转化反应2NO(g) +2CO(g)=N2(g)+2CO2(g)的△H=___________。
(2)氨是一种重要的化工原料,在工农业生产中有广泛的应用。在773 K时,分别将2.00 mol N2和6.00 mol H2充入一个固定容积为1 L的密闭容器中,随着反应的进行,气体混合物中n(H2)、n(NH3)与反应时间(t)的关系如表所示:
| t/min | 0 | 5 | 10 | 15 | 20 | 25 | 30 |
| n(H2)/mol | 6.00 | 4.50 | 3.60 | 3.30 | 3.03 | 3.00 | 3.00 |
| n(NH3)/mol | 0 | 1.00 | 1.60 | 1.80 | 1.98 | 2.00 | 2.00 |
①该温度下,若向同容积的另一容器中投入N2、H2、NH3,其浓度均为3 mol/L,则此时v正____v逆(填“大于”“小于”或“等于”)。
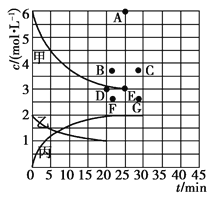
②由表中的实验数据可得到“c—t”的关系,如图所示,表示c(N2)—t的曲线是______。在此温度下,若起始充入4 mol N2和12 mol H2,则反应刚达到平衡时,表示c(H2)—t的曲线上相应的点为________。
(3)NOx的排放主要来自于汽车尾气,有人利用反应C(s)+2NO(g) N2(g)+CO2(g) △H=-34.0kJ/mol,用活性炭对NO进行吸附。已知在密闭容器中加入足量的C和一定量的NO气体,保持恒压测得NO的转化率随温度的变化如图所示:
N2(g)+CO2(g) △H=-34.0kJ/mol,用活性炭对NO进行吸附。已知在密闭容器中加入足量的C和一定量的NO气体,保持恒压测得NO的转化率随温度的变化如图所示:
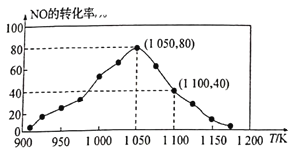
①由图可知,在1100K时,CO2的体积分数为__________。
②用某物质的平衡分压代替其物质的量浓度也可以表示化学平衡常数(记作Kp)。在1050K、1.1×106Pa时,该反应的化学平衡常数Kp=______[已知:气体分压(P分)=气体总压(Pa)×体积分数]。
(4)在酸性电解质溶液中,以惰性材料作电极,将CO2转化为丙烯 原理如图所示
原理如图所示
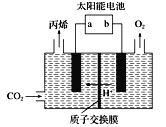
①太阳能电池的负极是_______(填“a”或“b”)
②生成丙烯的电极反应式是___________。
-
氮和硫的化合物在生产生活中广泛存在。研究发现,NOx和SO2是雾霾的主要成分。
Ⅰ.(1)已知:
2CO(g)+O2(g)  2CO2(g) △H1=﹣566.00kJ•mol-1
2CO2(g) △H1=﹣566.00kJ•mol-1
2SO2(g)+O2(g)  2SO3(g) △H2=﹣196.6kJ•mol-1
2SO3(g) △H2=﹣196.6kJ•mol-1
2NO(g)+O2(g)  2NO2(g) △H3=﹣113.0kJ•mol-1
2NO2(g) △H3=﹣113.0kJ•mol-1
则反应2NO2(g)+SO2(g)+ CO(g)  SO3(g)+2NO(g)+ CO2(g)的△H=_________kJ•mol-1。
SO3(g)+2NO(g)+ CO2(g)的△H=_________kJ•mol-1。
(2)NOx主要来源于汽车尾气。T℃时,模拟汽车尾气催化转化:2NO+2CO 2CO2+N2,将等物质的量的NO和CO充入容积为2L的密闭容器中,保持温度和体积不变,反应过程(0~15min)中NO的物质的量随时间变化如右图所示:
2CO2+N2,将等物质的量的NO和CO充入容积为2L的密闭容器中,保持温度和体积不变,反应过程(0~15min)中NO的物质的量随时间变化如右图所示:

①T℃时该化学反应的平衡常数K=____;
②图中a、b分别表示使用同种催化剂时,达到平衡过程中n(NO)的变化曲线,其中表示催化剂表面积较大的曲线是____(填“a”或“b”)。
Ⅱ.科学家发明了NH3燃料电池,以KOH为电解质,原理如右图所示。该燃料电池的负极反应式为__________________。

Ⅲ.SO2主要来源于煤的燃烧。
25℃时,电离平衡常数:
| 化学式 | H2CO3 | H2SO3 |
| 电离平衡常数 | K1=4.30×10-7 K2=5.61×10-11 | K1=1.54×10-2 K2=1.02×10-7 |
回答下列问题:
(1)常温下,pH相同的下列溶液:①Na2CO3、②NaHCO3、③Na2SO3。物质的量浓度由大到小的排列顺序为___________>___________>___________。(用序号表示)
(2)已知NaHSO3溶液显酸性,下列说法正确的是_________________。
A. c(Na+)=2c(SO32-)+2c(HSO3-)+2c(H2SO3)
B. c(Na+)+c(H+)=c(OH-)+c(HSO3-)+c(SO32-)
C. c(HSO3-)> c(H+)> c(H2SO3)> c(SO32-)
D. c(H+)+c(H2SO3)=c(SO32-)+c(OH-)
-
根据下列实验操作和现象所得到的实验结论正确的是( )
| 选项 | 实验操作和现象 | 实验结论 |
| A | 在蔗糖中滴加浓硫酸,蔗糖变黑并产生有刺激性气味的气体 | 只能证明浓硫酸具有脱水性 |
| B | 向黄色的Fe2(SO4)3溶液中滴加氢碘酸,溶液颜色加深 | 氧化性:Fe3+>I2 |
| C | 加热盛有少量NH4HCO3固体的试管,并在试管口放置湿润的红色石蕊试纸,石蕊试纸变蓝 | NH4HCO3显碱性 |
| D | 某钾盐溶于盐酸,产生能使澄清石灰水变浑浊的无色无味气体 | 该钾盐是K2CO3 |
A. A B. B C. C D. D
-
三氯化氮NCl3在常温下是一种淡黄色气体,其分子呈三角锥型,以下关于NCl3叙述正确的是( )
A.NCl3分子中的电荷分布是均匀、对称的
B.NCl3分子是非极性分子
C.NCl3分子中不存在极性共价键
D.分子中所有原子最外层都达到8个电子的稳定结构

N2(g)+CO2(g) △H=-34.0kJ/mol,用活性炭对NO进行吸附。已知在密闭容器中加入足量的C和一定量的NO气体,保持恒压测得NO的转化率随温度的变化如图所示:

原理如图所示


