-
I.(化学反应原理)
原电池原理的发现是储能和供能技术的巨大进步,是化学对人类的一项重大贡献。将纯锌片和纯铜片按图方式插入100mL相同浓度的稀硫酸中一段时间,回答下列问题:
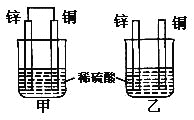
(1)在相同时间内, 两烧杯中产生气泡的速度:甲__乙(填“>”“<”或“=”)。
(2)请写出图中构成原电池的负极电极反应式:__。
II.(化学与生活)
材料是人类生存和发展的物质基础,合理使用材料可以改善我们的生活。
(1)在原子反应堆中得以广泛应用的钠钾合金在常温下呈液态,说明合金的熔点比其各成分金属的熔点___。(选填“高”或“低”)
(2)石英玻璃纤维又称光导纤维,其主要成分和NaOH溶液反应的化学方程式为___。
-
原电池原理的发现是储能和供能技术的巨大进步,是化学对人类一项重大贡献。
(1)现有如下两个反应:A.NaOH + HCl = NaCl + H2O, B.2FeCl3 + Cu = 2FeCl2 + CuCl2
判断能否设计成原电池A.__________B.____________。(填“能”或“不能”)
(2)由铜片、锌片和足量稀H2SO4组成的原电池中,若锌片只发生原电池腐蚀,一段时间后某电极产生3.36L标准状况下的气体。
①负极是_________(填“锌”或“铜”);
②正极的电极反应式为__________________________________;
③产生这些气体共需转移电子_________________mol。
-
原电池原理的发现是贮能和供能技术的巨大进步。关于右图所示原电池的说法不正确的是
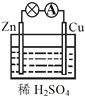
A. 电子经Zn片流向Cu片
B. 锌为负极,发生还原反应
C. 该装置能将化学能转化为电能
D. 锌片上发生的反应为 Zn-2e-  Zn2+
Zn2+
-
合成氨是人类科学技术上的一项重大突破,是化学和技术对社会发展与进步的巨大贡献之一。在制取合成氨原料气的过程中,常混有一些杂质,如CO会使催化剂中毒。除去CO的化学反应方程式(HAc表示醋酸): Cu(NH3)2Ac+CO+NH3==Cu(NH3)3 (CO) Ac。
请回答下列问题:
(1)C、N、O的第一电离能由大到小的顺序为________。
(2)配合物Cu(NH3)3 (CO) Ac中心原子的配位数为________,基态铜原子核外电子排布式为_________________。
(3)写出与CO互为等电子体的粒子________ (任写一个) 。
(4)在一定条件下NH3与CO2能合成化肥尿素[CO(NH2)2],尿素中,C原子轨道的杂化类型为________;1 mol尿素分子中,σ键的个数为____________。(设NA为阿伏加德罗常数的值)
(5)铜金合金形成的晶胞如图所示,其中Cu、Au原子个数比为________。铜单质晶胞与铜金合金的晶胞相似,晶胞边长为3.61×10-8cm,则铜的密度为________g/cm-3(结果保留3位有效数字)。

-
原电池原理的发现和各式各样电池装置的发明是化学对人类的一项重大贡献.关于如图所示原电池的说法正确的是( )
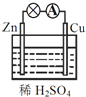
A.将电能转化为化学能的装置
B.电子由铜片经导线流向锌片
C.锌片为负极,发生氧化反应
D.铜片上发生的反应为Cu2++2e﹣═Cu
-
原电池原理的发现和各式各样电池装置的发明是化学对人类的一项重大贡献.关于如图所示原电池的说法正确的是( )
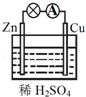
A.将电能转化为化学能的装置
B.电子由铜片经导线流向锌片
C.锌片为负极,发生氧化反应
D.铜片上发生的反应为Cu2++2e﹣═Cu
-
原电池的发明是化学对人类的一项重大贡献。
(1)一种新型燃料电池,它以多孔铂板为两个电极插入稀硫酸中,然后分别向两极通入氢气和氧气而获得电能。通入氢气的电极反应式为_________________。
(2)电子工业上常利用FeCl3溶液腐蚀铜板制作印刷电路,若将该反应原理设计成原电池,请写出原电池的正极反应______________________________。
(3)常温下,将除去表面氧化膜的铝片、铜片插入浓HNO3中组成原电池装置如图甲所示,测得原电池的电流强度(I)随时间(t)的变化如图乙所示,反应过程中有红棕色气体产生。

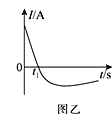
t1s前,原电池的负极是铝片,正极的电极反应式为________,溶液中的H+向______(填“正”或“负”)极移动。t1s后,外电路中电子流动方向发生改变,其原因是_________________。
-
电池的发明和应用是化学家们对人类社会的重要贡献之一。
I 每一次化学电池技术的突破,都带来了电子设备革命性的发展。最近,我国在甲醇燃料电池的相关技术上获得了新突破,原理如图1所示。
(1) 请写出从C口通入O2发生反应的电极反应式: 。
(2) 以石墨做电极电解饱和食盐水,如图2所示。电解开始后在 的周围(填“阴极”或“阳极”)先出现红色。假设电池的理论效率为80%(电池的理论效率是指电池产生的最大电能与电池反应所释放的全部能量之比),若消耗6.4g甲醇气体,外电路通过的电子个数为 (保留两位有效数字, 取
取 )
)

II 随着电池使用范围的日益扩大,废旧电池潜在的污染已引起社会各界的广泛关注。
(1) 电池生产企业排放的工业废水中常含有Cu2+等重金属离子,直接排放会造成污染,目前在工业废水处理过程中,依据沉淀转化的原理,常用FeS等难溶物质作为沉淀剂除去这些离子。已知室温下 (FeS)=
(FeS)=
 ,
, (CuS)=
(CuS)=
 。请用离子方程式说明上述除杂的原理: 。
。请用离子方程式说明上述除杂的原理: 。
(2) 工业上为了处理含有Cr2O72—的酸性工业废水,用绿矾(FeSO4·7H2O)把废水中的六价铬离子还原成三价铬离子,再加入过量的石灰水,使铬离子转变为Cr(OH)3沉淀。
①氧化还原过程的离子方程式为 。
②常温下,Cr(OH)3的溶度积 =
=
 ,溶液中pH至少为 ,才能使Cr3+沉淀完全。
,溶液中pH至少为 ,才能使Cr3+沉淀完全。
③现用上述方法处理100m3含铬(+6价)78 的废水,需用绿矾的质量为 Kg。(写出主要计算过程)
的废水,需用绿矾的质量为 Kg。(写出主要计算过程)
-
原电池是化学对人类的一项重大贡献。某兴趣小组为研究原电池原理,设计如图装置:
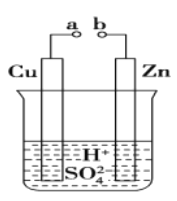
(1)a和b用导线连接,Zn极为原电池__________极(填“正”或“负”),Cu极发生__________(填“氧化”或“还原”),溶液中SO42-移向_________(填“Cu”或“Zn”)极
(2)无论a和b是否连接,Zn片均被腐蚀。若转移了0.4mol电子,则理论上Zn片应溶解__________g
(3)有同学想把Ba(OH)2·8H2O晶体与NH4NO3晶体的反应设计成原电池,你认为是否可行?__________(填“是”或“否”),理由是 __________
-
原电池是化学对人类的一项重大贡献。某兴趣小组为研究原电池原理,设计如图装置:

(1)a和b用导线连接,溶液中H+移向______(填“Cu”或“Zn”)极,Cu极的电极反应式为________;
(2)无论a和b是否连接,Zn片均被腐蚀.若转移了0.2mol电子,则理论上Zn片质量减轻___g。









