已知元素原子的下列结构或性质,能确定其在周期表中位置的是( )
A.某元素原子的第二电子层电子排布图为
B.某元素在某种化合物中的化合价为+4
C.某元素的原子最外层上电子数为6
D.某元素的外围电子排布式为5s25p1
高二化学单选题中等难度题
已知元素原子的下列结构或性质,能确定其在周期表中位置的是( )
A.某元素原子的第二电子层电子排布图为
B.某元素在某种化合物中的化合价为+4
C.某元素的原子最外层上电子数为6
D.某元素的外围电子排布式为5s25p1
高二化学单选题中等难度题
已知元素原子的下列结构或性质,能确定其在周期表中位置的是( )
A.某元素原子的第二电子层电子排布图为
B.某元素在某种化合物中的化合价为+4
C.某元素的原子最外层上电子数为6
D.某元素的外围电子排布式为5s25p1
高二化学单选题中等难度题查看答案及解析
已知元素原子的下列结构或性质,能确定其在周期表中位置的是( )
A.某元素原子的第二电子层电子排布图为
B.某元素在某种化合物中的化合价为+4
C.某元素的原子最外层上电子数为6
D.某元素的外围电子排布式为5s25p1
高二化学单选题中等难度题查看答案及解析
已知元素原子的下列结构或性质,能确定其在周期表中位置的是( )
A. 某元素原子的第二电子层电子排布图为
B. 某元素在某种化合物中的化合价为+4
C. 某元素的原子最外层上电子数为6
D. 某元素的外围电子排布式为5s25p1
高二化学单选题中等难度题查看答案及解析
具有下列电子层结构的原子或离子,其对应的元素在周期表中的位置说法正确的
A. 最外层电子排布为1s2的原子和最外层电子排布为2s2的原子,所对应的两元素一定在同一主族
B. 3p能级上有1个空轨道的原子和4p能级上有1空轨道的原子,所对应的两元素一定在同一主族
C. 最外层电子排布为nsnnpn的原子和最外层电子排布为2s22p6的离子,所对应的两元素一定在同一周期
D. 原子核外M层上的s能级和p能级都填满了电子,而d轨道上尚未有电子的两种原子,所对应的两元素一定在同一周期
高二化学单选题中等难度题查看答案及解析
【化学选修3:物质结构与性质】(15分)
(1)目前,利用金属或合金储氢的研究已取得很大进展,如图是一种镍基合金储氢后的晶胞结构图。
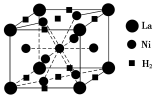
①Ni在元素周期表中的位置是 ,其基态原子的外围电子排布式 是 。
②该合金储氢后,含1 mol La的合金可吸收H2的物质的量为 。
(2)Ti(BH4)2是一种过渡元素硼氢化物储氢材料。
①Ti2+基态的电子排布式可表示为 。
②BH—4的空间构型是 (用文字描述)。
(3)液氨是富氢物质,是氢能的理想载体,利用N2+3H2 2NH3实现储氢和输氢。下列说法正确的是 (多项选择)。
a.NH3分子中N原子采用sp3杂化
b.相同压强时,NH3沸点比PH3高
c.[Cu(NH3)4]2+离子中,N原子是配位原子
d.CN—的电子式为:
(4)MgH2是金属氢化物储氢材料,其晶胞结构如图12所示,已知该晶体的密度ag·cm-3,则晶胞的体积为 cm3〔用含a、NA的代数式表示(NA表示阿伏伽德罗常数)〕。
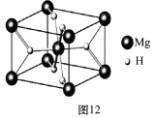
高二化学填空题中等难度题查看答案及解析
[化学-选修3:物质结构与性质]
铁铜是人类最早大规模使用的金属,它们的化合物在科学研究和工业生产中具有许多用途。请回答以下问题:
(1)铁元素在周期表中的位置是________,铜的基态原子核外电子排布式为__________,元素铁与铜的第二电离能分别为:ICu="1958" kJ·mol-1、IFe="1561" kJ·mol-1,ICu比IFe大得多的原因是_______。
(2)二茂铁[Fe(C5H5)2],橙色晶型固体,有类似樟脑的气味,抗磁性。熔点172.5~173℃,100℃以上升华,沸点249℃。据此判断二茂铁晶体类型为______________。
(3)蓝矾(CuSO4·5H2O)的结构如下图所示:
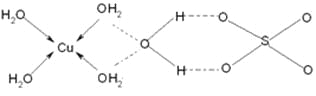
图中虚线表示_____________,SO42-的立体构型是__________,其中S原子的杂化轨道类型是___________;O原子的价电子排布图为__________________。
(4)铁有δ、γ、α三种同素异形体,下图是它们的晶体结构图,三种晶体中铁原子周围距离最近的铁原子个数之比为___________。
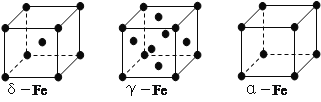
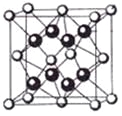
(5)某种具有储氢功能的铜合金晶体具有立方最密堆积的结构,晶胞中Cu原子处于面心,Au原子处于顶点位置,该晶体中原子之间的作用力是_______________。氢原子可进入到由Cu原子与Au原子构成的四面体空隙中。若将Cu原子与Au原子等同看待,该晶体储氢后的晶胞结构与 CaF2的结构(晶胞结构如右图)相似,该晶体储氢后的化学式为______________。
高二化学综合题中等难度题查看答案及解析
有四种短周期元素.它们的结构、性质等信息如下表所述:

请根据表中信息填写:
(1)A原子的核外电子排布式为________________。
(2)B元素在周期表中的位置是____;离子半径:B_____A(填“大于”或“小于”)。
(3)C原子的电子排布图是________,其原子核外有________个未成对电子,能量最高的电子为________轨道上的电子,其轨道呈________形。
(4)D原子的外围电子排布式为____________,D-的结构示意图是____________。
(5)B的最高价氧化物对应的水化物与A的最高价氧化物对应的水化物反应的化学方程式为________;B的最高价氧化物对应的水化物与D的氢化物的水溶液反应的化学方程式为__________________。
高二化学填空题简单题查看答案及解析
【物质结构与性质】(15分)
根据元素周期表中第四周期元素的相关知识,回答下列问题:
(1)第四周期元素的基态原子的电子排布中4s轨道上只有1个电子的元素有_______种;
写出Cu+的核外电子排布式_________。
(2)按电子排布,可将周期表里的元素划分成五个区域,第四周期元素中属于s区的元素有___________种,属于d区的元素有________种。
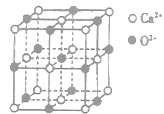
(3)CaO晶胞如图所示,CaO晶体中Ca2+的配位数为________;CaO的焰色反应为砖红色,许多金属或它们的化合物都可以发生焰色反应,其原因是________。
(4)由叠氮化钾(KN3)热分解可得纯,下列有关说法正确的是________(填选项字母)。
A.NaN3与KN3结构类似,前者晶格能较小
B.晶体钾的晶胞结构如右图所示,每个晶胞中分摊2个钾原子
C.氮的第一电离能大于氧
D.氮气常温下很稳定,是因为氮的电负性小
(5)二氧化钛(TiO2)是常用的、具有较高催化活性和稳定性的光催化剂。O2在其催化作用下,可将CN-氧化成CNO-。CN-的电子式为________,CNO-的中心原子的杂化方式为____________。
(6)在CrCl3溶液中,一定条件下存在组成为(n和x均为正整数)的配离子,将其通过氢离子交换树脂(R-H),可发生离子交换反应:
将含0.0015mol的溶液,与R-H完全交换后,中和生成的需浓度为
0.1200 mol/LNaOH溶液25.00 mL,则该配离子的化学式为____________。
高二化学填空题困难题查看答案及解析
[化学-选修3:物质结构与性质]
铁、铜、铬、镍及其化合物在现代社会中的用途越来越广泛。
(1)铁在元素周期表中的位置是_____________,基态铁原子价电子排布式为___________。
(2)锂—磷酸氧铜电池正极的的活性物质是Cu4O(PO4)2,PO43-的空间构型是______________,P、S元素第一电离能大小关系为_______________。
(3)镍可与CO形成配合物Ni(CO)n,CO分子与N2互为等电子体,则中CO分子σ键与π键的个数比为________;该配合物的熔点是170℃,则Ni(CO)n 属于 _______晶体。
(4)在铬的摧化作用下,乙醇可被空气氧化为乙醛(CH3CHO),乙醛分子中碳原子的杂化方式是______,乙醇极易溶于水,其主要原因是_______________。
(5)立方NiO晶体结构类似于NaCl,则Ni2+的配位数为________,其晶胞边长为a cm,列式表示NiO晶体的密度为____g/cm3(不必计算出结果,阿伏加德罗常数的值为NA)。
高二化学填空题中等难度题查看答案及解析
具有下列电子层结构的原子或离子,其对应的元素在周期表中的位置说法正确的
A.最外层电子排布为1s2的原子和最外层电子排布为2s2的原子,所对应的两元素一定在同一主族
B.3p能级上有1个空轨道的原子和4p能级上有1空轨道的原子,所对应的两元素一定在同一主族
C.最外层电子排布为nsnnpn的原子和最外层电子排布为2s22p6的离子,所对应的两元素一定在同一周期
D.原子核外M层上的s能级和p能级都填满了电子,而d轨道上尚未有电子的两种原子,所对应的两元素一定在同一周期
高二化学选择题中等难度题查看答案及解析