-
(1)氨气的水溶液称为氨水,其中主要存在的溶质微粒是NH3·H2O。
已知: a.常温下,醋酸和NH3·H2O的电离平衡常数均为1.74×10-5;b.CH3COOH+NaHCO3=CH3COONa+CO2↑+H2O。则CH3COONH4溶液呈__(填“酸”“碱”或“中”,下同)性,NH4HCO3溶液呈__性,NH4HCO3溶液中物质的量浓度最大的离子是____(填化学式)。
(2)99 ℃时,KW=1.0×10-12,该温度下测得0.1 mol·L-1Na2A溶液的pH=6。
①H2A在水溶液中的电离方程式为_______________。
②该温度下,将0.01 mol·L-1H2A溶液稀释到20倍后,溶液的pH=____。
③体积相等、pH均为1的盐酸与H2A溶液分别与足量的Zn反应,产生的氢气__(填字母序号)。
A. 盐酸多 B.H2A多 C.一样多 D.无法确定
④将0.1 mol·L-1H2A溶液与0.2 mol·L-1氨水等体积混合,完全反应后溶液中各离子浓度从大到小的顺序为______________________。
高三化学解答题中等难度题查看答案及解析
-
(5分)氨气的水溶液称为氨水,它的主要存在微粒是NH3·H2O。已知:a.常温下,醋酸和NH3·H2O的电离平衡常数均为1.74×10-5mol/L b.CH3COOH+NaHCO3=CH3COONa+CO2↑+H2O
则CH3COONH4溶液呈________性(填“酸”、“碱”或“中”),NH4HCO3溶液呈________性(填“酸”、“碱”或“中”),NH4HCO3溶液中浓度最大的离子是________(填离子的化学式)。
高三化学填空题中等难度题查看答案及解析
-
已知常温下CH3COOH和NH3·H2O的电离平衡常数分别为Ka、Kb。若在常温下向0.1mol/L的醋酸溶液中逐滴加入相同浓度的氨水直至完全过量,则下列说法正确的是
A. 加入氨水的过程中,溶液的导电性一直不断增强
B. CH3COONH4在水溶液中的水解平衡常数Kh=Kw/(Ka+Kb)
C. 若Ka≈Kb,当加入等体积的氨水时,溶液基本呈中性
D. 该等式在滴加过程中始终成立c(CH3COO-)+c(CH3COOH)=c(NH4+)+c(NH3·H2O)
高三化学单选题困难题查看答案及解析
-
已知常温下CH3COOH和NH3·H2O的电离平衡常数分别为Ka、Kb。若在常温下向0.1mol/L的醋酸溶液中逐滴加入相同浓度的氨水直至完全过量,则下列说法正确的是
A. 加入氨水的过程中,溶液的导电性一直不断增强
B. CH3COONH4在水溶液中的水解平衡常数Kh=Kw/(Ka+Kb)
C. 若Ka≈Kb,当加入等体积的氨水时,溶液基本呈中性
D. 该等式在滴加过程中始终成立c(CH3COO-)+c(CH3COOH)=c(NH4+)+c(NH3·H2O)
高三化学单选题困难题查看答案及解析
-
常温下,pH=12的氨水中存在以下电离平衡:NH3·H2O
NH4++OH-.往其中加入少量 0.01mol·L-1NaOH
溶液,保持不变的是
A.c(OH-) B.c(NH4+) C.c(NH3·H2O) D.c(NH4+)·c(OH-)
高三化学选择题简单题查看答案及解析
-
常温下,pH=12的氨水中存在以下电离平衡:NH3•H2O⇌NH4++OH-.往其中加入少量0.01mol•L-1 NaOH溶液,保持不变的是( )
A.c(NH4+)
B.c(OH-)
C.c
D.c(NH4+)•c(OH-)高三化学选择题中等难度题查看答案及解析
-
已知常温时CH3COOH的电离平衡常数Ka=1.75×10−5,NH3·H2O的电离平衡常数Kb=1.75×10−5。常温时,向10 mL浓度均为0.01mol·L−1的NaOH和氨水混合溶液中,逐滴加入0.01mol·L−1的 CH3COOH 溶液,混合溶液的pH与加入CH3COOH的体积V之间的变化曲线如图所示,下列有关说法正确的是
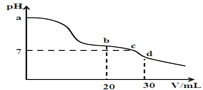
A. a 点溶液的pH<12
B. b 点时水的电离程度最大
C. c 点处的微粒间存在:c(CH3COO−)=c(NH4+)+c(NH3·H2O)
D. d 点处的微粒间存在:c(CH3COO−)>c(H+)>c(Na+)>c(NH4+)>c(OH−)
高三化学单选题困难题查看答案及解析
-
已知常温时CH3COOH的电离平衡常数Ka=1.75×10−5,NH3·H2O的电离平衡常数Kb=1.75×10−5。常温时,向10 mL浓度均为0.01mol·L−1的NaOH和氨水混合溶液中,逐滴加入0.01mol·L−1的 CH3COOH 溶液,混合溶液的pH与加入CH3COOH的体积V之间的变化曲线如图所示,下列有关说法正确的是

A. a 点溶液的pH<12
B. b 点时水的电离程度最大
C. c 点处的微粒间存在:c(CH3COO−)=c(NH4+)+c(NH3·H2O)
D. d 点处的微粒间存在:c(CH3COO−)>c(H+)>c(Na+)>c(NH4+)>c(OH−)
高三化学单选题困难题查看答案及解析
-
常温下,向1L0.1mol·L-1一元酸HR溶液中逐渐通入氨气[已知常温下NH3·H2O电离平衡常数K=1.76×10-5],使溶液温度和体积保持不变,混合溶液的pH与离子浓度变化的关系如图所示。下列叙述正确的是
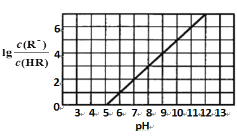
A. 0.1mol·L-1HR溶液的pH为5
B. HR为弱酸,常温时随着氨气的通入,c(R-)/[c(OH-).c(HR)] 逐渐增大
C. 当通入0.1 mol NH3时,c(NH4+)>c(R-)>c(OH-)>c(H+)
D. 当c(R-)= c(HR)时,溶液必为中性
高三化学单选题困难题查看答案及解析
-
常温下,向1L 0.1mol·L−1一元酸HR溶液中逐渐通入氨气(已知常温下NH3·H2O电离平衡常数K=1.76×10-5),使溶液温度和体积保持不变,混合溶液的pH与离子浓度变化的关系如图所示。下列叙述正确的是
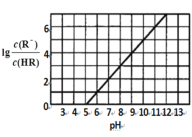
A.当c(R-)=c(HR)时,溶液必为中性
B.0.1mol·L-1HR溶液的pH为5
C.HR为弱酸,常温时随着氨气的通入,
逐渐增大
D.当通入0.1 mol NH3时,c(NH4+)>c(R-)>c(OH-)>c(H+)
高三化学单选题中等难度题查看答案及解析