-
X、Y、Z、M、W、N六种元素的原子序数依次增大,其中X、Y、Z、M、W为五种短周期元素。X元素的某种核素无中子,W原子核外电子数是M原子最外层电子数的2倍,Y、Z、M、W在周期表中的相对位置如图所示,N是用量最多的金属元素。下列说法不正确的是
Y
Z
M
W
A. 原子半径:W>Y>Z>M>X
B. N的一种氧化物可用作油漆和涂料
C. 热稳定性:XM>X2Z
D. X2Z、WM4分子中各原子最外层均为8电子稳定结构
高二化学选择题中等难度题查看答案及解析
-
X、Y、Z、M、W、N六种元素的原子序数依次增大,其中X、Y、Z、M、W为五种短周期元素。X元素的某种核素无中子,W原子核外电子数是M原子最外层电子数的2倍,Y、Z、M、W在周期表中的相对位置如图所示,N是用量最多的金属元素。下列说法不正确的是
Y
Z
M
W
A.原子半径:W>Y>Z>M>X
B.N的一种氧化物可用作油漆和涂料
C.氢化物的沸点:Z小于M
D.工业上制备W单质的方法为电解熔融的W的氧化物
高二化学单选题困难题查看答案及解析
-
短周期元素M、W、X、Y、Z的原子序数依次增大,M元素的一种核素没有中子,且M、W、X、Y+、Z的最外层电子数与其电子层数的比值依次为1、2、3、4、2(不考虑零族元素),下列关于这些元素的叙述正确的是( )
A. X分别和其它四种元素均可形成至少2种化合物
B. M分别和w、X、Y、Z形成化合物,均显相同化合价
C. M、X、Z三种元素组成的化合物含有离子键
D. M、X、Y组成化合物和Y、Z组成化合物,它们所含的化学键类型完全相同
高二化学选择题中等难度题查看答案及解析
-
短周期元素W、X、Y、Z、M的原子序数依次增大,元素W的一种核素的中子数为0,X的原子最外层电子数是次外层的2倍,Z与M同主族,Z2−电子层结构与氖相同。
(1)M位于元素周期表中第______周期______族。
(2)化合物p由W、X、Y、M四种元素组成。已知向p溶液中加入FeCl3溶液,溶液变血红色;向p溶液中加入NaOH溶液并加热可放出使湿润的红色石蕊试纸变蓝的气体。p的化学式为_________。
(3)由X、Y、Z三种元素可组成摩尔质量为84g/mol的物质q,且q分子中三种元素的原子个数之比为1:1:1。已知q分子中各原子均达到8电子稳定结构,且分子中不含双键,但含极性键和非极性键,q分子的结构式为_______________。
(4) (XY)2的性质与Cl2相似,(XY)2与NaOH溶液反应的离子方程式为_________。
高二化学综合题中等难度题查看答案及解析
-
A、B、C、D是原子序数依次增大的四种短周期主族元素,其相关信息如下表所示
元素代号
元素相关信息
A
原子核内无中子,核外只有1个电子
B
其单质是空气中含量最多的气体
C
最外层电子数是电子层数的3倍
D
短周期中原子半径最大的元素
试回答下列问题:
(1)写出下列元素名称:A________, C________
(2)B在元素周期表中的位置:第____周期,第_____族。
(3)B、C两种元素的气态氢化物的稳定性强弱为:_____>______(填化学式)。
(4)A、C、D三种元素可以形成离子化合物,该化合物的电子式为_____________。
(5)写出C与D形成的淡黄色化合物的用途(填一种即可)___________________。
高二化学推断题简单题查看答案及解析
-
W、X、Y、Z是四种短周期主族元素,原于序数依次增大,W的一种原子核内无中子,X、Y原子核外 L电子层的电子数之比为3:4,Y, Z位于同一周期,Z的一种单质常温下是淡黄色晶体,四种元素的原子最 外层电子数之和为14。下列说法错误的是()
A. X与其它三种元素均能形成二种二元化合物
B. X、Z阴离子的还原性强弱:Z>X
C. X、Y的简单离子半径大小:X>Y
D. X和Z的简单氢化物沸点;X<Z
高二化学单选题中等难度题查看答案及解析
-
短周期元素W、U、Q、R的原子序数依次增大,W元素的一种原子无中子,U与R同主族、与Q同周期,Q是地壳中含量最多的非金属元素,R元素原子的最外层电子数是内层电子数的0.4倍,下列有叙述正确的是( )
A.UQ2与RQ2的化学键类型和分子结构相同
B.RQ2为酸性氧化物,可以与强碱反应,但不能与任何酸反应
C.UW4与UQ2均为只含极性键的非极性分子
D.常温下R的单质很稳定,既不与酸反应,也不与强碱反应
高二化学单选题中等难度题查看答案及解析
-
(11分)现有A、B、C、D、E、F、G七种位于周期表前四周期元素,其原子序数依次增大,相关信息如下表所示:
元素
性质
A
一种核素的原子核内不含中子
B
原子核外电子有6种不同运动状态
C
最高价氧化物的水化物与其氢化物可发生非氧化还原反应
D
单质之一为淡蓝色气体,可阻挡对人体有害的紫外线
E
在地壳中的含量位居第三
F
周期表中位于短周期,基态原子M层成对电子数是未成对电子数的2倍
G
该元素的一种氧化物M可用作油漆颜料,与E的单质反应可应用于焊接钢轨
根据以上信息,回答下列问题:
(1)画出元素C的基态原子核外电子排布图: ;G元素位于周期表的 区;
B、C、D三种元素的第一电离能由大到小顺序为: (用元素符号表示)。
(2)化合物BA2D2蒸气293 K时,理论测算密度为2.0g·L-1,实际密度为2.5 g·L-1的原因是 。
(3)FD2中F原子的杂化类型为 ;分子空间构型为 ;FD2易溶于水的原因可能是: (填入序号)。①FD2与水极性相同 ②FD2可以与水反应
(4)有人推测化合物CA5的存在,该化合物中含有化学键的可能类型为:
高二化学填空题困难题查看答案及解析
-
(11分)现有A、B、C、D、E、F六种位于周期表前四周期元素,其原子序数依次增大,相关信息如下表所示:
元素
性质
A
一种核素的原子核内不含中子
B
原子核外电子有6种不同运动状态
C
最高价氧化物的水化物与其氢化物可发生非氧化还原反应
D
单质之一为淡蓝色气体,可阻挡对人体有害的紫外线
E
周期表中位于短周期,基态原子M层成对电子数是未成对电子数的2倍
F
该元素的一种氧化物M可用作油漆颜料,与某单质反应可应用于焊接钢轨
根据以上信息,回答下列问题:
(1)画出元素C的基态价电子排布图: ;F元素位于周期表的__ 区;B、C、D三种元素的第一电离能由大到小顺序为: (用元素符号表示)。
(2)化合物BA2D2蒸气293 K时,理论测算密度为2.0g·L-1,实际密度为2.5 g·L-1的原因是 。
(3)ED2中F原子的杂化类型为 ; ED2易溶于水的原因可能是: (填入序号)。
①ED2与水极性相同
②ED2可以与水反应
(4)有人推测化合物CA5的存在,该化合物中含有化学键的可能类型为: 。
高二化学填空题困难题查看答案及解析
-
现有A、B、C、D、E、F六种位于周期表前四周期的元素,其原子序数依次增大,相关信息如下表所示:
元素
性质
A
一种核素的原子核内不含中子
B
原子核外电子有6种不同运动状态
C
最高价氧化物的水化物与其氢化物可生成盐
D
单质之一为淡蓝色气体,可阻挡对人体有害的紫外线
E
周期表中位于短周期,基态原子M层成对电子数是未成对电子数的2倍
F
该元素的一种氧化物可用作油漆颜料,与某单质反应可应用于焊接钢轨
根据以上信息,回答下列问题:
(1)F元素位于周期表的____区(填s、p、d、ds或f),B、C、D三种元素的第一电离能由大到小顺序为______________________(用元素符号表示)。
(2)ED2中E原子的杂化类型为__________________;ED2易溶于水的原因可能是___________(填序号)。
①ED2与水极性相同 ②ED2可以与水反应 ③ED2可以与水形成氢键
(3)F元素的一种氯化物常温下为固体,熔点282℃,沸点315℃,在300℃以上易升华,易溶于水,也易溶于乙醚、丙酮等有机溶剂,据此判断该氯化物晶体为________晶体。
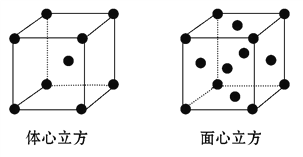
(4)F的单质晶体在不同温度下有两种堆积方式(晶胞结构如图所示),面心立方晶胞和体心立方晶胞中实际含有的F原子个数之比为________,其中体心立方晶胞空间利用率为___________(设F原子半径是r,列出含r的计算表达式,不需化简)。
高二化学综合题中等难度题查看答案及解析