-
碱式次氯酸镁[Mg2ClO(OH)3·H2O]微溶于水,不吸湿,相对稳定,是一种有开发价值的无机抗菌剂。某研发小组通过下列流程制备碱式次氯酸镁:

(1)从上述流程中可以判断,滤液中可回收的主要物质是__________。
(2)NaClO溶液用Cl2与NaOH溶液反应获得,写出该反应的化学方程式:_____。
(3)有效氯的含量是衡量次氯酸盐氧化能力的重要指标。次氯酸盐的有效氯含量可用次氯酸盐与盐酸反应所生成的氯气的含量来表示:ClO-+Cl-+2H+=Cl2↑+H2O ,若测得某碱式次氯酸镁产品中镁含量为29.01%,有效氯含量为40.28%。
,若测得某碱式次氯酸镁产品中镁含量为29.01%,有效氯含量为40.28%。
①通过计算判断该产品中镁和有效氯含量的测定值与理论值相比,是偏高或偏低?(写出计算过程)_____________
②根据你的判断,推测产品中可能含有的杂质,并给出制备过程能减少产品中含有该杂质的措施_____________
-
碱式氯化铜是重要的无机杀菌剂。
(1)碱式氯化铜有多种制备方法
①方法1:45 ~ 50℃时,向CuCl悬浊液中持续通入空气得到Cu2 (OH)2 Cl2·3H2O,该反应的化学方程式为_____________。
②方法2:先制得CuCl2,再与石灰乳反应生成碱式氯化铜。Cu与稀盐酸在持续通入空气的条件下反应生成CuCl2,Fe3+对该反应有催化作用,其催化原理如图所示。M'的化学式为______。

(2)碱式氯化铜有多种组成,可表示为Cua(OH)bClc·xH2O。为测定某碱式氯化铜的组成,进行下列实验:
①称取样品2.2320g,用少量稀HNO3溶解后配成100.00mL溶液A;
②取25. 00mL溶液A,加入足量AgNO3溶液,得AgCl 0. 3444g;
③另取25. 00mL溶液A,调节pH 4 ~ 5,用浓度为0.08000mol·L-1的EDTA(Na2H2Y·2H2O)标准溶液滴定Cu2+ (离子方程式为Cu2++ H2Y2-=CuY2-+2H+),滴定至终点,消耗标准溶液60.00mL。通过计算确定该样品的化学式(写出计算过程)。_____________
-
下列反应的离子方程式书写正确的是( )
A.钠和水反应:Na+H2O=Na++OH-+H2↑
B.磁性氧化铁溶于盐酸:Fe3O4+8H+=3Fe3++4H2O
C.将氯气溶于水制备次氯酸:Cl2+H2O=H++Cl-+HClO
D.盐酸与碳酸钙反应制备二氧化碳:CO32-+2H+=CO2↑+H2O
-
下列实验设计及其对应的离子方程式均正确的是
A.Na2O2与H2O反应制备O2:Na2O2+H2O=2 Na++2OH-+ O2↑
B.将氯气溶于水制备次氯酸:Cl2+H2O=2H+ + Cl-+ ClO-
C.用FeCl3溶液腐蚀铜线路板:Cu+2Fe3+= Cu2++2Fe2+
D.用浓盐酸酸化的KMnO4溶液与SO2反应,证明SO2具有还原性:2MnO4-+ SO2+2H2O=2Mn2+ +5 SO42-+4 H+
-
下列离子方程式正确的是
A. 将氯气溶于水制备次氯酸:Cl2+H2O═2H++Cl-+ClO-
B. 碳酸钙与稀盐酸反应:CO32-+2H+=H2O+CO2↑
C. 硫酸铝和氨水反应:Al3++3OH-=Al(OH)3↓
D. Na与H2O反应:2Na+2H2O=2Na++2OH-+H2↑
-
下列表示对应化学反应的离子方程式正确的是
A.Na2O2溶于水产生O2:Na2O2+H2O═2Na++2OH-+O2↑
B.Fe(OH)3溶于氢碘酸:Fe(OH)3+3H+=Fe3++3H2O
C.次氯酸钙溶液中通入过量二氧化碳:Ca2++2ClO-+H2O+CO2=CaCO3↓+2HClO
D.将一定量的Al片投入足量的NaOH溶液中:2Al+2OH-+2H2O =2AlO2-+3H2↑
-
(2015秋•湖州期末)亚氯酸盐在工业上有许多用途,常见的亚氯酸钠、亚氯酸镁、亚氯酸钡均易溶于水,亚氯酸盐在酸中不稳定,可生成Cl2、ClO2和H2O.用二氧化氯(ClO2)可制备用途广泛的亚氯酸钠(NaClO2),实验室可用下列装置(略去部分夹持仪器)制备少量的亚氯酸钠.
装置C中发生反应:2NaClO3+SO2═2ClO2+Na2SO4 (Ⅰ)
装置D中发生反应:2ClO2+H2O2+2NaOH═2NaClO2+2H2O+O2 (Ⅱ)
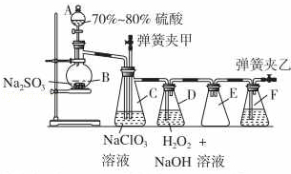
(1)仪器组装完毕,关闭两个弹簧夹,打开A中活塞,向A中注入水可检验装置气密性,装置气密性良好的现象是 .F中盛有的液体为 .
(2)装置E的作用是 .
(3)在碱性溶液中NaClO2比较稳定,所以装置D中应维持NaOH稍过量,判断NaOH是否过量所需要的试剂是 .
a.稀盐酸 b.品红溶液 c.石蕊溶液 d.酚酞溶液
(4)一次实验制备中,通过检验发现制备的NaClO2中含有NaOH、Na2SO3,出现这些杂质的可能原因是 .检验产物中含有Na2SO3杂质所用的试剂是 .(供选择的试剂有:Ba(OH)2溶液、H2O2溶液、AgNO3溶液、品红溶液、H2SO4溶液)
-
(1)以下反应:①木炭与水制备水煤气,②氯酸钾分解,③炸药爆炸,④酸与碱的中和反应,⑤生石灰与水作用制熟石灰,⑥Ba(OH)2•H2O 与 NH4Cl ,⑦浓硫酸溶于水, 属于放热反应__________.(填序号)
(2)Mg-Al-NaOH 电池中的负极反应:___________.
(3)FeCl3 溶液常用于腐蚀印刷电路铜板,发生 2FeCl3+Cu=2FeCl2+CuCl2,若将 此反应设计成原电池,则负极所用电极材料为___________,当线路中转移 0.2mol 电 子时,则被腐蚀铜的质量为___________g.
(4)已知拆开 1mol H-H 键、1mol N≡N、1mol N-H 键分别需要吸收的能量为 436kJ、946k J、391k J.则由 N2 和 H2 反应生成 1mol NH3 需要放出___________的热量。
(5)用序号回答:①HCl ②NaOH ③Cl2 ④H2O ⑤NH4Cl ⑥P4 ⑦NH3•H2O ⑧Na2O2 ⑨HClO⑩CaO⑪HF⑫MgCl2
属于共价化合物的是___________,存在非极性键的是___________。
-
关于卤素(用X表示)的下列叙述中正确的为( )
A. 卤素单质与水反应的通式为X2+H2O= HX+HXO
B. HX都极易溶于水,它们的热稳定性随核电荷数增大而增强
C. 卤素单质的颜色随相对分子质量增大的顺序不断加深
D. X-的还原性随卤素的核电荷数增大而增强,核电荷数小的卤素单质可将核电荷数大的卤素从它的盐溶液里置换出来
-
关于卤素(用X表示)的下列叙述正确的是( )
A.卤素单质与水反应均可用X2+H2O=HXO+HX表示
B.HX都极易溶于水,它们的热稳定性随核电荷数增加而增强
C.卤素单质的颜色从F2→I2按相对分子质量增大而加深
D.X-的还原性依次为F-<Cl-<Br-<I-,因此相对分子质量小的卤素单质可将相对分子质量大的卤素从它的盐溶液里置换出来

 ,若测得某碱式次氯酸镁产品中镁含量为29.01%,有效氯含量为40.28%。
,若测得某碱式次氯酸镁产品中镁含量为29.01%,有效氯含量为40.28%。
