-
下列热化学方程式中的 △ H 能表示物质燃烧热的是 ( )
A. 2CO(g)+O2(g)=2CO2(g) △H=-556kJ·mol-1
B. CH4(g)+2O2(g)=CO2(g)+2H2O(l) △H=-890kJ·mol-1
C. 2H2(g)+O2(g)=2H2O(l) △H=-571.6kJ·mol-1
D. H2(g)+Cl2(g)=3HCl(g) △H=-184.6kJ·mol-1
高二化学选择题中等难度题查看答案及解析
-
下列热化学方程式中的 △ H 能表示物质燃烧热的是 ( )
A.2CO(g)+O2(g)=2CO2(g) △H=-556kJ·mol-1
B.CH4(g)+2O2(g)=CO2(g)+2H2O(l) △H=-890kJ·mol-1
C.2H2(g)+O2(g)=2H2O(l) △H=-571.6kJ·mol-1
D.H2(g)+Cl2(g)=3HCl(g) △H=-184.6kJ·mol-1
高二化学单选题简单题查看答案及解析
-
下列热化学方程式中,△H能正确表示物质的燃烧热的是
A.2CO(g) +O2(g) ==2CO2(g) △H=—566.0 kJ/mol
B.C(s) +1/2O2(g) ==CO(g) △H=—110.5 kJ/mol
C. CH4(g) +2O2(g)== CO2(g)+2H2O(l) △H=—890.31 kJ/mol
D. 2C8H18(l) +25O2(g)==16CO2(g)+18H2O(l) △H=—11036 kJ/mol
高二化学选择题简单题查看答案及解析
-
下列热化学方程式中,△H能正确表示物质的燃烧热的是
A.2CO(g) +O2(g) ==2CO2(g) △H=—566.0 kJ/mol
B.C(s) +1/2O2(g) ==CO(g) △H=—110.5 kJ/mol
C.CH4(g) +2O2(g)== CO2(g)+2H2O(l) △H=—890.31 kJ/mol
D.2C8H18(l) +25O2(g)==16CO2(g)+18H2O(l) △H=—11036 kJ/mol
高二化学选择题中等难度题查看答案及解析
-
下列热化学方程式中,△H能正确表示物质的燃烧热的是
A.2CO(g) +O2(g) =2CO2(g) △H=-566.0 kJ/mol
B.C(s) +1/2O2(g) =CO(g) △H=-110.5 kJ/mol
C.CH4(g) +2O2(g)=CO2(g)+2H2O(l) △H=-890.31 kJ/mol
D.2C8H18(l) +25O2(g)=16CO2(g)+18H2O(l) △H=-11036 kJ/mol
高二化学选择题简单题查看答案及解析
-
下列热化学方程式中的△H能表示物质燃烧热的是
A.2CO(g)+O2(g)═2CO2(g)△H=﹣56kJ/mol
B.CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H=﹣890kJ/mol
C.2H2(g)+O2(g)═2H2O(l)△H=﹣571.6kJ/mol
D.H2(g)+Cl2(g)═2HCl(g)△H=﹣183kJ/mol
高二化学选择题中等难度题查看答案及解析
-
下列热化学方程式中的ΔH能表示物质燃烧热的是(假设数据均正确)
A. C2H5OH(l)+3O2(g)=2CO2(g)+3H2O(g) ΔH=+1 367 kJ·mol-1
B. 2CO (g)+O2(g)=2CO2(g) ΔH=-566 kJ·mol-1
C. H2 (g)+1/2O2(g)= H2O(g ) ΔH=-285.8 kJ·mol-1
D. S(s)+O2(g)=SO2(g) ΔH=-296.95 kJ·mol-1
高二化学单选题简单题查看答案及解析
-
(1)已知常温常压下:
①CH3OH(l)+O2(g)═CO(g)+2H2O(g) △H=-359.8kJ·mol-1
②2CO(g)+O2(g)=2CO2(g) △H=-556.0kJ·mol-1
③H2O(g)=H2O(l) △H=-44.0kJ·mol-1
写出体现甲醇燃烧热的热化学方程式为________________________________。
(2)某温度时,将2 mol CO与5 mol H2的混合气体充入容积为2 L的密闭容器中,在催化剂的作用下发生反应:CO(g)+2H2(g)
CH3OH(g)。
①经过5 min后,反应达到平衡,此时转移电子6 mol。该反应的平衡常数为________。v(H2)=________ mol/(L·min)。若保持体积不变,再充入2 mol CO和1.5 mol CH3OH,此时v(正)________v(逆)(填“>”“<”或“=”)。
②在其他条件不变的情况下,再增加2 mol CO与5 mol H2,达到新平衡时,CO的转化率________(填“增大”“减小”或“不变”)。
③下列不能说明该反应已达到平衡状态的是________。
a.CH3OH的质量不变 b.混合气体的平均相对分子质量不再改变 c.v逆(CO)=2v正(H2) d.混合气体的密度不再发生改变
高二化学综合题困难题查看答案及解析
-
下列过程都与热量变化有关,其中表述不正确的是( )
A.CO(g)的燃烧热是283.0 kJ/mol,则表示CO(g)燃烧反应的热化学方程式为:2CO (g)+O2(g)═2CO2 (g)△H=-586.0 kJ/mol
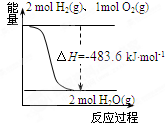
B.如图表示H2与O2发生反应过程中的能量变化,则H2的燃烧热为483.6 kJ•mol-1
C.铝热反应是放热反应,可用于铁单质的冶炼
D.焓变△H>0的化学反应发生时,不一定都需要特殊的温度条件高二化学选择题中等难度题查看答案及解析
-
悉尼奥运会所用火炬燃料为65%丁烷(C4H10)和35%丙烷,已知下列物质燃烧的热化学方程式为: CO:2CO(g)+O2(g)=2CO2(g);△H=-566.0kJ/mol.
丙烷:C3H8(g)+5O2(g)=3CO2(g)+4H2O(l);△H=-2221.5kJ/mol.
正丁烷:C4H10(g)+6.5O2(g)=4CO2(g)+5H2O(l);△H=-2878.0kJ/mol.
异丁烷:C4H10(g)+6.5O2(g)=4CO2(g)+5H2O(l);△H=-2869.6kJ/mol.
下列有关说法正确的是
A.等物质的量正丁烷比异丁烷能量低
B.相同质量的丙烷和正丁烷分别完全燃烧,前者需要的氧气多,产生的热量也多
C.常温下,CO的燃烧热为566.0 kJ/mol
D.人类利用的能源都是通过化学反应获得的
高二化学选择题中等难度题查看答案及解析