-
乙烯是重要的有机化工原料,可由乙醇脱水制备。涉及反应如下:
①2CH3OH(g) CH3OCH3(g)+ H2O(g) △H1=—23.9 kJ•mol-1
CH3OCH3(g)+ H2O(g) △H1=—23.9 kJ•mol-1
②2CH3OH(g) C2H4(g)+2H2O(g) △H2= —29.1kJ•mol-1
C2H4(g)+2H2O(g) △H2= —29.1kJ•mol-1
③CH3CH2OH(g) CH3OCH3(g) △H3= +50.7kJ•mol-1
CH3OCH3(g) △H3= +50.7kJ•mol-1
④C2H5OH(g) C2H4(g)+ H2O(g) △H4=akJ•mol-1
C2H4(g)+ H2O(g) △H4=akJ•mol-1
回答下列问题:
(1)a=___________。
(2)在1.0L密闭容器中放入0.10 mol C2H5OH(g),在一定温度下进行④反应,反应时间(t)与容器内气体总压强(P)的数据见下表:
| 时间t/h | 0 | 1 | 2 | 4 | 8 | 16 | 20 | 25 | 30 |
| 总压强P/100kPa | 4.91 | 5.58 | 6.32 | 7.31 | 8.54 | 9.50 | 9.52 | 9.53 | 9.53 |
①欲提高C2H5OH的平衡转化率,应采取的措施为___________(填字母)。
a.升高温度 b.增大压强
c.通入乙醇 d.降低压强
②由总压强P和起始压强P0计算反应物C2H5OH的转化率(C2H5OH)的表达式为_________,平衡时C2H5OH的转化率为_______(结果保留两位有效数字,下同),该反应的平衡常数K=_________。
③用总压强P和起始压强P0表示反应体系的总物质的量n(总)和反应物C2H5OH的物 质的量n(C2H5OH),n(总)=_____mol,n(C2H5OH)=_____mol。
(3)下表为反应④中反应物浓度与反应时间的数据,分析该反应中c(C2H5OH)变化与时间间隔(△t)的规律,得出的结论是______,由此规律推出反应在12h时c(C2H5OH)等于______mol•L-1
| 反应时间t/h | 0 | 4 | 8 | 16 |
| c(C2H5OH)/(mol•L-1) | 0.10 | 0.051 | 0.026 | 0.0065 |
-
乙烯是重要的有机化工原料,可由乙醇脱水制备。涉及反应如下:
①2CH3OH(g) CH3OCH3(g)+ H2O(g) △H1=—23.9 kJ•mol-1
CH3OCH3(g)+ H2O(g) △H1=—23.9 kJ•mol-1
②2CH3OH(g) C2H4(g)+2H2O(g) △H2= —29.1kJ•mol-1
C2H4(g)+2H2O(g) △H2= —29.1kJ•mol-1
③CH3CH2OH(g) CH3OCH3(g) △H3= +50.7kJ•mol-1
CH3OCH3(g) △H3= +50.7kJ•mol-1
④C2H5OH(g) C2H4(g)+ H2O(g) △H4=akJ•mol-1
C2H4(g)+ H2O(g) △H4=akJ•mol-1
回答下列问题:
(1)a=___________。
(2)在1.0L密闭容器中放入0.10 mol C2H5OH(g),在一定温度下进行④反应,反应时间(t)与容器内气体总压强(P)的数据见下表:
| 时间t/h | 0 | 1 | 2 | 4 | 8 | 16 | 20 | 25 | 30 |
| 总压强P/100kPa | 4.91 | 5.58 | 6.32 | 7.31 | 8.54 | 9.50 | 9.52 | 9.53 | 9.53 |
①欲提高C2H5OH的平衡转化率,应采取的措施为___________(填字母)。
a.升高温度 b.增大压强
c.通入乙醇 d.降低压强
②由总压强P和起始压强P0计算反应物C2H5OH的转化率(C2H5OH)的表达式为_________,平衡时C2H5OH的转化率为_______(结果保留两位有效数字,下同),该反应的平衡常数K=_________。
③用总压强P和起始压强P0表示反应体系的总物质的量n(总)和反应物C2H5OH的物 质的量n(C2H5OH),n(总)=_____mol,n(C2H5OH)=_____mol。
(3)下表为反应④中反应物浓度与反应时间的数据,分析该反应中c(C2H5OH)变化与时间间隔(△t)的规律,得出的结论是______,由此规律推出反应在12h时c(C2H5OH)等于______mol•L-1
| 反应时间t/h | 0 | 4 | 8 | 16 |
| c(C2H5OH)/(mol•L-1) | 0.10 | 0.051 | 0.026 | 0.0065 |
-
乙醇是重要的有机化工原料,可由乙烯水合法生产,反应的化学方程式如下:C2H4(g)+ H2O(g) C2H5OH(g),下图为乙烯的平衡转化率与温度(T)、压强(P)的关系[起始n(C2H4)∶n(H2O) =1∶1]。下列有关叙述正确的是
C2H5OH(g),下图为乙烯的平衡转化率与温度(T)、压强(P)的关系[起始n(C2H4)∶n(H2O) =1∶1]。下列有关叙述正确的是
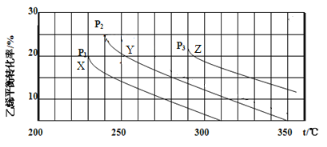
A. Y对应的乙醇的质量分数为1/9
B. X、Y、Z对应的反应速率:υ(X) > υ(Y) > υ(Z)
C. X、Y、Z对应的平衡常数数值:KX > KY > KZ
D. 增大压强、升高温度均可提高乙烯的平衡转化率
-
现代化学工业中,有机原料的主要来源为石油的裂化、裂解、重整产物、部分已经学习过的反应如下。
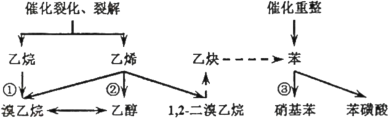
(1)请写出反应①由乙烷制备溴乙烷的化学反应方程式___;
(2)请写出反应②由乙烯制备乙醇的化学反应方程式___;
(3)请写出反应③由苯制备硝基苯的化学反应方程式___。
-
实验室制备1,2-二溴乙烷的反应原理是先用乙醇制备出乙烯,再将乙烯通入溴水中发生如下反应: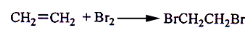 。可能存在的主要副反应有:乙醇在浓硫酸的存在下在l40℃脱水生成乙醚。用少量的溴和足量的乙醇制备1,2—二溴乙烷的装置如图所示。回答下列问题:
。可能存在的主要副反应有:乙醇在浓硫酸的存在下在l40℃脱水生成乙醚。用少量的溴和足量的乙醇制备1,2—二溴乙烷的装置如图所示。回答下列问题: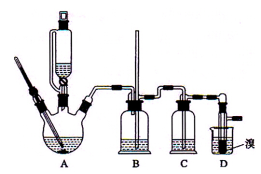
(1)写出装置A中制备乙烯的化学方程式 ;
(2)实验开始要尽可能快地把反应温度提高到170℃,其最主要目的是____(填正确选项前的字母);
A.引发反应 B.加快反应速度 C.防止乙醇挥发 D.减少副产物乙醚生成
(3)在装置C中应加入_____ (填正确选项前的字母),其目的是吸收反应中可能生成的酸性气体;
A.水 B.浓硫酸 C.氢氧化钠溶液 D.饱和碳酸氢钠溶液
(4)将1,2-二溴乙烷粗产品置于分液漏斗中加水,振荡后静置,产物应在________层(填“上”、“下”);
(5)若产物中有少量未反应的Br2,最好用_________洗涤除去 (填正确选项前的字母)。
A.水 B.氢氧化钠溶液 C.碘化钠溶液 D.乙醇
(6)装置B的作用有两个,分别是检查实验进行时试管D是否发生堵塞和_____________。
-
溴乙烷是一种重要的有机化工原料,其沸点为38.4℃。制备溴乙烷的一种方法是乙醇与氢溴酸反应,实际通 常是用溴化钠与一定浓度的硫酸和乙醇反应。某课外小组欲在 实验室制备溴乙烷的装置如图,实验操作步骤如下:
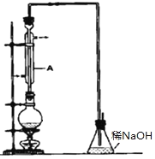
①检查装置的气密性;②在圆底烧瓶中加入 95%乙醇、80% 硫酸,然后加入研细的溴化钠粉末和几粒碎瓷片;③小心加热, 使其充分反应。请回答下列问题。
(1)装置 A 的作用是_____。
(2)反应时若温度过高,则有 SO2 生成,同时观察到还有一种红棕色气体产生,该气体的分子式是_____。
(3)反应结束后,得到的粗产品呈棕黄色。为了除去粗产品中的杂质,可选择下列试剂中 的_________(填写上正确选项的字母)。
a 亚硫酸钠溶液 b 乙醇 c 四氯化碳
该实验操作中所需的主要玻璃仪器是______。(填仪器名称)。
(4)要进一步制得纯净的溴乙烷,可继续用蒸馏水洗涤,分液后,再加入无水 CaCl2,然后进行的实验操作是__________。(填写正确选项的字母)。
a 分液 b 蒸馏 c 萃取
(5)为了检验溴乙烷中含有溴元素,不能直接向溴乙烷中滴加硝酸银溶液来检验,其原因 是_________。通常采用的方法是取少量溴乙烷,然后_____(按 实验的操作顺序选填下列序号)。
①加热 ②加入 AgNO3 溶液 ③加入稀 HNO3 酸化 ④加入 NaOH 溶液
-
溴乙烷是一种重要的有机化工原料,其沸点为38.4℃。制备溴乙烷的一种方法是乙醇与氢溴酸反应.某课外小组欲在实验室制备溴乙烷的装置如图,实验操怍步骤如下:
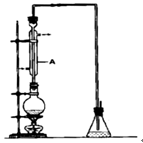
①检查装置的气密性;
②在圆底烧瓶中加入95%乙醇、溴化钠、浓硫酸及几粒碎瓷片;
③小心加热,使其充分反应。
请问答下列问题。
(1)装置A的作用是 。
(2)反应结束后,得到的粗产品呈棕黄色(含少量的溴单质)。为了除去粗产品中的杂质,可选择下列试剂中的 (填写上正确选项的字母)。
a.亚硫酸钠溶液 b.氢氧化钠溶液
c.乙醇 d.四氯化碳
该实验操作中所需的主要玻璃仪器是 (填仪器名称)。
(3)要进一步制得纯净的溴乙烷,可继续用蒸馏水洗涤,分液后,再加入无水 ,然后进行的实验操作是 (填写正确选项的字母)。
,然后进行的实验操作是 (填写正确选项的字母)。
a.分液 b.蒸馏 c.萃取
(4)为了检验溴乙烷中含有溴元素,通常采用的方法是取少量溴乙烷,然后 (按实验的操作顺序选填下列序号)。
①加热 ②加入 溶液 ③加入稀
溶液 ③加入稀 酸化 ④加入NaOH溶液
酸化 ④加入NaOH溶液
-
实验室用乙醇制备1,2-二溴乙烷的反应原理如下:①乙醇在浓硫酸的存在下制取乙烯、②乙烯与溴反应制得1,2-二溴乙烷。可能存在的主要副反应有:乙醇在浓硫酸的存在下在l40℃脱水生成乙醚。用少量的溴和足量的乙醇制备1,2-二溴乙烷的装置如图所示,有关数据列表如下:
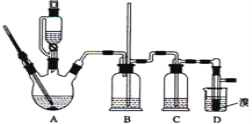
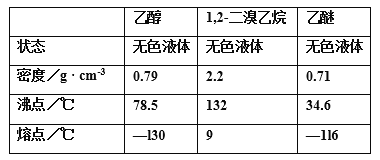
回答下列问题:
(1)写出乙醇在浓硫酸的存在下制取乙烯的化学方程式______________;浓硫酸所起的作用是___________ 。
(2)在此制各实验中,要尽可能迅速地把反应温度提高到170℃左右,其最主要目的是_______;(填正确选项前的字母)
a.引发反应 b.加快反应速度 c.防止乙醇挥发 d.减少副产物乙醚生成
(3)反应一段时间后三颈烧瓶A中的液体混合物会逐渐变黑,此时会发生另一个副反应生成其他酸性杂质气体,该反应的化学方程式为_________ 。
(4)在装置C中应加入______,其目的是吸收反应中可能生成的酸性气体:(填正确选项前的字母)
a.水 b.浓硫酸 c.氢氧化钠溶液 d.饱和碳酸氢钠溶液
(5)判断该制备反应已经结束的最简单方法是________________;
(6)若产物中有少量副产物乙醚,可用_____________的方法除去;
(7)反应过程中应用冷水冷却装置D,其主要目的是________________;但又不能过度冷却(如用冰水),其原因是___________________。
-
甲醇作为基本的有机化工产品和环保动力燃料具有广阔的应用前景,CO2加氢合成甲醇是合理利用CO2的有效途径。由CO2制备甲醇过程可能涉及反应如下:
反应Ⅰ:CO2(g)+H2(g)  CO(g)+H2O(g) ΔH1=+41.19 kJ·mol-1
CO(g)+H2O(g) ΔH1=+41.19 kJ·mol-1
反应Ⅱ:CO(g)+2H2(g)  CH3OH(g) ΔH2
CH3OH(g) ΔH2
反应Ⅲ:CO2(g)+3H2g)  CH3OH(g)+H2O(g) ΔH3=-49.58 kJ·mol-1
CH3OH(g)+H2O(g) ΔH3=-49.58 kJ·mol-1
回答下列问题:
(1)反应Ⅰ、Ⅱ、Ⅲ的化学平衡常数分别为K1、K2、K3、则K3=__________(用K的代数式表示)
(2)在恒压密闭容器中,充入一定量的 H2 和 CO2(假定仅发生反应Ⅲ),实验测得反应物在不同温度下,反应体系中 CO2 的平衡转化率与压强的关系曲线如图 1 所示。
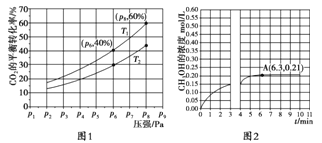
①比较 T1 与 T2 的大小关系:T1____________T2(填“<”、“=”或“>”)
②在 T1 和 p6 的条件下,往密闭容器中充入 3 mol H2 和 1 mol CO2,该反应在第 5 min 时达到平衡,此时容器的体积为 1.8 L,则该反应在此温度下的平衡常数为________。
a.若此条件下反应至 3 min 时刻,改变条件并于 A 点处达到平衡,CH3OH 的浓度随反应时间的变化趋势如图 2所示(3~4 min 的浓度变化未表示出来),则改变的条件为 __________,请用 H2 的浓度变化计算从4 min开始到 A点的反应速率v(H2)= _________(保留两位小数)。
b.若温度不变,压强恒定在 p8 的条件下重新达到平衡时,容器的体积变为_______L
-
(28分)乙烯是重要的化工原料,可制备很多有机物。实验室制取乙烯的装置如下图所示:

(1)①实验室制取乙烯的化学反应方程式为_______________________________________;②此反应属于______________反应;烧瓶中加入碎瓷片的作用是______________________
(2)某化学课外兴趣小组学生在实验室里制取的乙烯中常混有少量的二氧化硫,老师启发他们并由他们自己设计了下图实验装置,以确认上述混合气体中有C2H4和SO2。回答下列问题:
①、I、II、Ⅲ、IV装置可盛放不同的试剂,其中:

I是________IV是_____(填试剂的序号)
A.品红溶液 B.NaOH溶液 C.浓硫酸 D.酸性KMnO4溶液
②、能说明SO2气体存在的现象是____________________________________
③、确定含有乙烯的现象是_____________________________________
(3) 实践中可以根据原子核磁共振谱(PMR)中观察到的氢原子给出的峰情况,确定有机物
的结构。用核磁共振谱的方法来研究C2H6O的结构,若峰面积比为___________(填比值),则
为CH3CH2OH ;若峰面积比为___________(填比值),则为CH3OCH3。
(4)由乙醇可制取乙酸乙酯,书写有关反应方程式(注明反应条件):
①由乙醇催化氧化制乙醛:_____________________________________________________
②乙醛与新制Cu(OH)2反应:_________________________________________________
(产物酸化后得乙酸)
③乙酸与乙醇制乙酸乙酯:_________________________________________________
CH3OCH3(g)+ H2O(g) △H1=—23.9 kJ•mol-1
C2H4(g)+2H2O(g) △H2= —29.1kJ•mol-1
CH3OCH3(g) △H3= +50.7kJ•mol-1
C2H4(g)+ H2O(g) △H4=akJ•mol-1


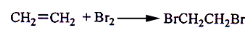 。可能存在的主要副反应有:乙醇在浓硫酸的存在下在l40℃脱水生成乙醚。用少量的溴和足量的乙醇制备1,2—二溴乙烷的装置如图所示。回答下列问题:
。可能存在的主要副反应有:乙醇在浓硫酸的存在下在l40℃脱水生成乙醚。用少量的溴和足量的乙醇制备1,2—二溴乙烷的装置如图所示。回答下列问题:






