一定条件下,在容积固定的某密闭容器中发生反应N2+3H22NH3。在10 s内N2的浓度由5 mol/L降至4 mol/L,下列说法正确的是( )
A. 用NH3表示的化学反应速率为0.1 mol/(L·s)
B. 使用合适的催化剂,可以加快该反应的速率
C. 增加H2的浓度或降低温度都会加快该反应的速率
D. 反应足够长时间,N2、H2中至少有一种物质浓度降为零
高三化学选择题中等难度题
一定条件下,在容积固定的某密闭容器中发生反应N2+3H22NH3。在10 s内N2的浓度由5 mol/L降至4 mol/L,下列说法正确的是( )
A. 用NH3表示的化学反应速率为0.1 mol/(L·s)
B. 使用合适的催化剂,可以加快该反应的速率
C. 增加H2的浓度或降低温度都会加快该反应的速率
D. 反应足够长时间,N2、H2中至少有一种物质浓度降为零
高三化学选择题中等难度题
一定条件下,在容积固定的某密闭容器中发生反应N2+3H22NH3。在10 s内N2的浓度由5 mol/L降至4 mol/L,下列说法正确的是( )
A. 用NH3表示的化学反应速率为0.1 mol/(L·s)
B. 使用合适的催化剂,可以加快该反应的速率
C. 增加H2的浓度或降低温度都会加快该反应的速率
D. 反应足够长时间,N2、H2中至少有一种物质浓度降为零
高三化学选择题中等难度题查看答案及解析
高三化学选择题中等难度题查看答案及解析
一定条件下,在容积固定的某密闭容器中发生反应N2+3H22NH3。在10s内N2的浓度由5mol/L降至4mol/L,下列说法正确的是
A.用表示的化学反应速率为0.1mol/(L·s)
B.使用合适的催化剂,可以加快该反应的速率
C.增加H2的浓度或降低温度都会加快该反应的速率
D.反应足够长时间,N2、H2中至少有一种物质浓度降为零
高三化学选择题简单题查看答案及解析
高三化学填空题中等难度题查看答案及解析
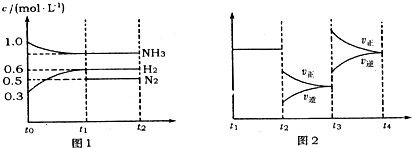
(l4分)向2L固定容积的密闭容器中加入一定量的NH3,H2和N2三种气体。一定条件下发生反应2NH3 N2+3H2,各物质浓度随时间变化如图1所示。图2为t时刻后改变容器中条件,平衡体系中反应速率随时间变化的情况,且两个阶段各改变一种不同的条件。
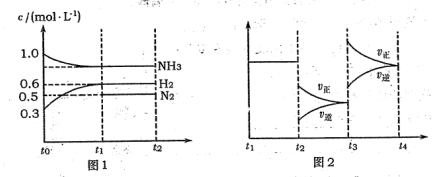
(1)能证明反应达到平衡状态的是________(填标号,下同)。
A.容器内压强不再发生变化 B. N2的体积分数不再发生变化
C. 容器内气体质量不再发生变化 D. 容器内气体密度不再发生变化
(2)若tl=15 s,则t0-t1阶段以H2浓度变化表示的反应速率为________ 。
(3)t3-t4阶段改变的条件为 ________。
(4)上述反应的平衡常数K=________(保留两位小数);向容器中再通入1.4molNH3、0.8 molH2,平衡________移动(填“向右”、“向左”或“不移动”)。
(5)25OC时,将a mol·L-1的氨水与0.1 mol·L-1的盐酸等体积混合。
①当溶液中离子浓度关系满足c(NH4+)<c(Cl-)时,则反应的情况可能为 ________
a.盐酸不足,氨水剩余 b. 氨水与盐酸恰好完全反应 c.盐酸过量
②当溶液中c(NH4+)=c(Cl-)时,用含a的代数式表示NH3·H2O的电离常数Kb= ________。
高三化学填空题简单题查看答案及解析
在一固定容积为2L的密闭容器内加入0.2mol的N2和0.6mol的H2,在一定条件下发生如下反应:N2(g)+3H2(g)2NH3(g) △H<0 。反应中NH3的物质的量浓度的变化情况如下图所示,请回答下列问题:
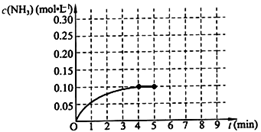
根据图,计算从反应开始到平衡时,平均反应速率v(NH3)=________。
⑵下列描述中能说明上述反应已达平衡的是________。
A.3v正(H2)=2v逆(NH3)
B.容器中气体的平均相对分子量不随时间而变化
C.容器中气体的密度不随时间而变化
D.容器中气体的分子总数不随时间而变化
⑶ 第5分钟末,保持恒温恒压,若继续通入0.2mol的N2和0.6mol的H2,平衡________移动(填“向正反应方向”、“向逆反应方向”或“不”)。
高三化学填空题困难题查看答案及解析
(12分)在一容积为2L的密闭容器内加入0.2mol的N2和0.6mol的H2,在一定条件下发生如下反应:N2(g)+3H2(g)2NH3(g)△H<0,反应中NH3的浓度变化如下图:
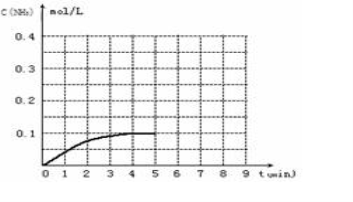
(1)根据上图,4min~5min之间,反应处于_________状态;(填“平衡”或“非平衡”)。
计算0~4min内,平均反应速率υ(NH3)= 。
(2)反应达到平衡后,第5分钟末,保持其它条件不变,若改变反应温度,反应达到新平衡后,则NH3的物质的量浓度不可能为 。
A.0.2mol·L-1 B.0.12mol·L-1 C.0.10mol·L-1 D.0.08mol·L-1
(3)反应达到平衡后,第5分钟末,保持其它条件不变,把容器的体积缩小为原来的一半,则平衡________________移动(填“向逆反应方向”、“向正反应方向”或“不”),化学平衡常数________(填“增大”、“减小”或“不变”)。
(4)在第5分钟末,将容器体积缩小为原来的一半后,若在第8分钟末达到新的平衡时(此时NH3的浓度约为0.25mol·L-1)。请在上图中画出第5分钟末到平衡时NH3浓度的变化曲线。
高三化学填空题中等难度题查看答案及解析
(10分)在一固定容积为2L的密闭容器内加入0.2mol的N2和0.6mol的H2,在一定条件下发生如下反应:N2(g)+3H2(g)2NH3(g) △H<0 。反应中NH3的物质的量浓度的变化情况如下图所示,请回答下列问题:
⑴ 根据下图,计算从反应开始到平衡时,平均反应速率v(NH3)=______________________________
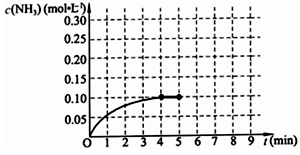
⑵ 该反应450℃的平衡常数________500℃时的平衡常数(填“>”、“<”或“=”)。
⑶ 下列描述中能说明上述反应已达平衡的是___________。
A.3v正(H2)=2v逆(NH3)
B.容器中气体的平均相对分子量不随时间而变化
C.容器中气体的密度不随时间而变化
D.容器中气体的分子总数不随时间而变化
⑷ 第5分钟末,保持恒温恒压,若继续通入0.2mol的N2和0.6mol的H2,平衡_______________移动(填“向正反应方向”、“向逆反应方向”或“不”)。
⑸ 第5分钟末将容器的体积缩小一半后,若在第8分钟末达到新的平衡(此时NH3浓度约为0.25mol/L),请在上图中画出第5分钟末到此平衡时NH3浓度的变化曲线。
高三化学填空题简单题查看答案及解析
(10分)在一固定容积为2L的密闭容器内加入0.2mol的N2和0.6mol的H2,在一定条件下发生如下反应:N2(g)+3H2(g)2NH3(g) △H<0 。反应中NH3的物质的量浓度的变化情况如下图所示,请回答下列问题:
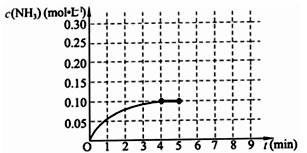
⑴ 根据上图,计算从反应开始到平衡时,平均反应速率v(NH3)=_________________。
⑵ 该反应450℃的平衡常数________500℃时的平衡常数(填“>”、“<”或“=”)。
⑶ 下列描述中能说明上述反应已达平衡的是___________。
A.3v正(H2)=2v逆(NH3)
B.容器中气体的平均相对分子量不随时间而变化
C.容器中气体的密度不随时间而变化
D.容器中气体的分子总数不随时间而变化
⑷ 第5分钟末,保持恒温恒压,若继续通入0.2mol的N2和0.6mol的H2,平衡_______________移动(填“向正反应方向”、“向逆反应方向”或“不”)。
⑸ 第5分钟末将容器的体积缩小一半后,若在第8分钟末达到新的平衡(此时NH3浓度约为0.25mol/L),请在上图中画出第5分钟末到此平衡时NH3浓度的变化曲线。
高三化学填空题简单题查看答案及解析
(10分)在一固定容积为2L的密闭容器内加入0.2 mol的N2和0.6 mol的H2,在一定条件下发生如下反应: N2(g)+3H2(g)2NH3(g) △H <0
(1)该反应450℃的平衡常数________500℃时的平衡常数(填“>”、“<”或“=”);
(2)下列描述中能说明上述反应已达平衡的是________
a.3v正(H2)=2v逆(NH3) b.容器中气体的平均相对分子量不随时间而变化
c.容器中气体的密度不随时间而变化 d.容器中气体的分子总数不随时间而变化
(3)上述反应若第5分钟时达到平衡,测得NH3的物质的量为0.2mol
计算从反应开始到平衡时,平均反应速率v(N2)为________mol/(L·min)
(4)保持其他条件不变,若初始投入量为a molN2、b molH2 、c molNH3,也可得到与上述相同的平衡,则a、b、c需满足关系式:________ ________ ;
(5)第5分钟末,保持其它条件不变, 若继续通入0.2 mol的N2和0.6 mol的H2,
则平衡________移动(填“向正反应方向”“向逆反应方向”或“不”)。
高三化学填空题困难题查看答案及解析