-
已知2H2(g)+ O2(g) = 2H2O(g),H—H、O=O和O—H键的键能分别为436 kJ·mol-1、496 kJ·mol-1和462 kJ·mol-1,则2mol H2完全燃烧放出的热量为
A. 480 kJ B. 916 kJ C. 960 kJ D. 190 kJ
高一化学单选题简单题查看答案及解析
-
已知2H2(g)+ O2(g) = 2H2O(g),H—H、O=O和O—H键的键能分别为436 kJ·mol-1、496kJ·mol-1和462 kJ·mol-1,则2g H2完全燃烧放出的热量为
A. 480 kJ B. 240 kJ C. 960 kJ D. 916 kJ
高一化学单选题中等难度题查看答案及解析
-
已知在反应2H2(g) + O2(g) = 2H2O(g)中,完全断开1mol H—H键需吸收热量436kJ,完全断开1mol O=O键需吸收热量496kJ,形成水蒸气中1molH—O键时可放出热量463kJ参加反应,则当1mol H2完全燃烧时该反应的能量变化为( )
A. 放出热量234.5 kJ B. 吸收热量234.5kJ
C. 放出热量242 kJ D. 吸收热量242kJ
高一化学选择题简单题查看答案及解析
-
已知:2H2(g)+O2(g)=2H2O(g) △H=-483.6KJ/mol。有关键能数据如下表:
化学键
H—H
O=O
键能/KJ▪mol-1
436
498
则水分子中O—H键键能为
A.463.4KJ/mol B.926.8KJ/mol
C.221.6KJ/mol D.413KJ/mol
高一化学选择题中等难度题查看答案及解析
-
已知:C(s)+H2O(g)=CO(g)+H2(g),ΔH=+130 kJ·mol-1
2C(s)+O2(g)=2CO(g),ΔH=-220kJ·mol-1
H-H、O=O键能分别为436、496 kJ·mol-1,则O-H键能为
A.222 kJ·mol-1 B.444 kJ·mol-1
C.462 kJ·mol-1 D.924 kJ·mol-1
高一化学选择题中等难度题查看答案及解析
-
已知:C(s)+H2O(g)=CO(g)+H2(g) ΔH=akJ·mol-1
2C(s)+O2(g)=2CO(g) ΔH=-220kJ·mol-1
H-H、O=O和O-H键的键能分别为436、496和462kJ·mol-1,则a为
A.+130 B.-118 C.+350 D.-332
高一化学选择题中等难度题查看答案及解析
-
已知C(s)+H2O(g)=CO(g)+H2(g) ΔH=AkJ/mol
2C(s)+O2(g)=2CO(g) ΔH=-220kJ/mol
若H-H、O=O和O-H键的键能分别为436/496和462kJ/mol,则a为
A.+130 B.+350 C.-332 D.-118
高一化学单选题简单题查看答案及解析
-
已知拆开1molH2需要消耗436kJ能量,拆开1molO2需要消耗496kJ能量,形成水分子中的1molH-O能够释放463kJ能量。根据以上所给的数据计算反应:
2H2(g)+O2(g)=2H2O(g) ;△H = ________ 。
(2)如图所示,可形成氢氧燃料电池。通常氢氧燃料电池有酸式(当电解质溶液为H2SO4溶液时)和碱式[当电解质溶液为NaOH(aq)或KOH(aq)时]两种。试回答下列问题:
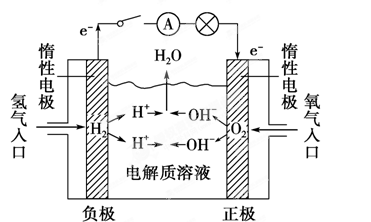
①酸式电池的电极反应:负极________________,正极______________;电池总反应:______________;电解质溶液pH的变化________(填“变大”、“变小”或“不变”)。
②碱式电池的电极反应:负极________________,正极______________;电池总反应:______________;电解质溶液pH的变化________(填“变大”、“变小”或“不变”)。
高一化学填空题中等难度题查看答案及解析
-
已知 2 g H2 完全燃烧生成水蒸气时放出 242 kJ 热量, 1 mol O2 中的化学键完全断裂时吸收 496 kJ 热量,1 mol H2 中 H—H 键完全断裂时吸收 436kJ 热量,则水蒸气中 1 mol H—O 键形成时放出 热量为
A.926kJ B.463 kJ C.402.5kJ D.23115 kJ
高一化学选择题简单题查看答案及解析
-
已知2H2(g)+O2(g)→2H2O(g) ΔH= -484KJ/mol;2H2(g)+O2(g)→2H2O(l) ΔH= -572KJ/mol
若在标准状况下,将H2和O2组成的混合气体点燃爆炸后,再恢复到标准状况下,气体总体积减少33.6升,计算反应过程中放出的热量是多少?(要求简要解析)
高一化学计算题简单题查看答案及解析