-
已知下列化学键的键能:
化学键
C-C
N-N
O-O
0=O
O-H
S-H
Se-H
N-H
As-H
键能/(kJ·mol-1)
347.7
193
142
497.3
462.8
363.5
276
386
247
回答下列问题:
(1)过氧化氢不稳定,易发生分解反应2H2O2(g)=2H2O(g) +O2(g),利用键能数据计算该反应的反应热为__________________;
(2)O-H、S-H、Se-H的键能逐渐减小,原因是_______________________________,据此可推测P-H键的键能范围为____________<P-H键键能<_______________;
(3)有机物是以碳骨架为基础的化合物,即碳原子间易形成C-C长链,而氮原子与氮原子间,氧原子与氧原子间难形成N-N长链和O-O长链,原因是_______________。
高二化学填空题中等难度题查看答案及解析
-
肼是一种高能燃料。已知各共价键键能(断裂或形成1mol共价键时吸收或释放的能量)如表:
N≡N
O=O
N-N
N-H
O-H
键能(KJ•mol﹣1)
946
497
154
391
463
(1)N2H4(g)+O2(g)⇌N2(g)+2H2O(l) ∆H=________KJ•mol﹣1 。
(2)密闭容器中进行反应:3Fe(s)+4H2O(g)
Fe3O4(s)+4H2(g) ∆H<0反应的化学平衡表达式为K=________。
(3)已知:600℃时,上述反应的平衡常数K=16。现有如图甲(恒温恒压)和如图乙(恒温恒容)两容器:
起始时按下表所示分别加入各物质,体积为2L,在600℃时反应经过一段时间后均达平衡。
Fe
H2O(g)
Fe3O4
H2
甲/mol
2.0
1.0
2.0
0.5
乙/mol
2.0
2.0
2.0
1.0
①关于甲、乙容器,下列说法正确的是________。
A.反应开始时两容器内的逆反应速率:甲<乙
B.若甲容器内气体的密度不再变化,则说明反应已达到平衡状态
C.若乙容器内气体的压强不再变化,则说明反应已达到平衡状态
D.平衡后添加Fe3O4,两容器内的平衡均逆向移动
②投料后甲5min达平衡,则此段时间内的平均反应速率v(H2)=________。
③平衡后若将乙容器体系温度突然降低100℃,图象中能正确反映平衡移动过程中容器内变化情况的是________。
A.
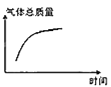 B.
B. 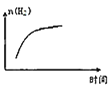 C.
C. (4)如图为恒容绝热容器:

进行上述反应,起始与平衡时的各物质的量见表:
Fe
H2O(g)
Fe3O4
H2
起始/mol
3.0
3.0
0
0
平衡/mol
m
n
p
q
Fe
H2O(g)
Fe3O4
H2
A/mol
3.0
3.0
0
0
B/mol
0
0
3.0
3.0
C/mol
m
n
p
q
若在达到平衡后的容器丙中,分别按照下列A、B、C三种情况继续添加各物质,则再次达平衡时,容器丙中H2的百分含量按由大到小的顺序______(用A、B、C表示)。
高二化学综合题中等难度题查看答案及解析
-
已知断裂1mol化学键所需的能量(kJ):N≡N键为942、N—N键为154、N—H键为391、H—O键为463。有关化学反应的能量变化如图所示。下列说法正确的是( )
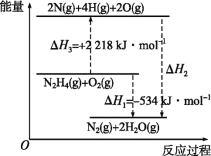
A.ΔH2=ΔH1+ΔH3
B.断裂1molO2(g)中的共价键需要吸收500kJ的能量
C.ΔH2>ΔH1
D.N2H4(g)+O2(g)=N2(g)+2H2O(l) ΔH=-534kJ·mol-1
高二化学单选题中等难度题查看答案及解析
-
肼(H2NNH2)是一种高能燃料,有关化学反应的能量变化如图所示,已知断裂1 mol化学键所需的能量(kJ):N≡N为942、O
O为500、N—N为154,则断裂1 mol N—H键所需的能量(kJ)是

A.194 B.391 C.516 D.658
高二化学选择题中等难度题查看答案及解析
-
肼(H2NNH2)是一种高能燃料,有关化学反应的能量变化如下图所示。已知断裂1 mol化学键所需的能量(kJ):N≡N为942、O=O为500、N—N为154,则断裂1 mol N—H键所需能量(kJ)是( )
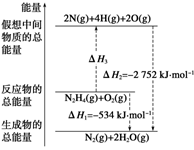
A.194 B.391 C.516 D.658
高二化学选择题中等难度题查看答案及解析
-
有关化学反应的能量变化如图所示,已知断裂1 mol化学键所需的能量(kJ): N
N键为942、O=O键为500、O—H键为463,则断裂1 molNH3中N—H键所需的能量是

A.658 B.516 C. 391 D. 194
高二化学选择题简单题查看答案及解析
-
肼(H2N—NH2)是一种高能燃料,有关化学反应的能量变化如图所示,已知断裂1 mol化学键所需的能量(kJ):N≡N键为942、O=O键为500、N—N键为154,则断裂1 mol N—H键所需的能量(kJ)是( )
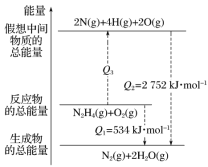
A. 194 B. 391 C. 516 D. 658
高二化学单选题简单题查看答案及解析
-
已知2NH3(g)+3Cl3(g)=N2(g)+6HCl(g)ΔH,已知反应的相关的化学键键能数据如下:
化学键
Cl-Cl
N-H
N≡N
H-Cl
O-H
E/(kJ·mol-1)
242.7
390.8
946
431.8
463
由此计算△H为
A.+463.9kJ·mol-1 B.-463.9kJ·mol-1
C.+231.95kJ·mol-1 D.-231.95kJ·mol-1
高二化学单选题中等难度题查看答案及解析
-
肼(H2NNH2)是一种高能燃料,有关化学反应的能量变化如图所示。已知断裂1 mol化学键所需的能量(kJ):N≡N为942、O=O为500、N-N为154,则断裂1 mol N-H键所需的能量 (kJ)是
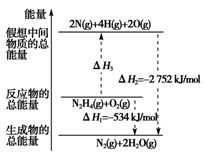
A. 194 B.391 C.516 D.658
高二化学选择题中等难度题查看答案及解析
-
肼(H2NNH2)是一种高能燃料,有关化学反应的能量变化如图所示。已知断裂1 mol化学键所需的能量(kJ):N≡N为942、O=O为500、N-N为154,则断裂1 mol N-H键所需的能量 (kJ)是

A. 194 B. 391 C. 516 D. 658
高二化学选择题困难题查看答案及解析