-
KMnO4和MnO2都是重要的化学物质,在实验室可以作氧化剂和催化剂。某化学学习小组对两种物质的制备探究如下:
Ⅰ.MnO2的制备:
该学习小组设计了将粗MnO2(含有较多的MnO、MnCO3和Fe2O3)样品转化为纯MnO2的实验,其工艺流程如下:
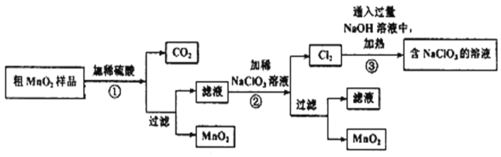
请回答下列问题:
(1)第②步操作中,NaClO3氧化MnSO4的离子方程式为______________
(2)第③步操作中,最终得到的固体除NaClO3外,还一定含有下列物质中的________(填序号)。
a.NaCl b.NaClO c.NaOH d.NaClO4
(3)为得到纯净的MnO2,须将过滤后的MnO2合并后进行洗涤。洗涤沉淀所用的玻璃仪器有______________。
(4)NaClO3和MnO2在一定条件下都可以氧化浓盐酸制取氯气,制取等量的氯气消耗NaClO3与MnO2的物质的量之比为__________。
Ⅱ.KMnO4的制备:
(5)实验室由二氧化锰制备高锰酸钾可分两步进行:
第一步:MnO2与KOH共熔并通入氧气:2MnO2+4KOH+O2=2K2MnO4+2H2O;
第二步:通入CO2,可使K2MnO4发生歧化反应生成KMnO4和MnO2。
第二步完成反应时,转化为KMnO4的K2MnO4占其全部的百分率约为________(精确到0.1%)。
-
研究催化剂对化学反应有重要意义。为探究催化剂对双氧水分解的催化效果,某研究小组做了如下实验:
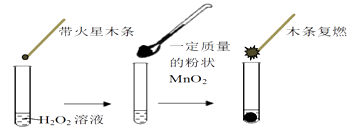
(1)甲同学欲用图所示实验来证明MnO2是H2O2分解反应的催化剂。该实验__________(填“能”或“不能”)达到目的,原因是__________。(若能,不必回答原因)
(2)为分析Fe3+和Cu2+对H2O2分解反应的催化效果,丙同学设计如下实验(三支试管中均盛有10mL5%H2O2)
| 试管 | 夏 | II | III |
| 滴加试剂 | 5滴0.lmol·L-1FeCl3 | 5 滴 0.1mol·L-1 CuCl2 | 5 滴 0.3mol·L-1 NaCl |
| 产生气泡情况 | 较快产生细小气泡 | 缓慢产生细小气泡 | 无气泡产生 |
由此得到的结论是__________,设计实验Ⅲ的目的是__________。
(3)在上述实验过程中,分别检测出溶液中有二价铁生成,査阅资料得知:将作为催化剂的FeCl3溶液加入H2O2溶液后,溶液中会发生两个氧化还原反应,且两个反应中H2O2均参加了反应,试从催化剂的角度分析,这两个氧化还原反应的化学方程式分别是__________和__________(按反应发生的顺序写)。
-
某化学实验小组的同学为探究和比较SO2和Cl2的漂白性,设计了如下的实验装置。

(1)实验室常用软锰矿(主要成分是MnO2)与浓盐酸混合加热的方法制备Cl2,写出实验室制备氯气的化学方程式:________________________________________________。在此化学反应中,氧化剂与还原剂的物质的量之比为____________;若反应过程中转移电子的物质的量为6 mol,则生成氯气的物质的量为____________mol。
(2)反应开始一段时间后, B、D两个试管中的品红溶液出现的现象是: B:_______________________; D:________________________;
(3)停止通气后,再给B、D两个试管分别加热,两个试管中的现象分别是:B:_______________________; D:________________________;
(4)实验中NaOH溶液的作用是________________________________________。若将C中NaOH溶液换成水,当通入物质的量比为1:1的SO2和Cl2,恰好反应生成两种强酸(其中一种是含氧酸,另一种是无氧酸),该反应的化学方程式是:_____________________________________________________________________。
-
(13分)某化学实验小组的同学为探究和比较SO2和氯水的漂白性,设计了如下的实验装置。
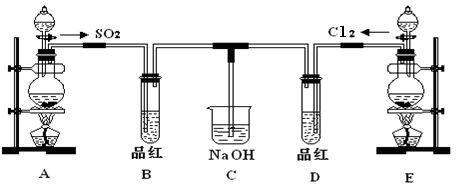
(1)实验室用装置E制备Cl2,其反应的化学化学方程式为:MnO2+4HCl(浓) MnCl2+Cl2 +2H2O请指出该反应中的液体反应物在反应中所表现出的化学性质:
MnCl2+Cl2 +2H2O请指出该反应中的液体反应物在反应中所表现出的化学性质:
____________________________________________________________________;
(2)①反应开始一段时间后,观察到B、D两个试管中的品红溶液出现的现象是:
B:________________________________,D:_________________________。
②停止通气后,再给B、D两个试管分别加热,两个试管中的现象分别为
B:________________________________,D:____________________________。
(3)另一个实验小组的同学认为SO2和氯水都有漂白性,二者混合后的漂白性肯定会更强,他们将制得的SO2和Cl2按1:1同时通入到品红溶液中,结果发现褪色效果并不像想象那样。请你分析该现象的原因(用化学方程式表示)__________________________________
-
某化学实验小组的同学为探究和比较SO2和氯水的漂白性,设计了如下的实验装置。请回答下列问题:
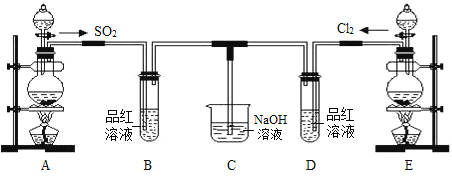
(1)实验室用装置E制备Cl2,其反应的化学方程式为MnO2+4HCl(浓)  MnCl2 + Cl2↑ + 2H2O。将上述化学方程式改写为离子方程式_______________________________。
MnCl2 + Cl2↑ + 2H2O。将上述化学方程式改写为离子方程式_______________________________。
(2)①反应开始一段时间后,观察到B、D两个试管中的品红溶液出现__________的现象(填选项序号,下同)。
A.品红溶液都褪色 B.品红溶液都不褪色
C.B中品红溶液褪色,D中不褪色 D.D中品红溶液褪色,B中不褪色
②停止通气后,再给B、D两个试管分别加热,两个试管中的溶液呈现的颜色分别为________。
A.无色、红色 B.无色、无色 C.红色、红色 D.红色、无色
(3)C烧杯中氢氧化钠溶液的作用是_____________________________,写出Cl2通入NaOH溶液中的化学方程式_______________________________。
(4)另一个实验小组的同学认为SO2和氯水都有漂白性,二者混合后的漂白性肯定会更强,他们将制得的SO2和Cl2按物质的量之比1︰1同时通入到品红溶液中,结果发现褪色效果并不像想象的那样。请分析该现象的原因(用离子方程式表示)_______________________________________。
-
某校化学实验兴趣小组为了探究在实验室制备Cl2的过程中 有水蒸气和HCl挥发出来,同时证明氯气的某些性质,甲同学设计了如下图所示的实验装置(支撑用的铁架台省略),完成下列问题。

(1)用 MnO2和浓盐酸混合共热制得氯气的化学方程式是____ ____。
(2)若用含有0.2 mol HCl的浓盐酸与足量的MnO2反应制Cl2,制得的Cl2体积在标准状况下总是小于1.12 L的原因是_____________________________________________。
(3)①装置B的作用是____________________________________________________,
装置B中的现象是____________________________。
②装置D和E出现的不同现象说明的问题是_____________________________。
③装置F的作用是________________________。
④装置G中发生反应的化学方程式为 。
-
实验室制备氯气的化学方程式为MnO2+4HCl(浓)
 MnCl2+Cl2↑+2H2O,该反应中氧化剂与还原剂的物质的量之比为________,请将该化学方程式改写为离子方程式________,氯气的工业制法是电解饱和食盐水,请列举出氯气在生产、生活中的应用(两条)________将氯气通入紫色石蕊试液中可观察到的现象是________.
MnCl2+Cl2↑+2H2O,该反应中氧化剂与还原剂的物质的量之比为________,请将该化学方程式改写为离子方程式________,氯气的工业制法是电解饱和食盐水,请列举出氯气在生产、生活中的应用(两条)________将氯气通入紫色石蕊试液中可观察到的现象是________.
-
某校化学实验兴趣小组为了探究实验室制备Cl2的过程中有水蒸气和HCl挥发出来,同时证明氯气的某些性质,甲同学设计了如下图所示的实验装置(支撑用的铁架台省略),完成下列问题。

(1)用 MnO2和浓盐酸混合共热制得氯气的化学方程式是__________________;
(2)若用含有0.2mol HCl的浓盐酸与足量的MnO2反应制Cl2,制得的Cl2体积在标准状况下总是小于1.12L的原因是__________________;
(3)①装置B的作用是__________________;
②装置D和E出现的不同现象说明的问题是__________________;
③装置F的作用是__________________;
④装置G中发生反应的化学方程式为__________________。
-
实验室制备氯气的化学方程式为MnO2+4HCl(浓) MnCl2+Cl2↑+2H2O,该反应中氧化剂与还原剂的物质的量之比为________,请将该化学方程式改写为离子方程式______________________________,氯气的工业制法是电解饱和食盐水,请列举出氯气在生产、生活中的应用(两条)_________________,___________________;
MnCl2+Cl2↑+2H2O,该反应中氧化剂与还原剂的物质的量之比为________,请将该化学方程式改写为离子方程式______________________________,氯气的工业制法是电解饱和食盐水,请列举出氯气在生产、生活中的应用(两条)_________________,___________________;
将氯气通入紫色石蕊试液中可观察到的现象是_______________________________。
-
无水AlCl3是一种重要的有机合成催化剂,该物质在183℃时升华,遇潮湿空气即产生大量白雾。某中学化学兴趣小组拟利用中学常见仪器设计实验制备无水AlCl3,实验装置如下图所示。请回答:
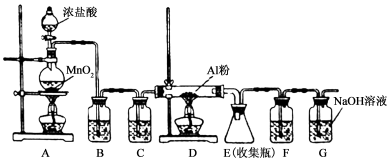
(1)制备实验开始时,先检查装置的气密性,接下来的操作依次是________。
a.加入MnO2粉末
b.点燃A中酒精灯
c.加入浓盐酸
d.点燃D处酒精灯
(2)写出A装置中发生反应的化学方程式___________________________________。
(3)装置B中的试剂是__________。该装置存在安全隐患,请指出 。
(4)装置F中试剂为 ,甲同学认为F和G可以用一种仪器替代,且加入一种药品即可达到相同效果。这种药品可以是 ,其作用是 。







