-
NaClO和KAl(SO4)2都是重要的化工产品,均可应用于造纸业。
(1)常温下,NaClO溶液的pH>7,原因是________________________________ (用离子方程式表示)。
(2)根据NaClO的性质推测,在纸浆中加入NaClO溶液的目的是________________。
(3)向饱和NaClO溶液中加入饱和KAl(SO4)2溶液可产生大量的白色胶状沉淀。反应的离子方程式是___________________。
高二化学填空题中等难度题查看答案及解析
-
NaClO和KAl(SO4)2都是重要的化工产品,均可应用于造纸业。
(1)NaClO溶液pH>7,原因是(用离子方程式表示)________________________。
(2)根据NaClO的性质推测,在纸浆中加入NaClO溶液的目的是___________________。
(3)某小组同学探究饱和NaClO和KAl(SO4)2溶液混合反应的实验。打开活塞向烧瓶中的NaClO加入饱和KAl(SO4)2溶液,产生大量的白色胶状沉淀。出现上述现象的原因是__________________________(请用反应的离子方程式表示)。
(4)25℃时,0.1 mol/L的HA溶液中c(H+)/c(OH-)=1010。请回答下列问题:
(a)在加水稀释HA溶液的过程中,
随着水量的增加而增大的是 (填字母)。
A.c(H+)/c(HA) B.c(HA)/(A-) C.c(H+)与c(OH-)的乘积 D.c(OH-)
(b)NaA溶液显________(填“酸性”、“中性”或“碱性”),
高二化学填空题简单题查看答案及解析
-
家用氯漂白剂的有效成分是NaClO,除用于漂白衣物、消除污渍外,在食品加工中也广泛应用。
Ⅰ.(1)常温下,一定浓度次氯酸钠水溶液的pH=a,则a______7(填>、<或=);结合离子方程式解释其原因是__________________________________________________,此时,溶液中由水电离出的c(OH-)=________mol/L。
(2)漂白剂与酸混合后效果更佳,将0.1000mol/L NaClO溶液与0.1000mol/L 硫酸溶液等体积混合后,关于所得溶液的以下分析正确的是____________(忽略HClO的分解;HSO4-的电离视为完全)。
A.c(HClO)+c(ClO-)=0.1000mol/L
B.c(H+)>c(Na+)=c(SO42-)>c(HClO)>c(ClO-)>c(OH-)
C.c(Na+)+c(H+)=c(SO42-)+c(ClO-)+c(OH-)
D.c(H+)-c(OH-)=2c(ClO-)+c(HClO)
Ⅱ.取20.00g家用氯漂白剂溶液配制成100mL溶液,取出10mL,加入过量KI处理,用足量稀硫酸酸化,然后立即用0.1000mol/L Na2S2O3溶液滴定生成的I2(2Na2S2O3+I2=2I-+Na2S4O6),指示剂显示滴定终点时,消耗Na2S2O3溶液30.00 mL;
(1)用KI处理漂白剂生成I2的离子方程式为________________________________。
(2)该滴定过程选用的指示剂通常为___________,判断滴定终点时的现象是___________________________________________________________________________。
(3)该漂白剂中“有效氯”的含量为_________________(结果保留一位小数)。若滴定结束时,发现滴定管尖嘴部分有气泡,则测定结果________(填“偏高”“偏低”“无影响”)。
注:“有效氯”指每克含氯消毒剂的氧化能力相当于多少克Cl2的氧化能力。
高二化学综合题困难题查看答案及解析
-
(6分)根据下列事实,完成相关的离子方程式或电离方程式
(1)Na2S溶液使酚酞显红色
(2)硫酸铝钾[明矾KAl(SO4)2·12H2O]可以作净水剂
(3)常温下,磷酸(H3PO4)溶液pH﹤7
高二化学填空题中等难度题查看答案及解析
-
氨是重要的工业原料,在农业、医药、国防和化工等领域有重要应用。
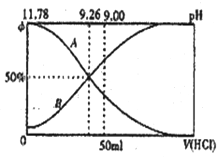
Ⅰ.常温下向100 mL 0.2 mol·L-l的氨水中逐滴加入0.2mol·L-1的盐酸,所得溶液的pH、溶液中NH4+和NH3·H2O物质的量分数与加入盐酸的体枳的关系如图所示,根据图象回答下列问题。
(1)表示NH3·H2O浓度变化的曲线是______(填“A”或“B”)。
(2)NH3·H2O的电离常数为______(已知 lg1.8=0.26)。
(3)当加入盐酸体积为50mL时,溶液中c(NH4+)-c(NH3·H2O)=____mol·L-1(用数字表示精确值)。
Ⅱ.若液氨中也存在类似水的电离(H2O+H2O
H3O++OH-),写出液氨的电离方程式__________________________。
III.氨是一种重要的化工原料,可以用来制备肼(N2H4)。肼的制备方法是用次氯酸钠氧化过量的氨。 已知ClO-水解的方程式为:ClO-+H2O
HClO+OH-。常温下,该水解反应的平衡常数为K=1.0×10-6mol·L-1,则1.0mol· L -1NaClO溶液的pH=________。
高二化学填空题中等难度题查看答案及解析
-
氨是重要的工业原料,在农业、医药、国防和化工等领域有重要应用。
Ⅰ.常温下向100 mL 0.2 mol·L-l的氨水中逐滴加入0.2mol·L-1的盐酸,所得溶液的pH、溶液中NH4+和NH3·H2O物质的量分数与加入盐酸的体枳的关系如图所示,根据图象回答下列问题。
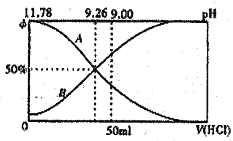
(1)表示NH3·H2O浓度变化的曲銭是____________(填“A”或“B”)。
(2)NH3·H2O的电离常数为____________ (已知 lg1.8=0.26)。
(3)当加入盐酸体积为50mL时,溶液中c(NH4+)·c(NH3·H2O)=____________mol·L-1(用数字表示精确值)。
Ⅱ.若液氨中也存在类似水的电离(H2O+H2O
H3O++OH-),碳酸钠溶于液氨后也能发生完全电离和类似水解的氨解。
(1)写出液氨的电离方程式__________________________。
(2)写出碳酸钠溶于液氨后第一级氨解的离子方程式____________________________________。
(3)写出碳酸钠的液氨溶液中各离子浓度的大小关系____________________________________。
高二化学综合题中等难度题查看答案及解析
-
氨是重要的工业原料,在农业、医药、国防和化工等领域有重要应用。
I.常温下向100mL0.2mo/L的氨水中逐滴加入0.2mol/L的盐酸,所得溶液的pH、溶液中NH4+和NH3·H2O物质的量分数与加入盐酸的体积的关系如下图所示,根据图像回答下列问题。
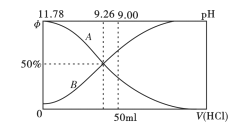
(1)表示NH3·H2O浓度变化的曲线是__________(填“A”或“B")。
(2)NH3·H2O的电离常数为_______(已知lg1.8 = 0.26)。
(3)当加入盐酸体积为50mL时,溶液中c(NH4+)- c(NH3·H2O) =_____mol/L (用数字表示)。
Ⅱ.若液氨中也存在类似水的电离( H2O+H2O
H3O+ +OH-),碳酸钠溶于液氨后也能发生完全电离和类似水解的氨解。
(1)写出液氨的电离方程式_________.
(2)写出碳酸钠溶于液氨后第一级氨解的离子方程式__________
(3)写出碳酸钠的液氨溶液中各离子浓度的大小关系____________
高二化学填空题中等难度题查看答案及解析
-
Ⅰ.常温下,浓度均为0.1 mol·L-1的六种溶液的pH如表所示:
溶质
CH3COONa
NaHCO3
Na2CO3
NaClO
NaCN
Na2SO4
pH
8.8
9.7
11.6
10.3
11.1
7.0
请回答下列问题:
(1)上述六种溶液中,水的电离程度最小的是________(填化学式)。
(2)若欲增大氯水中次氯酸的浓度,可向氯水中加入上表中的物质是_____(填写一种物质即可)。
Ⅱ.常温下,向100 mL 0.2 mol·L-1的氨水中逐滴加入0.2 mol·L-1的盐酸,所得溶液的pH、溶液中NH4+和NH3·H2O的物质的量分数与加入盐酸的体积的关系如图所示:
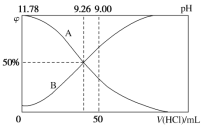
(3)根据图象回答下列问题。
①表示NH3·H2O浓度变化的曲线是__________(填“A”或“B”)。
②NH3·H2O的电离常数为______________。
③当加入盐酸体积为50 mL时,溶液中c(NH4+)-c(NH3·H2O)=______ mol·L-1(用数字计算式表示)。
Ⅲ.已知:Ag++SCN-=AgSCN↓(白色)。实验室可通过如下过程测定所制硝酸银样品的纯度(杂质不参与反应)。
(4)称取2.000 g制备的硝酸银样品,加水溶解,定容到100 mL。溶液配制过程中所用的玻璃仪器除烧杯、玻璃棒外还有________。
(5)准确量取25.00 mL溶液,酸化后滴入几滴铁铵钒[NH4Fe(SO4)2]溶液作指示剂,再用0.100 mol·L-1 NH4SCN标准溶液滴定。滴定终点的实验现象为____________。终点时消耗标准溶液25mL,硝酸银样品纯度为_______。
高二化学综合题中等难度题查看答案及解析
-
Ⅰ.KAl(SO4)2·12H2O(明矾)是一种复盐,在造纸等方面应用广泛。实验室中, 采用废易拉罐(主要成分为 Al,含有少量的 Fe、Mg 杂质)制备明矾的过程如下图所示。 回答下列问题:
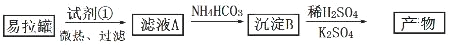
(1)为尽量少引入杂质,试剂①应选用______________(填标号)。
a.HCl 溶液 b.H2SO4 溶液 c.氨水 d.NaOH 溶液
(2)易拉罐溶解过程中主要反应的化学方程式为_________________________。
(3)沉淀 B 的化学式为______________________
II.毒重石的主要成分 BaCO3(含 Ca2+、Mg2+、Fe3+等杂质),实验室利用毒重石制备BaCl2·2H2O 的流程如下:

(4)毒重石用盐酸浸取前需充分研磨,目的是_________________________________。
Ca2+
Mg2+
Fe3+
开始沉淀时的pH
11.9
9.1
1.9
完全沉淀时的pH
13.9
11.1
3.2
(5)滤渣Ⅱ中含 (填化学式)。加入 H2C2O4 时应避免过量,原因是_________________________________。已知:Ksp(BaC2O4) =1.6×10-7, Ksp(CaC2O4)=2.3×10-9
高二化学推断题中等难度题查看答案及解析
-
常温下,浓度均为0.1 mol·L-1的六种溶液的pH如下表所示:
溶质
CH3COONa
NaHCO3
Na2CO3
NaClO
NaCN
Na2SO4
pH
8.8
9.7
11.6
10.3
11.1
7.0
请回答下列问题:
(1)上述六种溶液中的阴离子,结合H+能力最强的是____________(填离子符号)。
(2)上述六种溶液中,水的电离程度最小的是____________(填化学式)。
(3)若欲增大氯水中次氯酸的浓度,可向氯水中加入上表中的物质是________、________(每空填写一种物质)。
(4)依据复分解反应的规律,判断下列反应不能进行的是________。
A.CH3COOH+Na2CO3=NaHCO3+CH3COONa
B.CH3COOH+NaCN=CH3COONa+HCN
C.CO2+H2O+2NaCN=Na2CO3+2HCN
(5)将CO2气体通入饱和碳酸钠溶液中,可以观察到的现象是_______,原因为_________(用离子方程式表示)。
高二化学综合题中等难度题查看答案及解析