-
CO2和甲烷催化合成CO和H2是CO2资源化利用的有效途径。主要反应如下:
Ⅰ:CH4(g)+CO2(g)⇌2CO(g)+2H2(g) △H=+247kJ/mol
(1)已知CH4(g)+H2O(g)⇌CO(g)+3H2(g) △H=+206 kJ/mol
写出CH4和水蒸气反应生成CO2的热化学方程式:___。
(2)在恒温、恒容的密闭容器中发生反应Ⅰ,下列选项能够说明反应Ⅰ达到平衡状态的是___。
A.混合气体的密度不变
B.混合气体的总压强不变
C.CH4、CO2、CO、H2的物质的量之比为1:1:2:2
D.2v正(H2)=v逆(CH4)
E.混合气体的平均相对分子质量不变
(3)催化合成的温度通常维持在550﹣750℃之间,从反应速率角度分析其主要原因可能是___。
(4)将CH4与CO2各1mol充入某密闭容器中,发生反应Ⅰ。100kPa时,反应Ⅰ到达平衡时CO2的体积分数与温度的关系曲线如图所示。
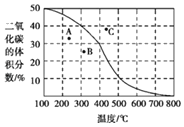
①图中A、B、C三点表示不同温度、压强下达到平衡CO2的体积分数,则___点对应的平衡常数最小,判断依据是___;___点对应的压强最大。
②300℃、100kPa下,该容器中反应Ⅰ经过40min达到平衡,计算反应在0﹣40 min内的平均反应速率为v(CO2)=___mol/min(用分数表示)。
-
CO2和甲烷催化合成CO和H2是CO2资源化利用的有效途径。主要反应为
Ⅰ:CH4(g)+CO2(g) 2CO(g)+2H2(g) △H=+247kJ/mol
2CO(g)+2H2(g) △H=+247kJ/mol
(1)已知CH4(g)+H2O(g) CO(g)+H2(g) △H=+206kJ/mol
CO(g)+H2(g) △H=+206kJ/mol
写出CH4和水蒸气反应生成CO2的热化学方程式_______________________________。
(2)在恒温、恒容的密闭容器中发生反应I,下列选项能够说明反应I达到平衡状态的是______。
A.混合气体的密度不变
B.混合气体的总压强不变
C.CH4、CO2、CO、H2的物质的量之比为1:1:2:2
D.3v正(H2)=v逆(CH4)
E.混合气体的平均相对分子质量不变
(3)将CH4与CO2各1mol充入某密闭容器中,发生反应I。100kPa时,反应I到达平衡时CO2的体积分数与温度的关系曲线如图所示。
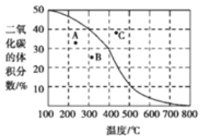
①图中A、B、C三点表示不同温度、压强下达到平衡时CO2的体积分数,则______点对应的平衡常数最小,判断依据是______________________________;________点对应的压强最大。
②300℃,100kPa下,该容器中反应I经过40min达到平衡,计算反应在0-40min内的平均反应速率为v(CO2)=_________mol/min(结果保留两位有效数字)
-
CO2甲烷化是一种实现CO2资源化利用的有效途径。
Ⅰ.热化学转化
CO2甲烷化过程发生反应:CO2(g)+4H2(g) CH4(g)+2H2O(g)ΔH
CH4(g)+2H2O(g)ΔH
(1)每生成1mol CH4(g),放热165 kJ,则ΔH=______。
(2)反应的平衡常数的表达式:K=______。温度升高,K______(填“增大”或“减小”)。
(3)其他条件不变时,一段时间内,压强对CO2的转化率及CH4的选择性的影响如下图。

注:选择性=转化为目标产物的原料量÷原料总的转化量
CO2甲烷化反应选择0.1MPa而不选择更高压强的原因是______。
Ⅱ.电化学转化
多晶Cu可高效催化CO2甲烷化,电解CO2制备CH4的原理示意图如下。电解过程中温度控制在10℃左右,持续通入CO2。阴、阳极室的KHCO3溶液的浓度基本保持不变。

(4)多晶Cu作______(填“阴”或“阳”)极。
(5)结合电极反应式,说明阴极室KHCO3溶液浓度基本不变的原因:______。
(6)上述电解过程中采取了______措施(写2条即可)使CO2优先于H+放电。
-
CO2是一种廉价的碳资源,其综合利用具有重要意义。回答下列问题:
(1)CO2与CH4经催化重整,制得合成气:CH4(g)+ CO2(g) 2CO (g)+ 2H2(g)
2CO (g)+ 2H2(g)
①已知上述反应中相关的化学键键能数据如下:
| 化学键 | C—H | C=O | H—H | C O(CO) O(CO) |
| 键能/kJ·mol−1 | 413 | 745 | 436 | 1075 |
则该反应的ΔH=_________。分别在v L恒温密闭容器A(恒容)、B(恒压,容积可变)中,加入CH4和CO2各1 mol的混合气体。两容器中反应达平衡后放出或吸收的热量较多的是_______(填“A” 或“B ”)。
(2)CO2可以被NaOH溶液捕获。
①若所得溶液pH=13,CO2主要转化为_______(写离子符号);若所得溶液c(HCO3−)∶c(CO32−)=2∶1,溶液pH=___________。(室温下,H2CO3的K1=4×10−7;K2=5×10−11)
②当2molCO2通入3molNaOH被吸收时,溶液中离子浓度关系正确的是(选填字母)________。
a.c(Na+)+c(H+)=c(CO32−)+c(HCO3-)+c(OH-)
b.c(Na+)>c(HCO3-)>c(CO32−)> c(OH-)>c(H+)
c.3c(Na+)=2[c(CO32−)+c(HCO3-) +c(H2CO3)]
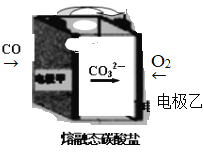
(3)CO2辅助的CO—O2燃料电池,工作原理如图所示,固体介质中CO32— 可定向移动。电池的负极反应式:________________________________电池工作时需向某电极通入CO2以触发反应,该电极为_____________(填“甲”或“乙”)
-
“温室效应”是全球关注的环境问题之一。CO2是目前大气中含量最高的一种温室气体,CO2的综合利用是解决温室及能源问题的有效途径。
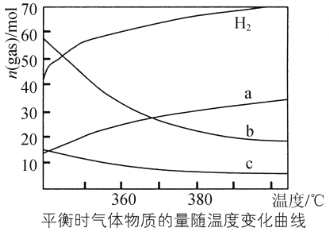
(1)CO2催化加氢能合成低碳烯烃:2CO2(g)+6H2(g) C2H4(g)+4H2O(g)。不同温度下平衡时的四种气态物质的物质的量如图所示,则曲线b表示的物质为________(填化学式)。
C2H4(g)+4H2O(g)。不同温度下平衡时的四种气态物质的物质的量如图所示,则曲线b表示的物质为________(填化学式)。
(2)CO2和H2在催化剂Cu/ZnO作用下可发生两个平行反应,分别生成CH3OH和CO。
反应A:CO2(g)+3H2(g) CH3OH(g)+H2O(g)
CH3OH(g)+H2O(g)
反应B:CO2(g)+H2(g) CO(g)+H2O(g)
CO(g)+H2O(g)
控制CO2和H2初始投料比为1∶3时,温度对CO2平衡转化率及甲醇和CO产率的影响如图所示。
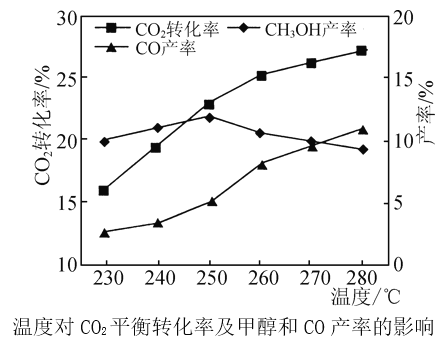
①由图可知温度升高CO的产率上升,其主要原因可能是_____。
②由图可知获取CH3OH最适宜的温度是________,下列措施有利于提高CO2转化为CH3OH的平衡转化率的有________(填字母)。
A. 使用催化剂
B. 增大体系压强
C. 增大CO2和H2的初始投料比
D. 投料比和容器体积不变,增加反应物的浓度
(3)在恒温恒容条件下,反应A达到平衡的标志有_____
A. 容器中气体压强不再发生变化
B. 容器中气体密度不再发生变化
C. 容器中气体颜色不再发生变化
D. 容器中气体平均摩尔质量不再发生变化
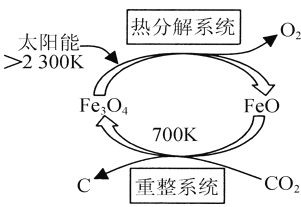
(4)由CO2制取C的太阳能工艺如图所示。“热分解系统”发生的反应为2Fe3O4 6FeO+O2↑,每分解1 mol Fe3O4转移电子的物质的量为_____;“重整系统”发生反应的化学方程式为___。
6FeO+O2↑,每分解1 mol Fe3O4转移电子的物质的量为_____;“重整系统”发生反应的化学方程式为___。
-
CO2是一种廉价的碳资源,CO2及碳的其他化合物综合利用具有重要意义
回答下列问题:
(1)CO2与CH4经催化重整制得合成气:CH4(g)+C02(g)  2CO(g)+2H2(g)ΔH=+120kJ·mol-1有利于提高CH4平衡转化率的条件是_______(填标号)
2CO(g)+2H2(g)ΔH=+120kJ·mol-1有利于提高CH4平衡转化率的条件是_______(填标号)
A高温低压 B.低温高压 C.高温高压 D.低温低压
(2)以甲烷为燃料的新型燃料电池,目前已得到了广泛的研究,如图是甲烷燃料电池原理示意图,回答下列问题:

电池的负极是_______(填“a”或“b”)电极,该极的电极反应式为____________________________
(3)CO2可以被NaOH溶液捕获,若所得溶液c(HCO3-):c(CO32-)=2:1,溶液pH=__________(室温下,H2CO3的K1=4×10-7,,K2=5×10-11) 0.1mol/L NaHCO3溶液中阴离子的浓度由大到小的顺序为_____________________________________
(4)已知25oC,H2SO3的Ka1=1.3×10-2Ka2=6.2×10-8,将SO2通入氨水中,当c(OH-)降至1.0×10-7mol/L时,溶液中 的c(SO32-)/c(HSO3-)=________________
-
“低碳经济”已成为全世界科学家研究的重要课题,其综合利用具有重要意义。回答下列问题:
(1)CO2与CH4经催化重整,制得合成气:CH4(g)+ CO2(g) 2CO (g)+ 2H2(g)
2CO (g)+ 2H2(g)
①已知上述反应中相关的化学键键能数据如下:
| 化学键 | C—H | C=O | H—H | C O(CO) O(CO) |
| 键能/kJ·mol−1 | 413 | 745 | 436 | 1075 |
则该反应的ΔH=_________。有利于提高CH4平衡转化率的条件是____(填标号)。
A.高温低压 B.低温高压 C.高温高压 D.低温低压
②某温度下,在体积为2 L的容器中加入2 mol CH4、1 mol CO2以及催化剂进行重整反应,达到平衡时CO2的转化率是50%,其平衡常数为_______mol2·L-2。
(2)CO2可以被NaOH溶液捕获。若所得溶液c(HCO3−)∶c(CO32 -)=2∶1,溶液pH=____。(室温下,H2CO3的K1=4×10-7;K2=5×10-11),0.1mol·L-1 NaHCO3溶液中阴离子的浓度由大到小的顺序为______________
(3)研究证实,CO2也可在酸性水溶液中通过电解生成甲醇,则生成甲醇的反应发生在_______极,该电极反应式是___________________________________
-
“低碳经济”已成为全世界科学家研究的重要课题,其综合利用具有重要意义。回答下列问题:
(1)CO2与CH4经催化重整,制得合成气:CH4(g)+ CO2(g) 2CO (g)+ 2H2(g)
2CO (g)+ 2H2(g)
①已知上述反应中相关的化学键键能数据如下:
| 化学键 | C—H | C=O | H—H | C O(CO) O(CO) |
| 键能/kJ·mol−1 | 413 | 745 | 436 | 1075 |
则该反应的ΔH=_________。有利于提高CH4平衡转化率的条件是____(填标号)。
A.高温低压 B.低温高压 C.高温高压 D.低温低压
②某温度下,在体积为2 L的容器中加入2 mol CH4、1 mol CO2以及催化剂进行重整反应,达到平衡时CO2的转化率是50%,其平衡常数为_______mol2·L-2。
(2)CO2可以被NaOH溶液捕获。若所得溶液c(HCO3−)∶c(CO32 -)=2∶1,溶液pH=____。(室温下,H2CO3的K1=4×10-7;K2=5×10-11),0.1mol·L-1 NaHCO3溶液中阴离子的浓度由大到小的顺序为______________
(3)研究证实,CO2也可在酸性水溶液中通过电解生成甲醇,则生成甲醇的反应发生在_______极,该电极反应式是___________________________________
-
CH4-CO2催化重整可以得到合成气(CO和H2),有利于减小温室效应,其主要反应为CH4(g)+CO2(g)⇌2CO(g)+2H2(g) ΔH=+247 kJ·mol−1,同时存在以下反应:积碳反应:CH4(g)⇌C(s)+2H2(g) ΔH=+75 kJ·mol−1,消碳反应:CO2(g)+C(s)⇌2CO(g) ΔH=+172 kJ·mol−1,积碳会影响催化剂的活性,一定时间内积碳量和反应温度的关系如图。下列说法正确的是
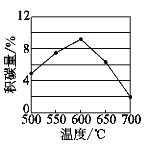
A.高压利于提高 CH4 的平衡转化率并减少积碳
B.增大CO2与CH4的物质的量之比有助于减少积碳
C.升高温度,积碳反应的化学平衡常数K减小,消碳反应的K增大
D.温度高于600℃,积碳反应的化学反应速率减慢,消碳反应的化学反应速率加快, 积碳量减少
-
甲烷作为一种新能源在化学领域应用广泛,请回答下列问题。
(1)高炉冶铁过程中,甲烷在催化反应室中产生水煤气(CO和H2)还原氧化铁,有关反应为:CH4(g)+CO2(g)===2CO(g)+2H2(g) ΔH=260 kJ·mol-1
已知:2CO(g)+O2(g)===2CO2(g)
ΔH=-566 kJ·mol-1。
则CH4与O2反应生成CO和H2的热化学方程式为_________________________________。
(2)如下图所示,装置Ⅰ为甲烷燃料电池(电解质溶液为KOH溶液),通过装置Ⅱ实现铁棒上镀铜。

①a处应通入________(填“CH4”或“O2”),b处电极上发生的电极反应式是__________________________________。
②电镀结束后,装置Ⅰ中溶液的pH________(填写“变大”“变小”或“不变”,下同),装置Ⅱ中Cu2+的物质的量浓度________。
③电镀结束后,装置Ⅰ溶液中的阴离子除了OH-以外还含有________(忽略水解)。
④在此过程中若完全反应,装置Ⅱ中阴极质量变化12.8 g,则装置Ⅰ中理论上消耗甲烷________L(标准状况下)。










