-
已知25℃时,BaCO3、BaSO4的Ksp分别为1×10-9、1×10-10,将1.97gBaCO3固体投入1L某浓度的Na2SO4溶液中(忽略加入固体后溶液体积变化),要实现BaCO3完全转化为BaSO4,Na2SO4溶液的物质的量浓度至少为( )
A.0.1mol/L B.0.11mol/L C.0.011mol/L D.0.01mol/L
高三化学单选题中等难度题查看答案及解析
-
下列实验方案中,不能达到实验目的是( )
选项
实验目的
实验方案
A
验证Ksp(BaSO4) <Ksp(BaCO3)
室温下,将BaSO4投入饱和Na2CO3溶液中充分反应,向过滤后所得固体中加入足量盐酸,固体部分溶解且有无色无味气体产生
B
验证氧化性:Br2>I2
将少量溴水加入KI溶液中,再加入CCl4,震荡,静止,可观察到下层液体呈紫色
C
验证酸性:HCN<CH3COOH
室温下,用pH试纸测得0.100 mol·L-1 CH3COOH溶液的pH值约为3,0.100 mol·L-1 HCN溶液的pH值约为5
D
验证Fe3+能催化H2O2分解,且该分解反应为放热反应
向FeCl3溶液中滴入几滴30%的H2O2溶液,有气体产生,一段时间后,FeCl3溶液颜色加深
A. A B. B C. C D. D
高三化学单选题困难题查看答案及解析
-
已知BaCO3、BaSO4溶度积常数分别为Ksp=5.1×10-9 mol2·L-2,Ksp=1.1×10-10 mol2·L-2,则BaSO4可作钡餐,BaCO3不能作钡餐的主要理由是( )
A.BaSO4的溶度积常数比BaCO3的小
B.S没有毒性,C有毒性
C.BaSO4的密度大
D.胃酸能与C结合,生成CO2和H2O,使BaCO3的溶解平衡向右移动,Ba2+浓度增大,造成人体Ba2+中毒
高三化学选择题中等难度题查看答案及解析
-
难溶物在水中溶解达到饱和时,即建立沉淀溶解平衡,平衡常数称为溶度积(Ksp).已知25℃时,Ksp(BaSO4)=1×10-10,Ksp(BaCO3)=2.5×10-9.
(1)将浓度均为0.1mol•L-1的BaCl2溶液与Na2SO4溶液等体积混合,充分搅拌后过滤,滤液中c (Ba2+)=______ mol•L-1.
(2)医学上进行消化系统的X射线透视时,常使用BaSO4作内服造影剂,这种透视俗称钡餐透视.请用沉淀溶解平衡原理解释以下问题:
①胃酸很强(pH约为1),但服用大量BaSO4仍然是安全的,BaSO4不溶于酸的原因是______.
②BaCO3不能代替BaSO4作为“钡餐”的原因______.
(3)万一误服了少量BaCO3,应尽快用大量0.5mol•L-1Na2SO4溶液给患者洗胃,如果忽略洗胃过程中Na2SO4溶液浓度的变化,残留在胃液中的Ba2+浓度仅为______mol•L-1.高三化学解答题中等难度题查看答案及解析
-
已知25℃时,Ksp(BaCO3)=8.1×10-9,Ksp(BaSO4)=1.0×10-10,下列说法正确的是( )
A.因为Ksp(BaCO3)>Ksp(BaSO4),所以BaSO4不能转化成BaCO3
B.25℃时,BaCO3要在Na2SO4溶液中开始转化成BaSO4,则Na2SO4的浓度必须不低于1.1×10-6mol·L-1
C.在20mL0.002mol·L-1的Na2SO4溶液中加入20mL0.002mol·L-1的BaCl2溶液,无BaSO4沉淀生成
D.向含有等浓度、等体积的BaCl2溶液的两支试管中同时滴加等浓度的Na2CO3和Na2SO4溶液,先生成BaCO3沉淀
高三化学单选题中等难度题查看答案及解析
-
25℃时,Ksp(BaSO4)=1×10-10,Ksp(BaCO3)=2.6×10-9。该温度下,下列说法不正确的是
A.同浓度的Na2SO4和Na2CO3混合溶液中滴加BaCl2溶液,BaSO4先析出
B.BaCO3的悬浊液中加入少量的新制氯水,c(Ba2+)增大
C.BaSO4和BaCO3共存的悬浊液中,
=
D.BaSO4悬浊液中加入Na2CO3浓溶液,BaSO4不可能转化为BaCO3
高三化学选择题中等难度题查看答案及解析
-
25℃时,Ksp(BaSO4)=1×10-10,Ksp (BaCO3)=2.6×10-9。该温度下,下列说法不正确的是( )
A.同浓度的Na2SO4和Na2CO3混合溶液中滴加BaCl2溶液,BaSO4先析出
B.BaCO3的悬浊液中加入少量的新制氯水,c(Ba2+)增大
C.BaSO4和BaCO3共存的悬浊液中,
D.BaSO4悬浊液中加入Na2CO3浓溶液,BaSO4不可能转化为BaCO3
高三化学单选题中等难度题查看答案及解析
-
某工厂以重晶石(主要含BaSO4)为原料,生产“电子陶瓷工业支柱”—钛酸钡(BaTiO3)
的工艺流程如下:
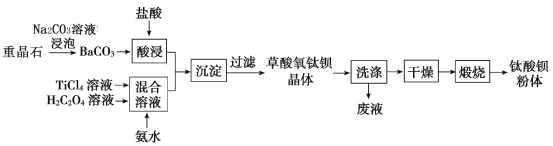
已知:
(1)Ksp(BaSO4)=1.0×10﹣10 ,Ksp(BaCO3)=5.0×10-9
(2)草酸氧钛钡晶体的化学式为 BaTiO(C2O4)2·4H2O
回答下列问题:
(1)为提高BaCO3的酸浸速率,可采取的措施为_________(写出一条)。
(2)配制一定浓度的TiCl4溶液时,通常是将TiCl4(室温下为液体)________________。
(3)用Na2CO3溶液泡重晶石(假设杂质不与Na2CO3溶液作用),待达到平衡后,移走上层清液,重复多次操作,将BaSO4转化为BaCO3,此反应的平衡常数K=______ (填写计算结果)。若不考虑CO32-的水解,则至少需要使用浓度为_____mol/LNa2CO3溶液浸泡重晶石才能开始该转化过程。
(4)设计实验方案验证草酸氧钛钡晶体已经洗涤干净:______________________________。
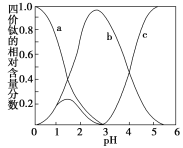
(5)“混合溶液液”环节,钛元素在不同pH下主要以TiOC2O4、TiO(C2O4)22-和TiO(OH)+三种形式存在,如图所示。实际制备工艺中,先用氨水调节混合溶液的pH于2.5~3之间,再进行“沉淀”,则图中曲线a对应钛的形式为_____(填化学式);写出“沉淀”时的离子方程式:___________。
(6)煅烧草酸氧钛钡晶体得到BaTiO3方程式为:__________。
高三化学工业流程中等难度题查看答案及解析
-
已知部分钡盐的溶度积如下:Ksp(BaCO3)=5.1×10-9,Ksp[Ba(IO3)2]=6.5×10-10,Ksp(BaSO4)=1.1×10-10,Ksp(BaCrO4)=1.6×10-10。一种溶液中存在相同浓度的CO
、CrO
、IO
、SO
,且浓度均为0.001 mol·L-1,若向该溶液中逐滴滴入BaCl2溶液,首先发生的离子反应为( )
A. Ba2++CO
===BaCO3↓
B. Ba2++CrO
===BaCrO4↓
C. Ba2++2IO
===Ba(IO3)2↓
D. Ba2++SO
===BaSO4↓
高三化学选择题中等难度题查看答案及解析
-
已知:25 ℃时,Ksp(BaSO4)=1×10-10,Ksp(BaCO3)=1×10-9。
(1)医学上进行消化系统的X射线透视时,常使用BaSO4作内服造影剂。胃酸酸性很强(pH约为1),但服用大量BaSO4仍然是安全的,BaSO4不溶于酸的原因是(用溶解平衡原理解释)____________________。
万一误服了少量BaCO3,应尽快用大量0.5 mol·L-1Na2SO4溶液给患者洗胃,如果忽略洗胃过程中Na2SO4溶液浓度的变化,残留在胃液中的Ba2+浓度仅为________mol·L-1。
(2)长期使用的锅炉需要定期除水垢,否则会降低燃料的利用率。水垢中含有的CaSO4,可先用Na2CO3溶液处理,使之转化为疏松、易溶于酸的CaCO3,而后用酸除去。
①CaSO4转化为CaCO3的离子方程式为____________________________。
②请分析CaSO4转化为CaCO3的原理:____________________________。
高三化学填空题中等难度题查看答案及解析