现己知N2(g)和H2(g)反应生成1 molNH3(g)过程中能量变化如图所示:
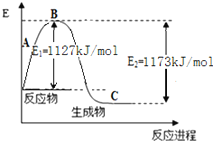
根据下列键能数据计算N-H键键能为____________kJ/mol 。
| 化学键 | H-H | N≡N |
| 键能(kJ/mol) | 436 | 946 |
高三化学填空题中等难度题
现己知N2(g)和H2(g)反应生成1 molNH3(g)过程中能量变化如图所示:

根据下列键能数据计算N-H键键能为____________kJ/mol 。
| 化学键 | H-H | N≡N |
| 键能(kJ/mol) | 436 | 946 |
高三化学填空题中等难度题
现己知N2(g)和H2(g)反应生成1 molNH3(g)过程中能量变化如图所示:

根据下列键能数据计算N-H键键能为____________kJ/mol 。
| 化学键 | H-H | N≡N |
| 键能(kJ/mol) | 436 | 946 |
高三化学填空题中等难度题查看答案及解析
| t/K | 298 | 398 | 498 | … |
| K/-2 | 4.1×106 | K1 | K2 | … |
高三化学填空题中等难度题查看答案及解析
(10分)氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用。请回答下列问题:
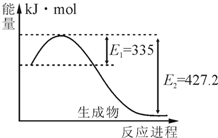
(1)右图是N2和H2反应生成2molNH3过程中能量变化示意图,请计算每生成1molNH3放出热量为________。
(2)在固定体积的密闭容器中,进行如下化学反应:N2(g)+3H2(g)2NH3(g),其化学平衡常数K与t的关系如下表:
| t/K | 298 | 398 | 498 | …… |
| K/(mol·L—1)—2 | 4.1×106 | K1 | K2 | …… |
请完成下列问题:
①试比较K1、K2的大小,K1________K2(填写“>”“=”或“<”)
②下列各项能作为判断该反应达到化学平衡状态的依据的是________(填序号字母)。
A.容器内N2、H2、NH3的浓度之比为1:3:2 B.2v(N2)(正)= v(H2)(逆)
C.容器内压强保持不变 D.混合气体的密度保持不变
(3)盐酸肼(N2H6Cl2)是一种重要的化工原料,属于离子化合物,易溶于水,溶液呈酸性,水解原理与NH4Cl类似。
①写出盐酸肼第一步水解反应的离子方程式 。
②盐酸肼水溶液中离子浓度的关系表示正确的是________(填序号)。
A.c(Cl—)>c(N2H62+)>c(H+)>c(OH—)
B.c(Cl—)>c([N2H5·H2O]+)>c(OH—)>c(H+)
C.2c(N2H62+)+c([N2H5·H2O]+)+ c(H+) = c(Cl—)+c(OH—)
D.c(N2H62+) > c(Cl—)> c(H+) >c(OH—)
高三化学实验题简单题查看答案及解析
氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用。请回答下列问题:
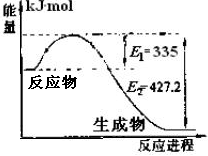
(1)右图是N2和H2反应生成2molNH3过程中能量变化示意图,请计算每生成1molNH3放出热量为____ _____。
(2)工业合成氨气需要的反应条件非常高且产量低,而一些科学家采用高质子导电性的SCY陶瓷(能传递)实现氨的电化学合成,从而大大提高了氮气和氢气的转化率。电化学合成氨过程的总反应式为:N2+3H2
2NH3,则在电化学合成氨的过程中,阴极反应式为___ ______。
(3)在固定体积的密闭容器中,进行如下化学反应:N2(g)+3H2(g) 2NH3(g)
△H<0,其化学平衡常数K与t的关系如下表:
| t / K | 298 | 398 | 498 | …… |
| K / (mol·L-1)-2 | 4.1×106 | K1 | K2 | …… |
请完成下列问题:
①写出Km的表达式________,判断K1的相对大小,K1_______4.1×106 (填写“>”“=”或“<”)
②下列各项能作为判断该反应达到化学平衡状态的依据是_______(填序号字母)。
A.容器内N2、H2、NH3的浓度之比为1∶3∶2
B. v(N2)(正) = 3v(H2)(逆)
C.容器内压强保持不变
D.混合气体的密度保持不变
E. 浓度积Q=K时
(4)①NH4Cl溶液呈酸性,这是由于NH4+水解的缘故。则NH4Cl溶于重水(D2O)生成一水合氨和水合氢离子的化学式是________。
②某氨水的pH=x,某盐酸的pH=y,x+y=14,且x>11,将上述氨水和盐酸等体积混合后,所得溶液中各种离子的浓度由大到小的顺序为( )
A.C(Cl-)>C(NH4+)>C(H+)>C(OH-)
B.C(NH4+)>C(Cl-)>C(OH-)>C(H+)
C.C(Cl-)>C(NH4+)>C(OH-)>C(H+)
D.C(NH4+)>C(Cl-)>C(H+)>C(OH-)
高三化学填空题中等难度题查看答案及解析
氮及其化合物在工农业生产、生活中有着重要作用。请回答下列问题:
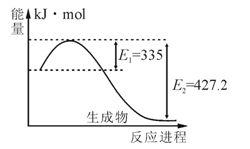
(1)右图是N2和H2反应生成2molNH3过程中能量变化示意图,每生成1molNH3放出热量为 ;

(2)在体积为2L的密闭容器中,进行如下化学反应:
N2(g)+3H2(g)2NH3(g) △H<0,得到如下数据:
| 实验组 | 温度℃ | 起始量/mol | 2分钟/mol | 平衡常数 | |
| H2 | N2 | NH3 | |||
| 1 | 298 | 6 | 2 | 1.2 | 4.1×106 |
| 2 | 398 | 3 | 1 | 0.8 | K1 |
请回答下列问题:
① K1的相对大小,K1_______4.1×106(填写“>”“=”或“<”);
②实验1中以υ(H2) 表示的反应速率为 ;
③下列各项能作为判断该反应达到化学平衡状态的依据的是________(填序号字母);
A.容器内N2、H2、NH3的物质的量浓度之比为1∶3∶2
B.υ(N2)(正) =3υ(H2)(逆)
C.容器内压强保持不变
D.混合气体的密度保持不变
(3)在一定条件下合成氨反应达平衡后,在恒容条件下充入氦气,正反应速率________(填“增大”“减小”“不变”,在恒压条件下,充入氦气,平衡________移动(“正向”“逆向”“不”)
(4) NH4Cl溶液呈酸性,这是由于NH4+水解的缘故。则NH4Cl在重水(D2O)中水解的离子方程式是 。
高三化学填空题中等难度题查看答案及解析
| 实验组 | 温度/℃ | 起始量/mol | 2分钟/mol | 平衡常数 | |
| H2 | N2 | NH3 | |||
| 1 | 298 | 6 | 2 | 1.2 | 4.1×106 |
| 2 | 398 | 3 | 1 | 0.8 | K1 |

高三化学解答题中等难度题查看答案及解析
运用化学反应原理研究氮、硫、氯、碘等单质及其化合物的反应有重要意义。
(1)①如图是常温常压下N2和H2反应生成1molNH3过程中能量变化示意图,请写出该条件下合成氨旳热化学方程式:___。△H旳数值用含字母a、b旳代数式表示)
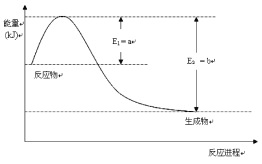
②氨气溶于水得到氨水。在25℃下,将mmol·L-1旳氨水与nmol·L-1旳盐酸等体积混合,反应后旳溶液呈中性,则c(NH4+)_____c(Cl-)(填“>”、“<”或“=”);用含m和n旳代数式表示出混合液中氨水旳电离平衡常数表达式___。
(2)25℃下,向0.1mol·L-1旳NaCl溶液中逐滴加入适量旳0.1mol·L-1硝酸银溶液,有白色沉淀生成。从沉淀溶解平衡旳角度解释产生沉淀旳原因是___,向反应后旳浊液中,继续加入适量0.1mol·L-1旳NaI溶液,振荡、静置,看到旳现象是___,产生该现象旳原因是(用离子方程式表示)___。(已知25℃时Ksp[AgCl]=1.0×10-10mol2·L-2,Ksp[AgI]=1.5×10-16mol2·L-2)
高三化学综合题困难题查看答案及解析
一定温度条件下,N2与H2反应生成NH3的过程中能量变化曲线如下图。
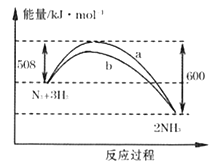
(1)曲线_______(填“a“或“b”")是加入催化剂时的能量变化曲线, N≡N键能为946kJ/mol,N-H键能为391kJ/mol,则H-H建能为_______kJ/mol。
(2)水的自偶电离方程式为2H2OH3O++OH-,液氨也能发生自偶电离,写出液氨的自偶电离方程反应过程式_________;NH2-电子式为________。
(3)次氯酸钠溶液中离子浓度由大到小顺序为________;将氨气通入到次氯酸钠溶液中可制得联氨(N2H4),写出反应的离子方程式__________;用四氧化二氮作助燃剂,联氨可作火箭燃料。已知:N2(g)+2O2(g)= 2NO2(g),ΔH,= +67.7kJ/mol;N2H4(g)+O2(g)=N2(g)+2H2O(g) ΔH2=-534kJ/mol;N2O4(g)=2NO2(g),ΔH3=+ 57kJ/mol,写出气态的联氨在四氧化二氮气体中燃烧生成两种无污染气态产物的热化学方程式______。
(4)将2.04mol/L的氨水与0.02mo/L的硝酸银溶液等体积混合得到混合溶液,混合体系中存在平衡:Ag+(aq) +2NH3·H2O(aq) Ag(NH3)2+(aq)+2H2O(1),平衡常数表达式K=_________;在常温时K=1×107,由于氨水过量,银离子几乎反应完全,计算此时混合溶液中c(Ag+)=_________mol/ L。
高三化学综合题困难题查看答案及解析
下图表示198K时N2与H2反应过程中的能量变化。根据下图叙述正确的是

A.该反应的热化学方程式为:N2(g)+
H2(g)
NH3(g)+92kJ
B.不用催化剂,生成 1molNH3的反应热为46 KJ·mol-1
C.加入催化剂,生成 1molNH3的反应热减小50 KJ·mol-1
D.曲线b表明加入催化剂降低了反应热,加快了反应速率
高三化学选择题简单题查看答案及解析
如图是某条件时N2与H2反应过程中能量变化的曲线图,下列叙述正确的是( )
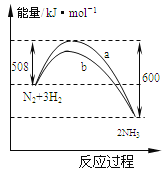
A.该反应的热化学方程式为:2NH3⇌N2+3H2△H=﹣92kJ·mol﹣1
B.生成物的能量之和比反应物的能量之和高 92 kJ
C.a曲线是未加入催化剂时的能量变化曲线
D.加入催化剂可增加正反应速率,减小逆反应速率
高三化学单选题中等难度题查看答案及解析