-
日常饮用水中NO3一的含量是水质卫生检验的重要标准之一,达到一定浓度时会对人类健康产生危害,为了降低饮用水中NO3一的浓度,某兴趣小组提出如下方案:

请回答下列问题:
(1)该方案在调节pH时,若pH过大或过小都会造成 ________的利用率降低。
(2)已知过滤后得到的滤液中几乎不含铝元素。①在溶液中铝粉和NO3一反应的离子方程式为________。
②滤渣在空气中煅烧过程中涉及的相关反应方程式为________
(3)用H2催化还原法也可降低饮用水中NO3—的浓度,已知反应中的还原产物和氧化产物均可参与大气循环,则催化还原法的离子方程式为________。
(4)饮用水中的NO3- 主要来自于NH4+。已知在微生物作用下,NH4+ 经过两步反应被氧化成NO3- 。两步反应的能量变化示意图如下:
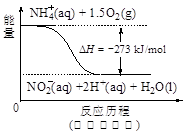

试写出1 mol NH4+ (aq)全部氧化成NO3- (aq)的热化学方程式是________。
(5)固体a熔融电解时阴极反应式为________
-
饮用水中NO3- 达到一定浓度时会对人类健康产生危害,为了降低饮用水中NO3 -的浓度,某兴趣小组提出如下方案:
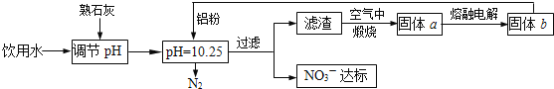
请回答下列问题:
(1)该方案中选用熟石灰调节 pH,理由是_______、__________、________, 在调节pH时,若pH过大或过小都会造成________的利用率降低。
(2)已知过滤后得到的滤渣是Al和Al(OH)3,则在溶液中铝粉和NO3-反应的离子方程式为____________________________________ 。
(3)用H2催化还原法也可降低饮用水中NO3-的浓度,已知反应中的还原产物和氧化产物 均可参与大气循环,则催化还原法的离子方程式为____________________________________ 。
(4)饮用水中的NO3-主要来自于NH4+。已知在微生物作用下,NH4+经过两步反应被氧化 成NO3-。两步反应的能量变化示意图如下:
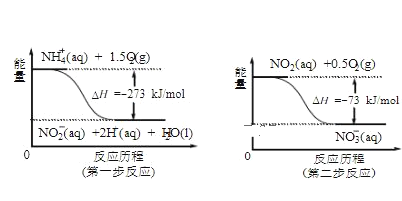
试写出1molNH4+(aq)全部氧化成NO3-(aq)的热化学方程式是__________________________。
-
饮用水中含有一定浓度的NO3﹣将对人类健康产生危害,NO3﹣能氧化人体血红蛋白中的Fe(Ⅱ),使其失去携氧功能.为了降低饮用水中NO3﹣的浓度,某兴趣小组提出如下方案:
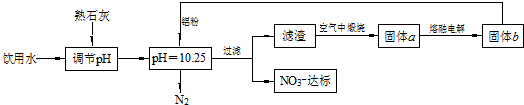
请回答下列问题:
(1)该方案中选用熟石灰调节pH时,若pH过大或过小都会造成 的利用率降低.
(2)已知过滤后得到的滤渣是一种混合物,该混合物的主要成份是 (填化学式).
(3)用H2催化还原法也可降低饮用水中NO3﹣的浓度,已知反应中的还原产物和氧化产物均可参与大气循环,则催化还原法的离子方程式为 .
(4)饮用水中的NO3﹣主要来自于NH4+.已知在微生物作用的条件下,NH4+经过两步反应被氧化成NO3﹣.两步反应的能量变化示意图如下:

试写出1mol NH4+ (aq)全部氧化成NO3﹣(aq)的热化学方程式是 .
-
(12分)饮用水中含有一定浓度的NO3一将对人类健康产生危害,NO3一能氧化人体血红蛋白中的Fe(II),使其失去携氧功能。为了降低饮用水中NO3一的浓度,某兴趣小组提出如下方案:

请回答下列问题:
(1)已知过滤后得到的滤渣是一种混合物,则在溶液中铝粉和NO3一反应的离子方程式为 。
(2)该方案中选用熟石灰调节pH,理由是 、 ,在调节pH时,若pH过大或过小都会造成 的利用率降低。
(3)用H2催化还原法也可降低饮用水中NO3-的浓度,已知反应中的还原产物和氧化产物均可参与大气循环,则催化还原法的离子方程式为 _。
(4)饮用水中的NO3-主要来自于NH4+。已知在微生物作用的条件下,NH4+经过两步反应被氧化成NO3-。两步反应的能量变化示意图如下:
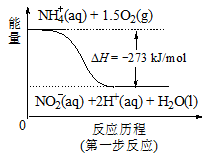

试写出1 mol NH4+ (aq)全部氧化成NO3-(aq)的热化学方程式是 。
-
(12分)饮用水中含有一定浓度的NO3一将对人类健康产生危害,NO3一能氧化人体血红蛋白中的Fe(II),使其失去携氧功能。为了降低饮用水中NO3一的浓度,某兴趣小组提出如下方案:

请回答下列问题:
⑴已知过滤后得到的滤渣是一种混合物,则在溶液中铝粉和NO3一反应的离子方程式为
__________________________________________。
⑵该方案中选用熟石灰调节pH,理由是_______________________、__________________,在调节pH时,若pH过大或过小都会造成________的利用率降低。
⑶用H2催化还原法也可降低饮用水中NO3-的浓度,已知反应中的还原产物和氧化产物均可参与大气循环,则催化还原法的离子方程式为____________________________________。
⑷饮用水中的NO3- 主要来自于NH4+。已知在微生物作用的条件下,NH4+ 经过两步反应被氧化成NO3- 。两步反应的能量变化示意图如下:

试写出1 mol NH4+ (aq)全部氧化成NO3- (aq)的热化学方程式是________。
-
饮用水中含有一定浓度的NO3-将对人类健康产生危害,NO3-能氧化人体血红蛋白中的Fe(II),使其失去携氧功能.为了降低饮用水中NO3-的浓度,某兴趣小组提出如图甲方案:

请回答下列问题:
(1)已知过滤后得到的滤渣是一种混合物,则在溶液中铝粉和NO3-反应的离子方程式为______.
(2)该方案中选用熟石灰调节pH,理由是______、______,在调节pH时,若pH过大或过小都会造成______的利用率降低.
(3)用H2催化还原法也可降低饮用水中NO3-的浓度,已知反应中的还原产物和氧化产物均可参与大气循环,则催化还原法的离子方程式为______ N2+4H2O+2OH-
-
(6分)饮用水中的NO3-对人类健康会产生危害,为了降低饮用水中NO的浓度,某兴趣小组提出以下两种方案:
a.在微碱性条件下,用Fe(OH)2还原NO3-,还原产物为NH3;
b.在碱性条件下,用铝粉还原NO3-,还原产物为N2。
(1)方案a中,生成34g NH3的同时生成__________mol Fe(OH)3。
(2)方案b中发生的反应如下(配平该反应离子方程式):
______Al+______NO3-+______OH-===______AlO2-+______N2↑+______H2O
(3)方案b中,当有0.15 mol电子转移时,生成的氮气在标准状况下的体积为_________mL。
-
(一)饮用水中的NO3-对人类健康会产生危害,为了降低饮用水中NO3-的浓度,某饮用水研究人员提出,在碱性条件下用铝粉将NO3-还原为 N2,请配平化学方程式:10Al+6NaNO3 + 4NaOH + 18H2O === 10 ________ + 3N2↑。若反应过程中转移5mol电子,则生成标况下的N2体积为________ L。
N2,请配平化学方程式:10Al+6NaNO3 + 4NaOH + 18H2O === 10 ________ + 3N2↑。若反应过程中转移5mol电子,则生成标况下的N2体积为________ L。
(二)化工生产盐酸的主要过程如图1所示:

其中关键的一步为图2所示的氯气和氢气在燃烧管口燃烧,生成HCl。氯气有毒,为防止污染大气,为此通入气体的合理方式是:A处通入_______,B处通入______;同时应采取的措施是___ __。
(三)已知氰(CN)2、硫氰(SCN)2和(OCN)2、ICl、BrCl的性质与卤素单质相似,故称它们为拟卤素。回答下列问题。
(1)写出硫氰(SCN)2的结构式 。
(2)(CN)2和KOH溶液反应的化学方程式为:______________。
(3)已知阴离子的还原性强弱为:Cl-<Br-<CN-<SCN-<I-。试写出在NaBr和KSCN的混合溶液中加入(CN)2反应的离子方程式:____________________________。
-
饮用水中的NO3-对人类健康会产生危害,为了降低饮用水中NO3-的浓度,某饮用水研究人员提出,在碱性条件下用铝粉将NO3-还原为N2,请配平化学方程式:10Al+6NaNO3+4NaOH+18H2O=10______+3N2↑+2H2O若反应过程中转移5 mol电子,则生成标况下的N2体积为______L.
-
某工厂排放出有毒物质NOCl,它遇水就会生成NO3-,NOCl分子中各原子均满足8 电子稳定结构,则NOCl的电子式为______。水源中的NO3-对人类健康会产生危害。为了降低水源中NO3-的浓度,有研究人员建议在碱性条件下用铝粉将NO3-还原为N2,该反应的离子方程式为______。













