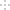-
(13分)X、Y、Z、R为前四周期元素,原子序数依次增大。X、Y同周期,X基态原子的最外层电子数是次外层的2倍,Y基态原子的s能级和p能级上电子数相等;Z是地壳中含量最高的金属元素;R+离子的3d轨道全充满。
请回答下列问题:
(1)Z3+离子的核外电子排布式是 。
(2)科学家成功地在高压下将XY2 转化为具有类似SiO2结构的原子晶体,该晶体中X原子的杂化轨道类型是 ;X、Z、R的单质分别与足量Y2充分反应所得产物的熔点由高到低的顺序是 。(填化学式)
(3)由Y、R形成的某化合物的晶胞结构如图所示,其化学式是 。
(4)常温下,pH相同的NaZY2与Na2XY3两种溶液,物质的量浓度较大的是 。(填化学式)
(5)将亚硫酸钠的水溶液逐滴加入RCl2的水溶液中,再加入少量浓盐酸混匀,得到难溶的白色沉淀RCl,该反应的离子方程式是 。
-
X、Y、Z、R为前四周期元素,原子序数依次增大。X、Y同周期,X基态原子的最外层电子数是次外层的2倍,Y基态原子的s能级和p能级上电子数相等;Z是地壳中含量最高的金属元素;R+离子的3d轨道全充满。请回答下列问题:
(1)Z3+离子的核外电子排布式是_______。
(2)科学家成功地在高压下将XY2转化为具有类似SiO2结构的原子晶体,该晶体中X原子的杂化轨道类型是_______;X、Z、R的单质分别与足量Y2充分反应所得产物的熔点由高到低的顺序是_______。(填化学式)
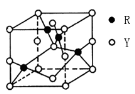
(3)由Y、R形成的某化合物的晶胞结构如图所示,其化学式是_______。
(4)常温下,pH相同的NaZY2与Na2XY3两种溶液,物质的量浓度较大的是_______。(填化学式)
(5)将亚硫酸钠的水溶液逐滴加入RCl2的水溶液中,再加入少量浓盐酸混匀,得到难溶的白色沉淀RCl,该反应的离子方程式是_______。
-
X、Y、Z、R为前四周期元素,原子序数依次增大。X、Y同周期,X基态原子的最外层电子数是次外层的2倍,Y基态原子的s能级和p能级上电子数相等;Z是地壳中含量最高的金属元素;R+离子的3d轨道全充满。请回答下列问题:
(1)Z3+离子的核外电子排布式是_______。
(2)科学家成功地在高压下将XY2转化为具有类似SiO2结构的原子晶体,该晶体中X原子的杂化轨道类型是_______;X、Z、R的单质分别与足量Y2充分反应所得产物的熔点由高到低的顺序是_______。(填化学式)
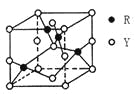
(3)由Y、R形成的某化合物的晶胞结构如图所示,其化学式是_______。
(4)常温下,pH相同的NaZY2与Na2XY3两种溶液,物质的量浓度较大的是_______。(填化学式)
(5)将亚硫酸钠的水溶液逐滴加入RCl2的水溶液中,再加入少量浓盐酸混匀,得到难溶的白色沉淀RCl,该反应的离子方程式是_______。
-
X、Y、Z、R为前四周期元素,原子序数依次增大。X、Y同周期,X基态原子的最外层电子数是次外层的2倍,Y基态原子的s能级和p能级上电子数相等;Z是地壳中含量最高的金属元素;R+离子的3d轨道全充满。请回答下列问题:
(1)Z3+离子的核外电子排布式是_______。
(2)科学家成功地在高压下将XY2转化为具有类似SiO2结构的原子晶体,该晶体中X原子的杂化轨道类型是_______;X、Z、R的单质分别与足量Y2充分反应所得产物的熔点由高到低的顺序是_______。(填化学式)
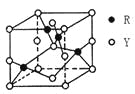
(3)由Y、R形成的某化合物的晶胞结构如图所示,其化学式是_______。
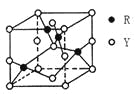
(4)常温下,pH相同的NaZY2与Na2XY3两种溶液,物质的量浓度较大的是_______。(填化学式)
(5)将亚硫酸钠的水溶液逐滴加入RCl2的水溶液中,再加入少量浓盐酸混匀,得到难溶的白色沉淀RCl,该反应的离子方程式是_______。
-
A、B、C、D、E、F为前四周期元素且原子序数依次增大,其中基态A原子的电子分布在3个能级,且每个能级所含的电子数相同;C的原子核外最外层有 6 个运动状态不同的电子;D是短周期元素中电负性最小的元素;E的最高价氧化物的水化物酸性最强;基态F原子核外最外层只有一个电子,其余能层均充满电子。G元素与D元素同主族,且相差3个周期。
(1)元素 A、 B、 C 的第一电离能由小到大的是__________________(用元素符号表示)。
(2)E的最高价含氧酸中 E 原子的杂化方式为_____________。 基态 E 原子中,核外电子占据最高能级的电子云轮廓形状为_________________。
(3)F原子的外围电子排布式为_______________________,
(4)已知元素 A、B形成的(AB)2分子中所有原子都满足 8电子稳定结构,则其分子中 σ键与 π键数目之比为__________。
(5)通常情况下,D单质的熔沸点比G单质高,原因是_________________________。
(6)已知 DE 晶体的晶胞如图所示:
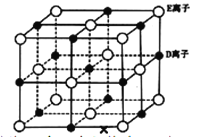
若将 DE 晶胞中的所有 E 离子去掉,并将 D 离子全部换为 A 原子,再在其中的 4 个“小立方体”中心各放置一个A 原子,且这 4 个“小立方体”不相邻。位于“小立方体”中的 A 原子与最近的 4 个 A 原子以单键相连,由此表示 A的一种晶体的晶胞(已知 A—A 键的键长为a cm, NA表示阿伏加德罗常数),则该晶胞中含有_________个 A 原子,该晶体的密度是_______g·cm-3(列式表示)。
-
a、b、c、d、e、f是前四周期原子序数依次增大的6种元素,a元素的基态原子核外s能级上的电子数是p能级上电子数的2倍;c元素原子的最外层电子数是次外层电子数的3倍;d是地壳中含量最高的金属元素;e的正三价基态离子的d能级为半充满结构;f的基态原子最外层只有一个电子,且内层电子排布均为全充满结构。
(1)b元素基态原子的价电子排布图为________。
(2)a、b、c三种元素的第一电离能由大到小的顺序为_________。(用元素符号回答)
(3)b与c组成的一种分子甲中有16个价电子,甲分子与______(填写一种物质的分子式)是等电子体,甲分子中σ键和π键的数目比是______。
(4)c的氢化物中,电子总数为18的分子是乙,乙中c原子的杂化方式为_______。它是______分子(填“极性”或“非极性”)
(5)已知c、f能形成两种化合物,其晶胞如图所示,甲的化学式为_________。高温时,甲易转化为乙的原因为_________。

(6)e元素对应的单质在形成晶体时,采用如图所示的堆积方式_________。则这种堆积模型的配位数为,如果e的原子半径为 r pm;阿伏伽德罗常数的值为NA,计算此单质的密度表达式为_______g/cm3。

-
a、b、c、d、e、f是前四周期原子序数依次增大的6种元素,a元素的基态原子核外s能级上的电子数是p能级上电子数的2倍;c元素原子的最外层电子数是次外层电子数的3倍;d是地壳中含量最高的金属元素;e的正三价基态离子的d能级为半充满结构;f的基态原子最外层只有一个电子,且内层电子排布均为全充满结构。
(1)b元素基态原子的价电子排布图为________。
(2)a、b、c三种元素的第一电离能由大到小的顺序为_________。(用元素符号回答)
(3)b与c组成的一种分子甲中有16个价电子,甲分子与______(填写一种物质的分子式)是等电子体,甲分子中σ键和π键的数目比是______。
(4)c的氢化物中,电子总数为18的分子是乙,乙中c原子的杂化方式为_______。它是______分子(填“极性”或“非极性”)
(5)已知c、f能形成两种化合物,其晶胞如图所示,甲的化学式为_________。高温时,甲易转化为乙的原因为_________。
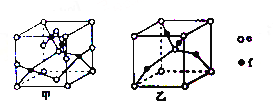
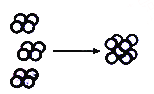
(6)e元素对应的单质在形成晶体时,采用如图所示的堆积方式_________。则这种堆积模型的配位数为,如果e的原子半径为 r pm;阿伏伽德罗常数的值为NA,计算此单质的密度表达式为_______g/cm3。
-
X、Y、Z、W、Q五种元素的原子序数依次增大,X、Y、Z、W属于短周期元素。已知X位于周期表的s区,其原子中电子层数和未成对电子数相同;Y原子核外有三个能级,且每个能级上容纳的电子数相同;W原子最外层电子数是次外层电子数的3倍;Q元素的原子核外有26个运动状态完全不相同的电子。回答下列问题:
(1)仅由X与W组成的含18个电子的分子的结构式为___________。
(2)Y、Z、W中第一电离能最大的是_________(填元素符号),Q的基态原子核外电子排布式为________。
(3)YW32-离子的空间构型是________,其中心原子的杂化轨道类型是__________。
(4)已知由Q、Z、W三种元素按照1:3:9的原子个数比可形成某离子化合物,常温下测得该离子化合物的水溶液pH=2,则该溶液中由水电离产生的c(H+)为_________。
(5)Y的一种单质相对分子质量为720,分子构型为一个32面体,其中有12个五元环,20个六元环(如图1)。则1个这种单质分子中所含π键的数目为____________。
(6)Q元素的单质在形成晶体时,其晶胞如图2所示。则Q原子的配位数为___________,若Q的原子半径为acm,阿伏加德罗常数的值为NA,则该单质的密度为_________g/cm3(不必化简)。
-
现有前四周期元素A、B、C、D、E,原子序数依次增大。A的基态原子核外电子占据3个能级,最外层电子数是电子层数的2倍。基态B原子与A同周期,p能级达到半充满。C原子电子层数与最外层电子数相等。B和E同主族,基态D原子的价层电子排布通式为ns2np1。
请回答下列问题:
(1)基态E原子的价电子排布式为 。
(2)上述5种元素中,电负性最大的元素是 ,lmolAB-中含有 键的数目是 。
键的数目是 。
(3)BO3-的空间构型为 ,写出它的一种等电子体 。
(4)B、C可组成二种新型无机非金属材料CB,具有耐高温,耐磨性能。它的晶体类型为 ,其晶胞与金刚石晶胞相似,已知晶胞边长为apm,则该晶胞的密度为 g/cm3。(用含a、NA的式子表示)。
(5)D、B可组成第三代半导体材料,其晶胞如图所示,它的化学式为 。

-
A、B、C、D、E为五种短周期元素,且原子序数依次增大。其中A、B、C属于同一周期,A原子最外层p能级的电子数等于次外层的电子总数。C原子的最外层中有两个不成对的电子。D、E的原子核内各自的质子数与中子数相等。C可分别与A、B、D、E形成XC2型化合物(X代表A、B、D、E中的一种元素)。已知在DC2和EC2中,D与C的质量之比为7:8;E与C的质量之比为1:1。请回答下列问题:
(1)基态D原子的电子排布式为________,单质B2中 键与
键与 键的数目之比为
键的数目之比为
(2)化合物BH3(H代表氢元素)的立体构型为____,B原子的杂化轨道类型 是________。
(3)C和E的最简单氢化物分别为甲和乙,请比较相同条件下甲、乙的沸点大小,并说明理________。
(4)A可以形成多种结构不同的单质,其中M是所有已知晶体中硬度最大的,其晶体类型是________;若该晶体晶胞(如图所示)的边长为a cm,则其密度是________g·cm -3(只要求列式,不必计算出数值,阿伏加德罗常数为NA)。