-
PCl3是制造有机磷农药和磺胺嘧啶类医药的原料,其制备方法是将熔融黄磷(P4)与干燥氯气进行氯化反应。
(1) PCl3遇水会强烈水解,写出PCl3与水反应的化学方程式:________。
(2) 制得的PCl3粗产品中常含有POCl3、PCl5等杂质。通过实验测定粗产品中PCl3的质量分数,实验步骤如下(不考虑杂质的反应):
a. 迅速移取20.00 g PCl3粗产品,加水完全水解后,再配成500.00 mL溶液;
b. 量取所配溶液25.00 mL于碘量瓶中,加入0.500 0 mol·L-1碘溶液20.00 mL和1.000 mol·L-1(NH4)3BO3溶液30.00 mL,振荡;
c. 加入2~3滴淀粉溶液,用1.000 0 mol·L-1 Na2S2O3标准溶液滴定过量的碘,滴至终点时消耗Na2S2O3标准溶液12.00 mL。
已知测定过程中的部分反应为H3PO3+H2O+I2 H3PO4+2HI,3HI+(NH4)3BO3===3NH4I+H3BO3,I2+Na2S2O3―→Na2S4O6+NaI(未配平)。
H3PO4+2HI,3HI+(NH4)3BO3===3NH4I+H3BO3,I2+Na2S2O3―→Na2S4O6+NaI(未配平)。
①步骤b中加入(NH4)3BO3溶液的目的是________。
②判断步骤c中滴定终点的方法为________。
③根据上述数据,计算制得粗产品中PCl3的质量分数(写出计算过程)。_________
-
PCl3主要用于制造敌百虫等有机磷农药和磺胺嘧啶(S.D)等医药的原料。如图为实验室中制取粗PCl3产品的装置,夹持装置略去。
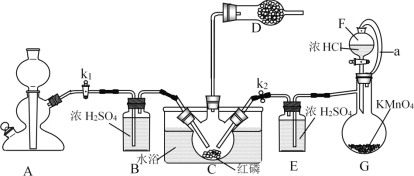
经查阅资料知:红磷与少量Cl2反应生成PCl3,与过量Cl2反应生成PCl5。PCl3遇水会强烈水解生成H3PO3。PCl3遇O2会生成POCl3(三氯氧磷),PCl3、POCl3的熔沸点见下表。
| 物质 | 熔点/℃ | 沸点/℃ |
| PCl3 | -112 | 75.5 |
| POCl3 | 2 | 105.3 |
回答下列问题:
(1)仪器G的名称是______。装置F与G由橡胶管a相连通,a的作用是_______。
(2)A是制取CO2装置,CO2的作用是_____,选择A中的药品是_____(填字母)。
a.稀盐酸 b.稀硫酸 c.NaHCO3粉末 d.块状石灰石
(3)装置D中盛有碱石灰,其作用是__________________。
(4)装置G中生成Cl2,反应的离子方程式为___________。
(5)装置C采用65-70℃水浴加热,制得的PCl3粗产品中常含有POCl3、PCl5等杂质,除杂的方法是:先加入红磷加热,除去PCl5,然后通过___________(填实验操作名称),即可得到较纯净的PCl3。
(6)通过实验测定粗产品中PCl3的质量分数,实验步骤如下(不考虑杂质的反应):
第一步:迅速移取20.0 g PCl3粗产品,加水完全水解后,再配成500mL溶液;
第二步:移取25.00mL溶液置于锥形瓶中;
第三步:加入0. 5mol•L-1碘溶液20 mL,碘过量,H3PO3完全反应生成H3PO4;
第四步:加入几滴淀粉溶液,用1.0 mol•L-1Na2S2O3标准溶液滴定过量的碘,反应方程式为I2+2Na2S2O3=Na2S4O6+2NaI,滴至终点时消耗Na2S2O3标准溶液12mL。
①第三步中反应的化学方程式为_____________。
②根据上述数据,计算该产品中PCl3的质量分数为______%。
-
四氯化锡用作媒染剂和有机合成的氯化催化剂,实验室制备四氯化锡的反应、装置示意图和有关信息如下:
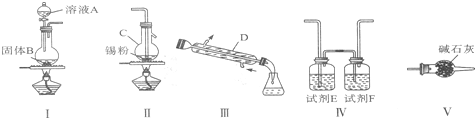
有关信息:
①将金属锡熔融,通入干燥氯气进行反应,生成四氯化锡。
②无水四氯化锡是无色易流动的液体,熔点-33℃,沸点114.1℃。
⑧暴露于空气中与空气中的水分反应生成白烟,有强烈的刺激性,遇水分解。
回答下列问题:
(1)仪器C的名称是 。
(2)制备无水四氯化锡各装置的连接顺序是( )→( )→( )→( )→( )(填装置序号)。
(3)装置V的作用是 。
(4)若无装置V存在,在装置Ⅲ中除生成SnCl4外,还存在的副产物化学式为 。
(5)若Ⅱ中用去锡粉5.95 g,反应后,Ⅲ中锥形瓶里收集到12.0 g SnCl4,则SnCl4的产率为 。
-
(14分)四氯化锡用作媒染剂和有机合成上的氯化催化剂,实验室制备四氯化锡的反应、装置示意图和有关信息数据如下:
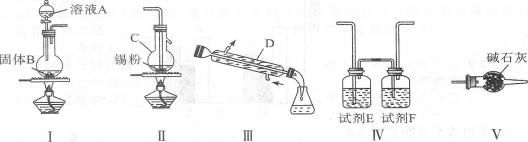
有关信息数据:①将金属锡熔融,通入干燥氯气进行反应。生成四氯化锡。②无水四氯化锡是无色易流动的液体,熔点-33℃,沸点114.1℃。⑧无水四氯化锡暴露于空气中与空气中的水分反应生成白色烟雾。有强烈的刺激性。回答下列问题:
(1)仪器C的名称是 ,仪器D的作用是 。
(2)制备无水四氯化锡各装置的连接顺序是( )一( )一( )一( )一( )(填装置序号)。
(3)试剂E和F分别是 、 ,装置V的作用是 。
(4)若无装置V存在,在装置Ⅲ中除生成SnCl4外,还存在的副产物的化学式为 。
(5)实验制得的SnCl4中因溶解了C12而略显黄色,提纯SnCl4的方法是 。
(6)若Ⅱ中用去锡粉5.95 g.反应后,Ⅲ中锥形瓶里收集到12.0 g SnCl4,则SnCl4的产率为 (结果保留三位有效数字)。
-
四氯化锡可用作媒染剂、有机合成中氯化的催化剂等。实验室制备四氯化锡所需的有关装置和信息如下:
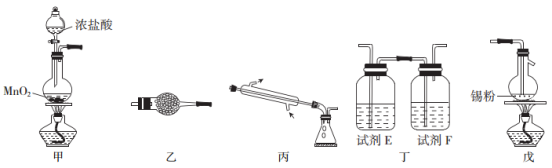
有关信息:①将金属锡熔融,通入干燥氯气进行反应,生成四氯化锡;②无水四氯化锡是无色易流动的液体,熔点-33℃,沸点114.1℃;③四氯化锡易水解。
回答下列问题:
(1)装置甲中反应容器的名称是____________;试剂E和F分别是___________、____________。
(2)装置甲中发生反应的化学方程式为_____________________;
装置戊中发生反应的化学方程式为______________________。
(3)上述各装置的连接顺序是甲→_________→___________→_________(填装置标号),实验开始时点燃的酒精灯是_________(填“甲”或“戊”)。
(4)装置乙的作用是______________________________。
(5)实验所得SnCl4中因溶解了Cl2而略显黄色,提纯SnCl4的方法是__________(填标号)。
a.用NaOH溶液洗涤 b.升华 c.重结晶 d.蒸馏 e.过滤 f.萃取
(6)四氯化锡暴露于空气中与空气中水分反应生成白烟,有强烈的刺激性,原因是___________(用化学方程式表示)。
-
(13分) 四氯化锡可用作媒染剂、有机合成中氯化的催化剂等。实验室制备四氯化锡所需的有关装置和信息如下:
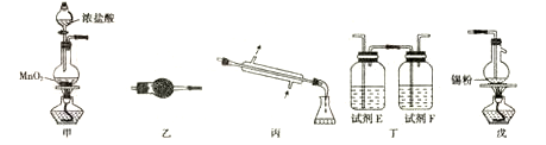
有关信息:①将金属锡熔融,通入干燥氯气进行反应,生成四氯化锡;②无水四氯化锡是无色易流动的液体,熔点-33℃,沸点114,1℃;③四氯化锡易水解。
回答下列问题:
(1)装置丁的名称是 ;试剂E和F分别是____、____。
(2)装置甲中发生反应的化学方程式为____;装置戊中发生反应的化学方程式为____。
(3)上述各装置的连接顺序是甲一→ 一→ 一→ (填装置标号),实验开始时点燃的酒精灯是 (填“甲”或“戊”)。
(4)装置乙的作用是 。
(5)实验所得SnCl4中因溶解了Cl2而略显黄色,提纯SnCl4的方法是 (填标号)。
a.用NaOH溶液洗涤
b.升华
c.重结晶
d.蒸馏
e.过滤
f.萃取
(6)四氯化锡暴露于空气中与空气中水分反应生成白烟,有强烈的刺激性,原因是 (用化学方程式表示)。
-
四氯化锡可用作媒染剂、有机合成中氯化的催化剂等。实验室制备四氯化锡所需的有关装置和信息如下:
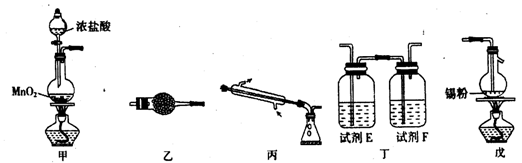
有关信息:①将金属锡熔融,通入干燥氯气进行反应,生成四氯化锡;
②无水四氯化锡是无色易流动的液体,熔点-33℃ ,沸篇114.1℃;
③四氯化锡易水解。
回答下列问题:
(1)装置甲中反应容器的名称是__________;试剂E 和F 分别是________、________。
(2)装置甲中发生反应的化学方程式为_______;装置戊中发生反应的化学方程式为______________。
(3)上述各装置的连接顽序是甲→______→______→______→______(填装置标号),实验开始时点燃的酒精灯是_________(填“甲”或“戊”)。
(4)装置乙的作用是___________。
(5)实验所得SnCl4中因溶解了Cl2而略显黄色,提纯SnCl4的方法是_________(填标号)
A.用Na0H溶液洗涤蒸馏 B.升华 c.重结晶 D.蒸馏 e.过滤 f.萃取
(6)四氯化锡暴露于空气中与空气中水分反应生成白雾,有强烈的刺激性气味,原因是:___________(用化学方程式表示)。
-
四氯化锡(SnCl4) 用作媒染剂和有机合成上的氯化催化剂。实验室制备四氯化锡的装置如下图(部分夹持装置已略去),已知:①金属锡熔融时通入干燥氯气反应可生成四氯化锡;② 无水四氯化锡熔点-33℃,沸点114.1℃;③无水四氯化锡遇水蒸气生成白色烟雾。下列说法不正确的是
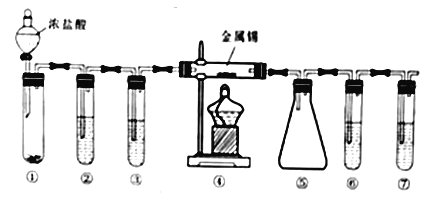
A. 实验时滴加浓盐酸反应一段时间,然后再点燃④处的酒精灯
B. ①、②、⑥、⑦的试管中依次盛装MnO2、饱和食盐水、浓H2SO4、NaOH溶液
C. ⑤装置用于收集SnCl4,浸泡在冷水浴中效果更好
D. ⑥、⑦两个试管可以用一个装有碱石灰的干燥管来代替
-
四氯化锡(SnCl4)用作媒染剂和有机合成上的氯化催化剂。实验室制备四氯化锡的装置如下图(部分夹持装置已略去)。已知:①金属锡熔融时通入干燥氯气反应可生成四氯化锡;②无水四氯化锡熔点-33℃,沸点114.1℃;③无水四氯化锡遇水蒸气生成白色烟雾。下列说法不正确的是
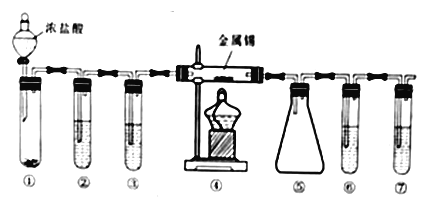
A. ①、②、⑥、⑦的试管中依次盛装MnO2、饱和食盐水、浓H2SO4、NaOH溶液
B. 实验时滴加浓盐酸反应一段时间,然后再点燃④处的酒精灯
C. ⑤装置用于收集SnCl4,浸泡在冷水浴中效果更好
D. ⑥、⑦两个试管可以用一个装有碱石灰的干燥管来代替
-
水合肼作为一种重要的精细化工原料,在农药、医药及有机合成中有广泛用途。用尿素法制备水合肼,可分为两个阶段,第一阶段为低温氯化阶段,第二阶段为高温水解阶段,总反应方程式为:(NH2)2CO +NaClO+2NaOH → H2N—NH2·H2O+NaCl+Na2CO3。
主要副反应:N2H4+2NaClO= N2↑+2H2O+2NaCl △H<0
3NaClO=" 2NaCl" +NaClO3 △H>0
CO(NH2)2 +2NaOH= 2NH3↑+Na2CO3 △H>0
【深度氧化】:(NH2)2CO+3NaClO= N2↑+3NaCl+CO2↑+2H2O △H<0
实验步骤:
步骤1.向30%的NaOH溶液中通入Cl2,保持温度在30℃以下,至溶液显浅黄绿色停止通Cl2。
步骤2.静置后取上层清液,检测NaClO的浓度。
步骤3.倾出上层清液,配制所需浓度的NaClO和NaOH的混合溶液。
步骤4.称取一定质量尿素配成溶液,置于冰水浴。将一定体积步骤3配得的溶液倒入分液漏斗中,慢慢滴加到尿素溶液中,0.5h左右滴完后,继续搅拌0.5h。
步骤5.将步骤4所得溶液,加入5g KMnO4作催化剂,转移到三口烧瓶(装置见图),边搅拌边急速升温,在108℃回流5 min。
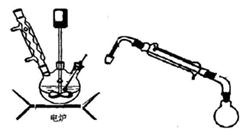
步骤6.将回流管换成冷凝管,蒸馏,收集( 108~114℃)馏分,得产品。
(1)步骤1温度需要在30℃以下,其主要目的是________。
(2)步骤2检测NaClO浓度的目的是________。
a.确定步骤3中需NaClO溶液体积及NaOH质量
b.确定步骤4中冰水浴的温度范围
c.确定步骤4中称量尿素的质量及所取次氯酸钠溶液体积关系
d.确定步骤5所需的回流时间
(3)尿素法制备水合肼,第一阶段为反应________(选填:“放热”或“吸热”)。
(4)步骤5必须急速升温,严格控制回流时间,其目的是________。
(5)已知水合肼在碱性条件下具有还原性(如:N2H4+2I2=N2+4HI)。测定水合肼的质量分数可采用下列步骤:
a.准确称取2.000g试样,经溶解、转移、定容等步骤,配制250mL溶液。
b.移取l0.00 mL于锥形瓶中,加入20mL水,摇匀.
c.用0.l000 mol/L碘溶液滴定至溶液出现微黄色且Imin内不消失,计录消耗碘的标准液的体积。
d.进一步操作与数据处理
①滴定时,碘的标准溶液盛放在________滴定管中(选填:“酸式”或“碱式”)。
②若本次滴定消耗碘的标准溶液为18.00mL,可测算出产品中N2H4-H2O的质量分数为________。
③为获得更可靠的滴定结果,步骤d中进一步操作主要是:________
H3PO4+2HI,3HI+(NH4)3BO3===3NH4I+H3BO3,I2+Na2S2O3―→Na2S4O6+NaI(未配平)。








