-
实验室用软锰矿(主要成分为MnO2)和黄铁矿(主要成分为FeS2)为原料制取Mn2O3和单质硫,其实验流程如下:
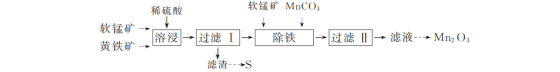
已知:① 在碱性条件下,二价锰以Mn(OH)2形式稳定存在,三价锰以MnOOH形式稳定存在。Mn(OH)2和MnOOH均难溶于水和碱性溶液。
②无水MnSO4晶体熔点700 ℃,在不同温度下它和MnOOH固体受热发生分【解析】
4MnSO4 2Mn2O3+4SO2↑+O2↑;2MnOOH
2Mn2O3+4SO2↑+O2↑;2MnOOH Mn2O3+H2O↑。
Mn2O3+H2O↑。
(1)溶浸过程中生成MnSO4、Fe2(SO4)3及单质S,该反应的化学方程式为________。
(2)室温下,为使杂质离子浓度小于1×10-6mol·L-1,除铁步骤中需调节溶液pH范围为________(已知:Ksp[Fe(OH)2]=1.0×10-16、Ksp[Fe(OH)3]=1.0×10-39,pH=7.1时Mn(OH)2开始沉淀)
(3)为提高Mn2O3的产率,流程中两次过滤操作后均需对滤渣进行洗涤,并________。
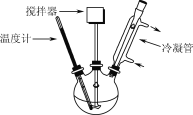
(4)(NH4)2S溶液浸取过滤Ⅰ得到的滤渣时发生反应:(NH4)2S +xS (NH4)2Sx+1,单质硫转化为多硫化铵[(NH4)2Sx+1]转移到液相中。实验时采用过量的饱和(NH4)2S溶液浸取的目的是________。将多硫化铵溶液置于如图所示的装置中,控制在90 ℃条件下分解,单质硫的提取率可达98%。实验中适宜的加热方式为____________________。
(NH4)2Sx+1,单质硫转化为多硫化铵[(NH4)2Sx+1]转移到液相中。实验时采用过量的饱和(NH4)2S溶液浸取的目的是________。将多硫化铵溶液置于如图所示的装置中,控制在90 ℃条件下分解,单质硫的提取率可达98%。实验中适宜的加热方式为____________________。
(5)请补充完整由MnSO4溶液制备较纯净Mn2O3的实验方案:向MnSO4溶液中________,72 h后得到产品Mn2O3。(须使用的试剂:0.2 mol·L-1氨水、3%H2O2溶液、BaCl2溶液、热水)
-
一种用软锰矿(主要成分MnO2)和黄铁矿(主要成分FeS2) 制取MnSO4·H2O并回收单质硫的工艺流程如下:
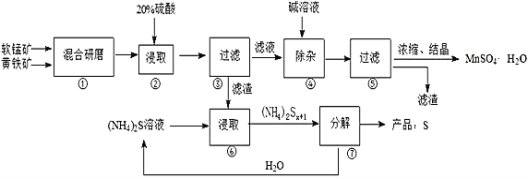
已知:本实验条件下,高锰酸钾溶液与硫酸锰溶液混合产生二氧化锰。
回答下列问题:
(1)步骤①混合研磨成细粉的主要目的是___________________________________;步骤②浸取时若生成S、MnSO4及Fe2(SO4)3的化学方程式为___________________________________。
(2)步骤③所得酸性滤液可能含有Fe2+,为了除去Fe2+可先加入_________________;步骤④需将溶液加热至沸然后在不断搅拌下加入碱调节pH为4-5,再继续煮沸一段时间,“继续煮沸”的目的是_____________________________________。步骤⑤所得滤渣为__________________(填化学式)。
(3)步骤⑦需在90-100℃下进行,该反应的化学方程式________________________。
(4)测定产品MnSO4·H2O的方法之一是:准确称取a g产品于锥形瓶中,加入适量ZnO及H2O煮沸,然后用c mol·L-1KMnO4标准溶液滴定至浅红色且半分钟不褪色,消耗标准溶液VmL,产品中Mn2+的质量分数为w(Mn2+)=________________。
-
一种用软锰矿(主要成分MnO2)和黄铁矿(主要成分FeS2) 制取MnSO4·H2O并回收单质硫的工艺流程如下:
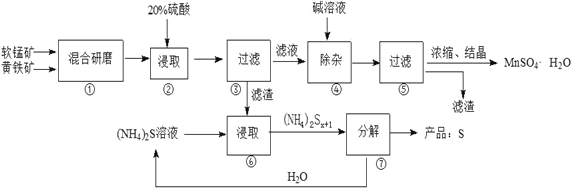
已知:本实验条件下,高锰酸钾溶液与硫酸锰溶液混合产生二氧化锰。
回答下列问题:
(1)步骤①混合研磨成细粉的主要目的是_____________________________________________;步骤②浸取时若生成S、MnSO4及Fe2(SO4)3的化学方程式为_____________________________________。
(2)步骤③所得酸性滤液可能含有Fe2+,为了除去Fe2+可先加入______________________;步骤④需将溶液加热至沸然后在不断搅拌下加入碱调节pH为4~5,再继续煮沸一段时间,“继续煮沸”的目的是_____________________________________。步骤⑤所得滤渣为__________________(填化学式)。
(3)步骤⑦需在90~100℃下进行,该反应的化学方程式为_________________________________。
(4)测定产品MnSO4·H2O的方法之一是:准确称取a g产品于锥形瓶中,加入适量ZnO及H2O煮沸,然后用c mol·L-1KMnO4标准溶液滴定至浅红色且半分钟不褪色,消耗标准溶液VmL,产品中Mn2+的质量分数为w(Mn2+)=________________。
-
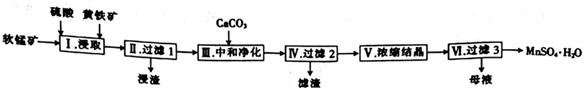
一种以软锰矿(主要成分是MnO2)和黄铜矿(主要成分是FeS2)为原料制取硫酸锰的工艺流程如下:
回答下列问题:
(1)浸取前需将软锰矿和黄铁矿进行粉碎,其目的是_____________________________。
(2)浸取过程中生成硫酸铁和硫酸锰的化学方程式为 _______________________________________。
(3)加入CaCO3发生的反应之一为CaCO3+SO42- CaSO4+ CO32-,该反应的平衡常数K=_________[已知Ksp(CaCO3) =2.7×10-9,Ksp(CaSO4) =9.0×10-6,该工艺中有大量硫酸钙沉淀生成,是因为_________________。
CaSO4+ CO32-,该反应的平衡常数K=_________[已知Ksp(CaCO3) =2.7×10-9,Ksp(CaSO4) =9.0×10-6,该工艺中有大量硫酸钙沉淀生成,是因为_________________。
(4)为提高步骤Ⅵ中锰的回收率,可采取的措施是______________________________________。
-
一种用软锰矿(主要成分MnO2)和黄铁矿(主要成分FeS2)制取MnSO4·H2O并回收单质硫的工艺流程如下:
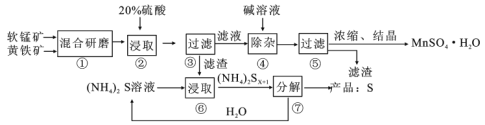
(1)步骤①混合研磨成细粉的主要目的是__________;步骤②浸取时若生成S、MnSO4及Fe2(SO4)3,则反应的离子方程式为___________。
(2)步骤③所得酸性滤液可能含有Fe2+,检验Fe2+的方法是________;除去Fe2+的方法是__________。步骤④是破坏Fe(OH)3胶体并使沉淀颗粒长大,便于过滤分离。步骤⑤所得滤渣为___________(填化学式)。
(3)步骤⑦需在90~100℃下进行,该反应的化学方程式为___________。
(4)硫化铵水解的离子方程式为:S2-+ +H2O
+H2O HS-+NH3·H2O,如何判断溶液的酸碱性______。
HS-+NH3·H2O,如何判断溶液的酸碱性______。
(5)测定产品MnSO4·H2O的方法之一是:准确称取a g产品于锥形瓶中,加入适量ZnO及H2O煮沸,然后用c mol·L-1 KMnO4标准溶液滴定至浅红色且半分钟不褪,消耗标准溶液V mL,滴定反应的离子方程式为2 +3Mn2++2H2O=5MnO2↓+4H+,产品中Mn2+的质量分数为ω(Mn2+)=___________。
+3Mn2++2H2O=5MnO2↓+4H+,产品中Mn2+的质量分数为ω(Mn2+)=___________。
-
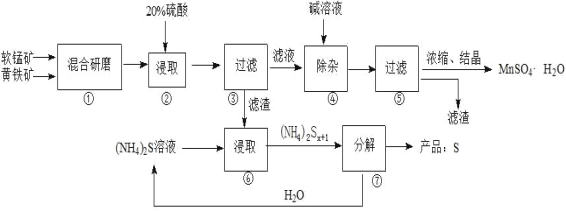
一种用软锰矿(主要成分MnO2)和黄铁矿(主要成分FeS2)制取MnSO4·H2O并回收单质硫的工艺流程如下:
回答下列问题:
(1)步骤①混合研磨成细粉的主要目的是__________________________。
(2)步骤③所得酸性滤液可能含有Fe2+,除去Fe2+可用的方法是__________;步骤④需将溶液加热至沸然后在不断搅拌下加入碱,调节pH 4~5,再继续煮沸一段时间,“继续煮沸”的目的是____________。步骤⑤所得滤渣为___________(填化学式)。
(3)步骤⑦需在90~100℃下进行,该反应的化学方程式为_______________。
(4)测定产品MnSO4·H2O的方法之一是:准确称取a g产品于锥形瓶中,加入适量ZnO及H2O煮沸,然后用c mol·L-1KMnO4标准溶液滴定至浅红色且半分钟不褪,消耗标准溶液V mL,产品中Mn2+的质量分数为w(Mn2+)=_________________。
-
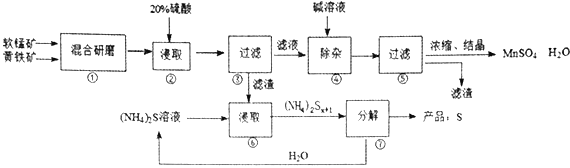
一种用软锰矿(主要成分MnO2)和黄铁矿(主要成分FeS2)制取MnSO4·H2O并回收单质硫的工艺流程如下:
回答下列问题:
(1)步骤②浸取时若生成S、MnSO4及Fe2(SO4)3的化学方程式为______________________。
(2)步骤③所得酸性滤液可能含有Fe2+,除去Fe2+可用的物质是______________________;步骤④需将溶液加热至沸然后在不断搅拌下加入碱调节pH4~5,再继续煮沸一段时间,“继续煮沸”的目的是___________。步骤⑤所得滤渣为___________(填化学式)。
(3)步骤⑦需在90~100℃下进行,该反应的化学方程式为______________________。
(4)测定产品MnSO4·H2O的方法之一是:准确称取ag产品于锥形瓶中,加入适量ZnO及H2O煮沸,然后用 c mol·L-1 KMnO4标准溶液滴定至浅红色且半分钟不褪,消耗标准溶液VmL,滴定反应的离子方程式为_________________________________,产品中Mn2+的质量分数为w(Mn2+)=_________________________________。
-
工业上可用软锰矿(主要成分是MnO2)和黄铁矿(主要成分是FeS2)为主要原料制备高性能磁性材料碳酸锰(MnCO3)。其工业流程如下:
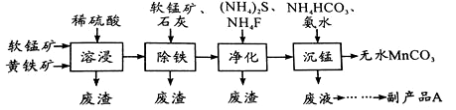
已知:MnCO3难溶于水、乙醇,潮湿时易被空气氧化,100℃开始分解。
回答下列问题:
(1)净化工序的目的是除去溶液中的Cu2+、Ca2+等杂质。若测得滤液中c(F-)=0.01mol/L-1,滤液中残留的c(Ca2+)= 〔已知:Ksp(CaF2)=1.46×10-10〕
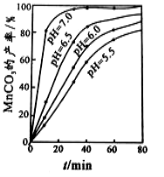
(2)沉锰工序中,298K、c(Mn2+)为1.05 mol/L-1时,实验测得MnCO3的产率与溶液pH、反应时间的关系如图所示。根据图中信息得出的结论是 。
(3)从沉锰工序中得到纯净MnCO3的操作方法是:过滤、 。
(4)为测定某软锰矿中二氧化锰的质量分数,准确称量1.20g软锰矿样品,加入2.68g草酸钠固体,再加入足量的稀硫酸并加热(杂质不参加反应),充分反应后冷却,将所得溶液转移到250mL容量瓶中用蒸馏水稀释至刻度,从中取出25.0mL,用0.0200mol·L-1高锰酸钾溶液进行滴定,当滴入20.0mL溶液时恰好完全反应。
已知高锰酸钾、二氧化锰在酸性条件下均能将草酸钠(Na2C2O4)氧化:
2MnO4- + 5C2O42- + 16H+ =2Mn2+ + 10CO2↑+ 8H2O
MnO2 + C2O42- + 4H+ = Mn2+ + 2CO2↑+ 2H2O
求该软锰矿中二氧化锰的质量分数 (写出计算过程)。
-
工业上可用软锰矿(主要成分是MnO2)和黄铁矿(主要成分是FeS2)为主要原料制备高性能磁性材料碳酸锰(MnCO3)。其工业流程如下:
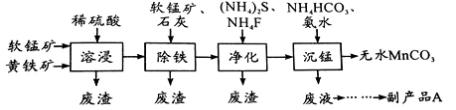
已知:MnCO3难溶于水、乙醇,潮湿时易被空气氧化,100℃开始分解。
回答下列问题:
(1)净化工序的目的是除去溶液中的Cu2+、Ca2+等杂质。若测得滤液中c(F-)=0.01mol/L-1,滤液中残留的c(Ca2+)= 〔已知:Ksp(CaF2)=1.46×10-10〕
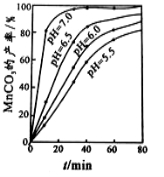
(2)沉锰工序中,298K、c(Mn2+)为1.05 mol/L-1时,实验测得MnCO3的产率与溶液pH、反应时间的关系如图所示。根据图中信息得出的结论是 。
(3)从沉锰工序中得到纯净MnCO3的操作方法是:过滤、 。
(4)为测定某软锰矿中二氧化锰的质量分数,准确称量1.20g软锰矿样品,加入2.68g草酸钠固体,再加入足量的稀硫酸并加热(杂质不参加反应),充分反应后冷却,将所得溶液转移到250mL容量瓶中用蒸馏水稀释至刻度,从中取出25.0mL,用0.0200mol·L-1高锰酸钾溶液进行滴定,当滴入20.0mL溶液时恰好完全反应。
已知高锰酸钾、二氧化锰在酸性条件下均能将草酸钠(Na2C2O4)氧化:
2MnO4- + 5C2O42- + 16H+ == 2Mn2+ + 10CO2↑+ 8H2O
MnO2 + C2O42- + 4H+ == Mn2+ + 2CO2↑+ 2H2O
求该软锰矿中二氧化锰的质量分数 (写出计算过程)。
-
工业上可用软锰矿(主要成分是MnO2)和黄铁矿(主要成分是FeS2)为主要原料制备高性能磁性材料碳酸锰(MnCO3)。其工艺流程如下:( )
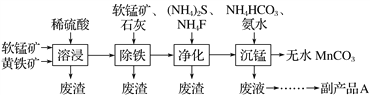
已知:净化工序的目的是除去溶液中的Ca2+、Cu2+等杂质(CaF2难溶)。
下列说法不正确的是
A. 研磨矿石、适当升高温度均可提高溶浸工序中原料的浸出率
B. 除铁工序中,在加入石灰调节溶液的pH前,加入适量的软锰矿,发生的反应为MnO2+2Fe2++4H+===2Fe3++Mn2++2H2O
C. 副产品A的化学式(NH4)2S
D. 从沉锰工序中得到纯净MnCO3的操作方法是过滤、洗涤、干燥

2Mn2O3+4SO2↑+O2↑;2MnOOH
Mn2O3+H2O↑。

(NH4)2Sx+1,单质硫转化为多硫化铵[(NH4)2Sx+1]转移到液相中。实验时采用过量的饱和(NH4)2S溶液浸取的目的是________。将多硫化铵溶液置于如图所示的装置中,控制在90 ℃条件下分解,单质硫的提取率可达98%。实验中适宜的加热方式为____________________。










