-
室温下,用0.10 mol·L-1KOH溶液滴定10.00 mL 0.10 mol·L-1H2C2O4(二元弱酸)溶液所得滴定曲线如图(混合溶液的体积可看成混合前溶液的体积之和)。请回答下列问题:

(1)点①所示溶液中,Kw=__________。
(2)点②所示溶液中的电荷守恒式为______________________________________。
(3)点③所示溶液中存在________种平衡。
(4)点④所示溶液中的物料守恒式为0.10 mol·L-1=___________________________。
(5)点⑤所示溶液中各离子浓度的大小顺序为________________________________。
(6)上述5点所示溶液中,水的电离程度最大的是_______,最小的是________(用序号回答)。
-
室温下,用0.10 mol·L-1KOH溶液滴定10.00 mL 0.10 mol·L-1H2C2O4(二元弱酸)溶液所得滴定曲线如图(混合溶液的体积可看成混合前溶液的体积之和)。请回答下列问题:
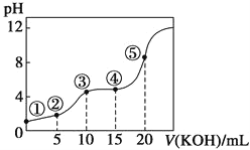
(1)点①所示溶液中,Kw=__________。
(2)点②所示溶液中的电荷守恒式为______________________________________。
(3)点③所示溶液中存在________种平衡。
(4)点④所示溶液中的物料守恒式为0.10 mol·L-1=___________________________。
(5)点⑤所示溶液中各离子浓度的大小顺序为________________________________。
(6)上述5点所示溶液中,水的电离程度最大的是_______,最小的是________(用序号回答)。
-
室温下,用0.10mol/LKOH溶液滴定10.00mL0.10mol/LH2C2O4(二元弱酸)溶液,所得滴定曲线如图(混合溶液的体积可看成混合前溶液的体积之和)。请回答:
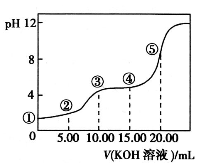
(1)点①所示溶液中,Kw=_____________。
(2)点②所示溶液中的电荷守恒式为_____________________。
(3)点③所示溶液中所有离子的浓度由大到小的顺序为___________________。
(4)点④所示溶液中的物料守恒式为0.10mol/L=___________。
-
常温下,用0.10 mol·L-1 KOH溶液滴定10.00 mL 0.10 mol·L-1H2C2O4(二元弱酸)溶液所得滴定曲线如图(混合溶液的体积可看成混合前溶液的体积之和)。下列说法正确的是( )
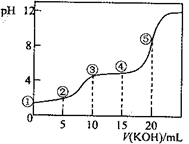
A.点①所示溶液中: c(H+)/c(OH—)=1012
B.点②所示溶液中:c(K+)+c(H+)=c(HC2O4—)+c(C2O42-)+c(OH—)
C.点③所示溶液中:c(K+)>c(HC2O4—)>c(H2C2O4)>c(C2O42-)
D.点④所示溶液中:c(K+)+ c(H2C2O4)+ c(HC2O4—) +c(C2O42-)=0.10mol·L-1
-
常温下,用0.10 mol·L-1 KOH溶液滴定10.00 mL 0.10 mol·L-1H2C2O4(二元弱酸)溶液所得滴定曲线如图(混合溶液的体积可看成混合前溶液的体积之和)。下列说法正确的是
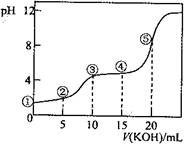
A.点①所示溶液中: c(H+)/c(OH—)=1012
B.点②所示溶液中: c(K+)+c(H+)=c(HC2O4—)+c(C2O42-)+c(OH—)
C.点③所示溶液中:c(K+)>c(HC2O4—)> c(H2C2O4)>c(C2O42-)
D.点④所示溶液中:c(K+)+ c(H2C2O4)+ c(HC2O4—) +c(C2O42-)=0.10mol·L-1
-
常温下,用0.10 mol·L-1 KOH溶液滴定 10.00 mL 0.10 mol·L-1 H2C2O4(二元弱酸)溶液所得滴定曲线如图(混合溶液的体积可看成混合前溶液的体积之和)。下列说法正确的是
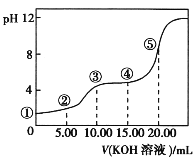
A.点①所示溶液中: =1012
=1012
B.点②所示溶液中:c(K+)+c(H+)=c(HC2O4-)+c(C2O42-)+c(OH-)
C.点③所示溶液中:c(K+)>c(HC2O4-)>c(C2O42-)>c(H+)>c(OH-)
D.点④所示溶液中:c(K+)+c(H2C2O4)+c(HC2O4-)+c(C2O42-)=0.10 mol·L-1
-
25℃时,用0.10mol•L-1的氨水滴定10.00mL0.05mol•L-1的二元酸H2A的溶液,滴定过程中加入氨水的体积(V)与溶液中 的关系如图所示。下列说法正确的是( )
的关系如图所示。下列说法正确的是( )
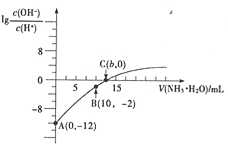
A.H2A的电离方程式为H2A⇌H++HA-
B.B点溶液中,水电离出的氢离子浓度为1.0×10-6mol•L-1
C.C点溶液中,c(NH4+)+c(NH3•H2O)=2c(A2-)
D.25℃时,氨水的电离平衡常数为
-
25℃时,用0.10 mol/L的氨水滴定10.00 mL 0.05 mol/L的二元酸H2A的溶液,滴定过程中加入氨水的体积(V)与溶液中 的关系如图所示。下列说法正确的是
的关系如图所示。下列说法正确的是
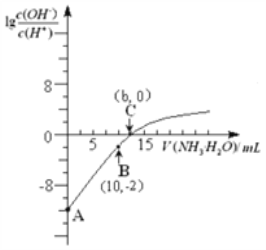
A. H2A的电离方程式为H2A H++HA -
H++HA -
B. B点溶液中,水电离出的氢离子浓度为1.0×10-6 mol/L
C. C点溶液中,c(NH4+)+c(NH3·H2O)= 2c(A2-)
D. 25℃时,该氨水的电离平衡常数为
-
25℃时,用0.10 mol/L的氨水滴定10.00mL0.05mol/L的二元酸H2A的溶液,滴定过程中加入氨水的体积(V)与溶液中 的关系如图所示。下列说法正确的是( )
的关系如图所示。下列说法正确的是( )

A. H2A的电离方程式为H2A H++HA -
H++HA -
B. B点溶液中,水电离出的氢离子浓度为1.0×10-6 mol/L
C. C点溶液中,c(NH4+)+c(NH3·H2O)= 2c(A2-)
D. 25℃时,该氨水的电离平衡常数为
-
室温下,用0.10mol/L的氢氧化钠溶液滴定10.00mL0.10mol/L醋酸溶液,水的电离度随氢氧化钠溶液体积的变化曲线如图所示,下列说法正确的是( )

A.该滴定过程应该选择甲基橙作为指示剂
B.N点溶液中c(OH-)=c(CH3COO-)+c(CH3COOH)+c(H+)
C.从P点到N点,溶液中水的电离程度逐渐增大
D.M点对应的NaOH溶液的体积为10.00mL









