-
硫化氢是天然气及石油中含硫杂质,近年来发现H2S可用于高效制取氢气。回答下列问题:
(1)H2S可用FeCl3溶液、NaClO溶液及氨水等吸收。
①FeCl3溶液吸收H2S气体,该反应的还原产物为_________。
②NaClO溶液吸收H2S,氧化剂与还原剂的物质的量之比为4:1,则该反应的离子方程式
为___________。
(2) Linkkous等学者通过多硫化物作循环液,设计出如下四步反应:
(Ⅰ)H2S+OH-=HS-+H2O (Ⅱ)2HS-+H2O H2↑+S22-
H2↑+S22-
(Ⅲ)H2S+S22-=2HS-+S↓ (Ⅳ)HS-+H2O=H2S+OH-
四步反应的总反应的化学方程式为__________________;能量转化方式为______。
(3)克劳斯法脱硫包含的反应为:
2H2S(g)+3O2(g)=2SO2(g)+2H2O(l) △H1
2H2S(g)+ SO2(g)=3S(s)+ 2H2O(l) △H2
H2S(g)+  O2(g)= S(s)+ 2H2O(l) △H3
O2(g)= S(s)+ 2H2O(l) △H3
①△H3=_________(用△H1、△H2表示)。
②为了达到较好的脱硫率,除采用多级脱硫外,还可采取的措施是___________________。
(4)硫化氢裂解制氢气的反应为2H2S(g)  S2 (g)+2H2 (g),设起始时容器中只有H2S,平衡时三种物质的组成与裂解温度关系如图所示。
S2 (g)+2H2 (g),设起始时容器中只有H2S,平衡时三种物质的组成与裂解温度关系如图所示。
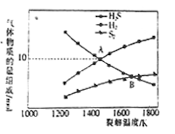
①A点时,H2S的转化率为_______________。
②B点时,设容器的总压为p Pa,则平衡常数Kp为________(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
-
硫化氢大量存在于天然气及液化石油气中,近年来发现 可用于制取氢气、合成硫醇等。回答下列问题:
可用于制取氢气、合成硫醇等。回答下列问题:
(1)D.Berk等学者设计的用FeS催化分解 包括下列反应:
包括下列反应:
Ⅰ.
Ⅱ.
Ⅲ.
① =____________(用
=____________(用 表示)。
表示)。
②已知单质硫气态时以 形式存在(结构为S=S)。键能E(H-S)=339
形式存在(结构为S=S)。键能E(H-S)=339 、E(H-H)=436
、E(H-H)=436 、E(S=S)=225
、E(S=S)=225 ,则
,则 =____________
=____________ 。
。
③ 是离子化合物,Fe显+2价,
是离子化合物,Fe显+2价, 的电子式为______________。
的电子式为______________。
(2)银器长期露置在含 的空气中表面会生成
的空气中表面会生成 而变黑,该反应的氧化剂为________;将表面变黑的银器放在盛有食盐水的铝制容器中煮沸,表面重新变为光亮,正极发生的电极反应为________。
而变黑,该反应的氧化剂为________;将表面变黑的银器放在盛有食盐水的铝制容器中煮沸,表面重新变为光亮,正极发生的电极反应为________。
(3)实验室用粗锌制取氢气时常含有少量的 ,可用酸性
,可用酸性 溶液(
溶液( 被还原为
被还原为 )将
)将 氧化为S而除去,该反应的离子方程式为_______。
氧化为S而除去,该反应的离子方程式为_______。
(4) 与
与 合成硫醇
合成硫醇 的反应
的反应 在不同温度及不同物质的量之比时
在不同温度及不同物质的量之比时 的平衡转化率如图所示:
的平衡转化率如图所示:
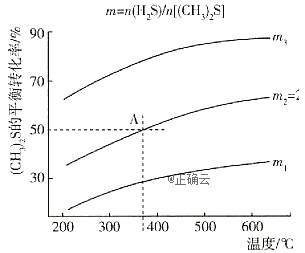
①该反应的 ______0(填“>”或“<");
______0(填“>”或“<"); _________
_________ (填“>”或“<”)。
(填“>”或“<”)。
②在2L密闭容器中充入0.2mol 和0.1mol
和0.1mol ,在A点达到平衡时,A点对应温度下反应的平衡常数为K=_________。
,在A点达到平衡时,A点对应温度下反应的平衡常数为K=_________。
③为提高 的平衡转化率,除改变温度及投料比(m)外,还可采取的措施是_____
的平衡转化率,除改变温度及投料比(m)外,还可采取的措施是_____
-
煤气中主要的含硫杂质有H2S以及COS(有机硫),煤气燃烧后含硫杂质会转化成SO2从而引起大气污染。煤气中H2S的脱除程度已成为其洁净度的一个重要指标。回答下列问题:
(1)将H2S通入FeCl3溶液中,该反应的还原产物为___________。
(2)脱除煤气中COS的方法有Br2的KOH溶液氧化法、H2还原法以及水解法等。
①COS的分子结构与CO2相似,COS的电子式为_____________。
②Br2的KOH溶液将COS氧化为硫酸盐和碳酸盐的离子方程式为_____________。
③已知断裂1mol化学键所需的能量如下:
| 化学键 | H—H | C═O | C═S | H—S | C≡O |
| E/kJ•mol-1 | 436 | 745 | 577 | 339 | 1072 |
H2还原COS发生的反应为H2(g)+COS(g) ═H2S(g)+CO(g),该反应的ΔH=________kJ·mol-1。
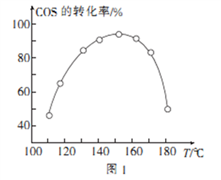
④用活性α—Al2O3催化COS水解的反应为COS(g)+ H2 O(g)  CO2(g)+ H2S (g) ΔH<0,相同投料比、相同流量且在催化剂表面停留相同时间时,不同温度下COS的转化率(未达到平衡)如图1所示;某温度下,COS的平衡转化率与
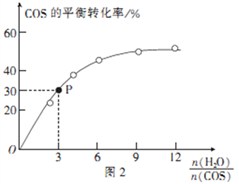
CO2(g)+ H2S (g) ΔH<0,相同投料比、相同流量且在催化剂表面停留相同时间时,不同温度下COS的转化率(未达到平衡)如图1所示;某温度下,COS的平衡转化率与 的关系如图2所示。
的关系如图2所示。
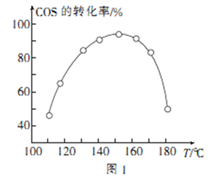
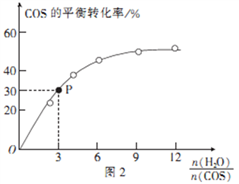
由图1可知,催化剂活性最大时对应的温度约为____________;由图2可知,P点时平衡常数K=_____
(保留2位有效数字)。
(3)常温下可发生反应:ZnS(s)+2H+(aq)  Zn2+(aq)+H2S(aq),达到平衡时,该反应的平衡常数K=_______[已知:Ksp(ZnS)=2.93×10-25;H2S电离常数;Ka1=9.5×10-8,Ka2=1.3×10-14]。
Zn2+(aq)+H2S(aq),达到平衡时,该反应的平衡常数K=_______[已知:Ksp(ZnS)=2.93×10-25;H2S电离常数;Ka1=9.5×10-8,Ka2=1.3×10-14]。
-
煤气中主要的含硫杂质有H2S以及COS(有机硫),煤气燃烧后含硫杂质会转化成SO2从而引起大气污染。煤气中H2S的脱除程度已成为其洁净度的一个重要指标。回答下列问题:
(1)将H2S通入FeCl3溶液中,该反应的还原产物为___________。
(2)脱除煤气中COS的方法有Br2的KOH溶液氧化法、H2还原法以及水解法等。
①COS的分子结构与CO2相似,COS的电子式为_____________。
②Br2的KOH溶液将COS氧化为硫酸盐和碳酸盐的离子方程式为_____________。
③已知断裂1mol化学键所需的能量如下:
| 化学键 | H—H | C═O | C═S | H—S | C≡O |
| E/kJ•mol-1 | 436 | 745 | 577 | 339 | 1072 |
H2还原COS发生的反应为H2(g)+COS(g) ═H2S(g)+CO(g),该反应的ΔH=________kJ·mol-1。
④用活性α—Al2O3催化COS水解的反应为COS(g)+ H2 O(g)  CO2(g)+ H2S (g) ΔH<0,相同投料比、相同流量且在催化剂表面停留相同时间时,不同温度下COS的转化率(未达到平衡)如图1所示;某温度下,COS的平衡转化率与
CO2(g)+ H2S (g) ΔH<0,相同投料比、相同流量且在催化剂表面停留相同时间时,不同温度下COS的转化率(未达到平衡)如图1所示;某温度下,COS的平衡转化率与 的关系如图2所示。
的关系如图2所示。
由图1可知,催化剂活性最大时对应的温度约为____________;由图2可知,P点时平衡常数K=_____
(保留2位有效数字)。
(3)常温下可发生反应:ZnS(s)+2H+(aq)  Zn2+(aq)+H2S(aq),达到平衡时,该反应的平衡常数K=_______[已知:Ksp(ZnS)=2.93×10-25;H2S电离常数;Ka1=9.5×10-8,Ka2=1.3×10-14]。
Zn2+(aq)+H2S(aq),达到平衡时,该反应的平衡常数K=_______[已知:Ksp(ZnS)=2.93×10-25;H2S电离常数;Ka1=9.5×10-8,Ka2=1.3×10-14]。
-
(15分)开发氢能是实现社会可持续发展的需要。下图是以含H2S杂质的天然气为原料制取氢气的流程图。
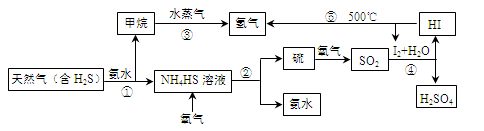
回答下列问题:
(1)反应②的化学方程式为 。
(2)反应④的离子方程式为 。
(3)步骤③中制氢气的原理如下:
Ⅰ:CH4(g)+H2O(g) CO(g)+3H2(g) ΔH=+206.4 kJ·mol-1
CO(g)+3H2(g) ΔH=+206.4 kJ·mol-1
Ⅱ:CO(g)+H2O(g)  CO2(g)+H2(g) ΔH=-41.2 kJ·mol-1
CO2(g)+H2(g) ΔH=-41.2 kJ·mol-1
①对于反应Ⅰ,一定可以提高平衡体系中H2的百分含量,又能加快反应速率的措施是 (填字母代号)。
a.升高温度 b.增大水蒸气浓度 c.加入催化剂 d.降低压强
②利用反应Ⅱ,将CO进一步转化,可提高H2的产量。若1.00 mol CO和H2的混合气体(CO的体积分数为20%)与H2O反应,得到1.18 mol CO、CO2和H2的混合气体,则CO的转化率为 。
③若该天然气中硫化氢的体积分数为5%,且甲烷与水蒸气反应转化成二氧化碳和氢气的总转化率为80%,则通过上述流程1.00 m3 天然气理论上可制得氢气 m3(同温同压条件下)。
(4)一定条件下,如图所示装置可实现有机物的电化学储氢(生成的有机物为气体,忽略其他有机物)。
①生成目标产物的电极反应式为 。
②该储氢装置的电流效率为η= 。(η=  ×100%,计算结果保留小数点后1位)
×100%,计算结果保留小数点后1位)

-
利用天然气及化工废气中的硫化氢,不仅可制取氢气并回收单质硫,还可减少对环境的污染。
回答下列问题:
(1)在一定的条件下,天然气脱硫工艺中会发生以下反应:
2H2S(g)+3O2(g)=2SO2(g)+2H2O(g) ΔH1
4H2S(g)+SO2(g)=3S2(g)+4H2O(g) ΔH2
2H2S(g)+O2(g)=2S(g)+2H2O(g) ΔH3
则相同条件下反应2S(g)=S2(g)的△H=_______(用含△H1、△H2和△H3的代数式表示)。
(2)硫化氢分解反应2H2S(g) 2H2(g)+S2(g),在101 kPa时各气体的体积分数与温度的关系如下图所示:
2H2(g)+S2(g),在101 kPa时各气体的体积分数与温度的关系如下图所示:
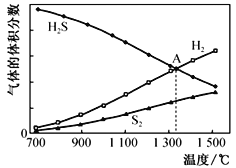
①该反应的△H______0(填“>”、“<”)。
②为提高H2S的平衡分解率,除改变温度外,还可采取的措施是______________________________。
③图中A点时反应的平衡常数Kp=______(用平衡分压代替浓度,平衡分压=总压×物质的量分数)。
(3)我国学者发明的一种分解硫化氢制氢并回收硫的装置如下图所示:
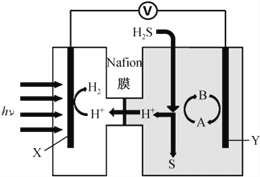
①该装置中能量转化的方式为____________________________________________________。
②若Y极液中的电对(A/B)选用I3-/I-,装置工作时Y极上的电极反应式为__________________________,Y极溶液中发生的离子反应为________________________________;再列举一种可作为Y极循环液常见的电对:_______________。
③该分解H2S制氢的方法主要优点是_____________________________________________________。
-
含硫化氢的工业废气要经过治理方能排放,既回收硫单质又防止大气污染.请根据如下治理方法回答相关问题.
(1)电解法治理硫化氢的工艺流程如下:
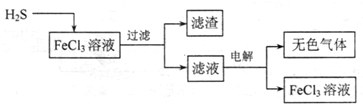
①FeCl3溶液吸收H2S的生成物是______
②用惰性电极电解滤液时,阴极的电极反应式为______,电解总反应的离子方程式是______ 2Fe3++H 2↑
-
热化学碘硫循环可用于大规模制氢气,SO2水溶液还原I2和HI分解均是其中的主要反应。回答下列问题:
(1)以太阳能为热源,热化学硫碘循环分解水是一种高效、无污染的制氢方法。其反应过程如图所示。
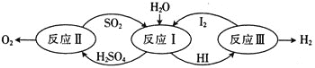
反应II包含两步反应:
①H2SO4(l)=SO3(g)+H2O(g) △H1=+177kJ/mol
②2SO3(g)=2SO2(g)+O2(g) △H2=+196kJ/mol
①写出反应①自发进行的条件是:________。
②写出反应Ⅱ的热化学方程式:________。
(2)起始时 HI的物质的量为1mo1,总压强为0.1MPa下,发生反应HI(g)
 H2(g)+
H2(g)+ I2(g) 平衡时各物质的物质的量随温度变化如图所示:
I2(g) 平衡时各物质的物质的量随温度变化如图所示:
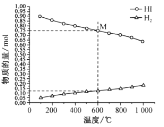
①该反应的△H ________ (“>”或“<”)0。
②600℃时,平衡分压p(I2)= ___MPa,反应的平衡常数Kp=______ (Kp为以分压表示的平衡常数)。
(3)反应 H2(g)+I2(g)  2HI(g)的反应机理如下:
2HI(g)的反应机理如下:
第一步:I2 2I(快速平衡)
2I(快速平衡)
第二步:I+H2 H2I(快速平衡)
H2I(快速平衡)
第三步:H2I+I  2HI (慢反应)
2HI (慢反应)
①第一步反应_____ (填 “放出”或“吸收”)能量。
②只需一步完成的反应称为基元反应,基元反应如aA+dD = gG+hH 的速率方程,v= kca(A)•cd(D),k为常数;非基元反应由多个基元反应组成,非基元反应的速率方程可由反应机理推定。H2(g)与I2(g)反应生成 HI(g)的速率方程为v= ____(用含k1、k-1、k2…的代数式表示)。
-
 是一种高效氧化剂,可用来氧化吸附有机异味物,也可以与水中的杂质如二价铁、锰、硫、氰、酚等反应.实验室常用
是一种高效氧化剂,可用来氧化吸附有机异味物,也可以与水中的杂质如二价铁、锰、硫、氰、酚等反应.实验室常用 标准溶液标定未知浓度的
标准溶液标定未知浓度的 溶液,发生反应
溶液,发生反应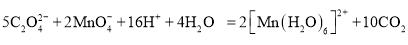 ↑.
↑.
根据以上信息,完成下列问题:
(1)按电子排布K位于元素周期表的________区,基态 的核外电子排布式可表示为________.
的核外电子排布式可表示为________.
(2) 中所含有的共价键数目为________.
中所含有的共价键数目为________.
(3)基态C原子的核外电子中占据最高能级的电子云轮廓图为________, 中碳原子的轨道杂化类型是________.
中碳原子的轨道杂化类型是________.
(4)同主族元素氧、硫、硒对应最简单氢化物的沸点: ,原因是________.
,原因是________.
(5) 的结构中Se为面心立方最密堆积,晶胞结构如图所示.
的结构中Se为面心立方最密堆积,晶胞结构如图所示.
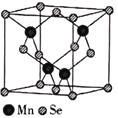
 中Mn的配位数为________.
中Mn的配位数为________.
 若该晶体的晶胞参数为apm,阿伏加德罗常数的值为
若该晶体的晶胞参数为apm,阿伏加德罗常数的值为 则距离最近的两个锰原子之间的距离为________pm,
则距离最近的两个锰原子之间的距离为________pm, 的密度
的密度 ________
________ 列出表达式
列出表达式 。
。
-
H2S作为一种有毒气体,广泛存在于石油、化工、冶金、天然气等行业的废气中,脱除气体中的硫化氢对于保护环境、合理利用资源都有着现实而重要的意义。
请回答下列问题:
(1)H2S的电子式为____________,其热稳定性弱于HCl的原因是____________。
(2)用H2S和天然气生产CS2的反应为CH4(g)+2H2S(g)  CS2(l)+4H2(g)。
CS2(l)+4H2(g)。
已知:I.CH4(g)+4S(s)  CS2(g)+2H2S(g) △H1=akJ·mol-1;
CS2(g)+2H2S(g) △H1=akJ·mol-1;
II.S(s)+H2(g)  H2S(g) △H2=bkJ·mol-1;
H2S(g) △H2=bkJ·mol-1;
Ⅲ.CS2(1)  CS2(g) △H3=ckJ·mol-1;
CS2(g) △H3=ckJ·mol-1;
则反应CH4(g)+2H2S(g)  CS2(1)+4H2(g)的△H=____________ kJ·mol-1(用含a、b、c的代数式表示)。
CS2(1)+4H2(g)的△H=____________ kJ·mol-1(用含a、b、c的代数式表示)。
(3)800℃时,将一定量的H2S气体充入恒容密闭容器中,发生反应H2S(g)  S(s)+H2(g),tmin后反应达到化学平衡状态,测得容器中H2与H2S的质量浓度分别为0.02g/L、0.34g/L,则H2S的初始浓度_______mol/L,该温度下,反应的化学平衡常数K=______。
S(s)+H2(g),tmin后反应达到化学平衡状态,测得容器中H2与H2S的质量浓度分别为0.02g/L、0.34g/L,则H2S的初始浓度_______mol/L,该温度下,反应的化学平衡常数K=______。
(4)向恒压密闭容器中充入0.1 molCH4和0.2molH2S,发生反应CH4(g)+2H2S(g)  CS2(g)+4H2(g),测得不同温度下,CH4的平衡转化率(%)与温度(℃)的关系如图所示:
CS2(g)+4H2(g),测得不同温度下,CH4的平衡转化率(%)与温度(℃)的关系如图所示:
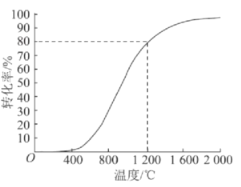
①该反应的活化能:E正____________E逆(填“>”“<”或“=”)
②若初始容积为V0L,1200℃反应达到平衡时,容器的容积为____________L(用含V0的代数式表示)。
③1200℃时,欲提高CH4的平衡转化率,可以采取的措施是____________(填选项字母)。
A.增大压强 B.再充入CH4
C.再充入H2S D.充入He E.使用高效催化剂
(5)H2S废气可用碳酸钠溶液吸收,将吸收足量H2S气体后的溶液加入到如图所示的电解池中进行电解,在阳极生成有工业价值的Na2S2O3,电解时阳极的电极反应式为____________。

H2↑+S22-
O2(g)= S(s)+ 2H2O(l) △H3
S2 (g)+2H2 (g),设起始时容器中只有H2S,平衡时三种物质的组成与裂解温度关系如图所示。













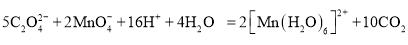 ↑.
↑.

