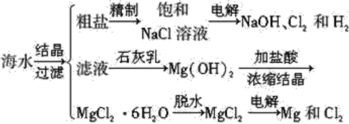-
海水是应用前景广阔的化工原料资源,从海水中可提取各种化工原料.如图是工业上对海水的几项综合利用的示意图:
回答下列问题:
(1)①粗盐中含有Ca2+、Mg2+、SO42-等杂质,精制时所用试剂为:A:盐酸;B:BaCl2溶液;C:NaOH溶液;D:Na2CO3溶液.加入试剂的顺序是________.
②电解饱和食盐水时,与电源正极相连的电极上发生的反应为________,与电源负极线连的电极附近溶液pH________(变大、不变、变小).
(2)工业上从海水中提取的NaCl,可用来制取纯碱,其简要过程如下:向饱和食盐水中先通入气体A,后通入气体B,充分反应后过滤得到晶体C和滤液D,将晶体C灼烧即可制得纯碱.
①气体A、B是CO2或NH3,则气体A应是________(填化学式).C的制得发生反应的化学方程式为________.
②滤液D中主要含有NH4Cl、NaHCO3等物质,工业上是向滤液D中通入NH3,并加入细小食盐颗粒,冷却析出不含有NaHCO3的副产品
NH4Cl晶体,则通入NH3的作用是________.
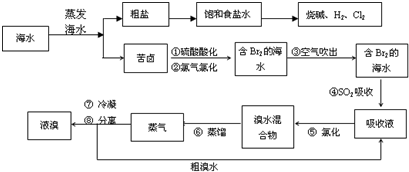
(3)空气吹出法工艺,是目前“海水提溴”的最主要方法之一.
a、写出步骤①④反应的离子方程式:①________;④________.
b、在步骤⑥的蒸馏过程中,温度应控制在80-90℃、温度过高过低都不利于生产,请解释原因:________.
c、在步骤①、②之后并未直接用“含溴的海水”进行蒸馏得到液溴,而是经过“空气吹出”、“SO2吸收”、“氯化”后再蒸馏,这样操作的意义是________.
-
海水是应用前景广阔的化工原料资源,从海水中可提取各种化工原料.如图1是工业 上对海水的几项综合利用的示意图(已知气体X为电解饱和食盐水所得;母液苦卤中主要 含有Ca2+、Mg2+,Cl-,SO42‑、Br-等离子)请回答:
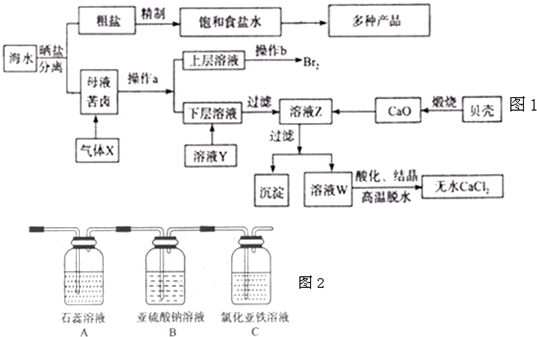
(1)在粗盐中含有Ca2+、Mg2+、SO42-等杂质,梢制时所用的试剂为:A.盐酸B.氯化钡溶 液C.氢氧化钠溶液D.碳酸钠溶液,则加入试剂的顺序是(填编号)______.
(2)气体X的化学式为______,操作a所用的主要仪器是______.
(3)加入溶液Y的目的是______,用CaO调节溶液Z的pH,可以除去Mg2+得到溶液W.由表中数据可知,理论上可选择pH最大范围是______.酸化溶液W时,使用的试剂为______.
| 开始沉淀时的pH | 沉淀完全时的pH |
| Mg2+ | 9.6 | 11.0 |
| Ca2+ | 12.2 | c(OH-)=1.8mol•L-1 |
(4)将气体X依次通过如图2所示装置以验证气体X的性质:
①通入气体X后,A中出现的现象是______.
②C装置中发生反应的离子方程式为______.
③请你帮该小组同学设计一个实验,证明洗气瓶B中的Na2SO3已被氧化(简述实验步骤)______.
-
海水是应用前景广阔的化工原料资源,从海水中可提取各种化工原料.如图是工业上对海水的几项综合利用的示意图(已知气体X为电解饱和食盐水所得;母液苦卤中主要含有Ca2+、Mg2+,Cl-,SO42-、Br-等离子)请回答:

(1)在粗盐中含有Ca2+、Mg2+、SO42-等杂质,梢制时所用的试剂为:A.盐酸B.氯化钡溶液C.氢氧化钠溶液D.碳酸钠溶液,则加入试剂的顺序是(填编号)______
(2)气体X的化学式为______,操作a所用的主要仪器是______。
(3)加入溶液Y的目的是______,用CaO调节溶液Z的pH,可以除去Mg2+得到溶液W。由表中数据可知,理论上可选择pH最大范围是______。酸化溶液W时,使用的试剂为______

(4)将气体X依次通过下列装置以验证气体X的性质:

①通入气体X后,A中出现的现象是____________
②C装置中发生反应的离子方程式为____________。
③请你帮该小组同学设计一个实验,证明洗气瓶B中的Na2SO3已被氧化(简述实验步骤)
________________________________________________________________________
-
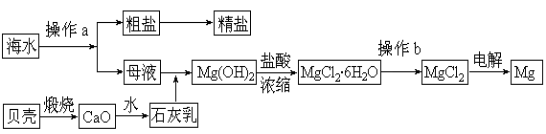
海水是一种丰富的资源,工业上从海水中可提取许多种物质,广泛应用于生活、生产、科技等方面。下图是某工厂对海水资源进行综合利用的示意图。
回答下列问题:
(1)流程图中操作a的名称为 。
(2)工业上从海水中提取的NaCl,可用来制取纯碱,其简要过程如下:向饱和食盐水中先通入气体A,后通入气体B,充分反应后过滤得到晶体C和滤液D,将晶体C灼烧即可制得纯碱。
①已知气体A、B是CO2或NH3,则气体A应是 (填化学式)。
②灼烧晶体C的反应方程式为 。
③滤液D中主要含有NH4Cl、NaHCO3等物质,工业上是向滤液D中通入NH3,并加入细小食盐颗粒,冷却后,可析出不含有NaHCO3的副产品NH4Cl晶体,则通入NH3的作用是 。
(3)镁是一种用途很广的金属材料,目前世界上60%的镁从海水中提取。
① 若要验证所得无水MgCl2中不含NaCl,最简单的操作方法是: 。
② 通过操作b获得无水MgCl2是在 氛围中进行,若直接在空气中加热,则会生成Mg(OH)Cl,写出有关反应的化学方程式: 。
-
海水是一种丰富的资源,工业上从海水中可提取NaCl、Na2CO3、Mg等多种物质,这些物质广泛应用于生产、生活等领域.如图所示是某工厂对海水资源进行综合利用的流程.
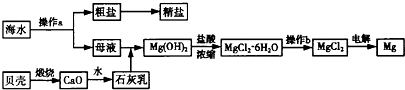
请回答下列问题:
(1)流程图中操作a的名称为______.
(2)工业上从海水中提取的NaCl,可用来制取纯碱,其简要过程如下:向饱和食盐水中先通入气体A,后通入气体B,充分反应过滤得到晶体C和滤液D,将晶体C灼烧即可制得纯碱.
①气体A应是______(填化学式),此过程的化学方程式为______.
②滤液D中主要含有NH4Cl、NaHCO3等物质,工业上常向滤液D中通入NH3,并加入细小食盐颗粒,使溶液冷却,析出不含有NaHCO3副产品的NH4Cl晶体,通入NH3的作用是______.
(3)操作b应在______气流中进行,若在空气中加热,则会水解生成Mg(OH)Cl,写出有关反应的化学方程式:______ Mg(OH)Cl+HCl↑+5H2O
-
(8分)【化学-化学与技术】
海洋是化学资源宝库,海洋资源的综合利用具有广阔的前景。回答下列问题:
(1)蒸馏法是人类最早使用的淡化海水的方法,技术和工艺比较完备,但常规蒸馏法法也存在较大缺陷,请说明常规蒸馏法淡化海水的最大缺陷。
__________________________________________________________
(2)离子交换法也是常用的水处理技术。聚丙烯酸钠是一种离子交换树脂,写出聚丙烯酸钠单体的结构简式________。
(3)目前从海水中提取溴的常用流程如下(苦卤,海水蒸发结晶分离出食盐的母液):
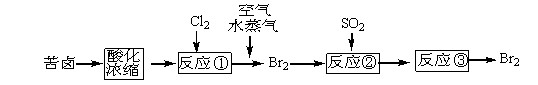
从反应③后的溶液中分离出单质溴的方法是________。
(4)海水提镁过程中,与石灰窑和盐酸厂有着紧密的联系,试说明海水提镁与盐酸厂之间的必然联系。__________________________________________________________
-
海水中可提取多种化工原料,下面是工业上对海水的几项综合利用示意图。

根据示意图回答下列问题:
(1)粗盐中含有Ca2+、Mg2+、SO42-等杂质离子,精制时所用试剂为盐 酸、BaCl2溶液、NaOH溶液、Na2CO3溶液,加入试剂的顺序是、 、、。
(2)电解饱和食盐水的总反应的化学方程式为。
(3)工业上MgCl2·6H2O晶体在________气氛中加热脱水,通入此种气体的作用是。
-
海洋是个巨大的资源宝库,海水资源的利用具有非常广阔的发展前景。海水中溴元素以Br-形式存在,工业上用空气吹出法从海水中提取溴的工艺流程如下所示:
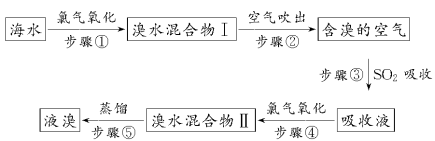
(1)步骤①反应的廊子方程式为_______________________________。
(2)步骤③反应的化学方程式为_________________________________。
(3)Br的原子序数是________,在周期表中位于第________周期、________族。
(4)步骤⑤蒸馏的过程中,温度应控制在80~90℃。温度过高或过低都不利于生产,请解释原因:________________。
(5)为什么不直接用“溴水混合物Ⅰ”而要用“溴水混合物Ⅱ”进行蒸馏,得出液溴?
-
从海水中可提取多种化工原料,下面是工业上对海水成分综合利用的示意图。
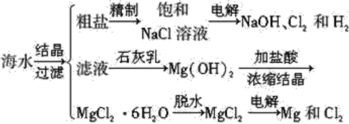
试回答下列问题:
(1)写出用海滩上的贝壳制Ca(OH)2的化学方程式_________________________。
(2)写出电解饱和NaCl溶液的化学方程式___________________________________。
(3)将电解生成的氯气通入石灰乳中可制得漂白粉,写出其反应的化学方程式_______________________。
(4)用海滩上的贝壳制Ca(OH)2而不从异地山中开凿石灰石制取,主要考虑到什么问题?_________________________________。
-
海水中有非常丰富的化学资源,从海水中可提取多种化工原料。某工厂对海水资源综合开发利用的部分工艺流程图如下。回答下列问题:

(1)精制食盐水时下列物质中,用到的有______________________(填序号)。
①NaOH溶液 ②盐酸 ③K2CO3溶液 ④BaCl2溶液 ⑤硫酸 ⑥Na2CO3溶液 ⑦Ba(NO3)2溶液
(2)工业上经过②、③、④制备Ba2。步骤②中Cl2氧化Br-应在________(填酸性或碱性)条件下进行;步骤③Br2可用热空气吹出,其原因是_____________________。
(3)为了除去工业Br2中微量的Cl2,可向工业Br2中____________________。
a.通入HBr b.加入Na2CO3溶液 c.加入NaBr溶液 d.加入Na2SO3溶液
(4)若步骤⑤所得Mg(OH)2沉淀中混有Ca(OH)2杂质,写出除去杂质的实验步骤 ________________(写出加入的试剂和操作)。