-
某固体甲 [成分为M3Z2 (OH) a(CO3) b]可用作塑料阻燃剂,该盐分解产生大量的CO2可以作为原料制备有机产品。取甲46g高温灼烧至恒重,得到11.2L CO2(标准状况)和22.2g仅含两种金属氧化物的固体乙,其中Z的氧化物既溶于强酸又溶于强碱,向乙中加入足量的稀硫酸所得产物中含有MSO4。请回答:
(1)甲灼烧至恒重的化学方程式 (M、Z用元素符号表示)。
(2)甲能用作塑料阻燃剂的原因 。
(3)工业上利用CO2和H2在一定条件下反应合成甲醇。已知下列反应:
①CO2(g)+ 3H2(g) CH3OH (g)+ H2O(g) ΔH1
CH3OH (g)+ H2O(g) ΔH1
② 2H2 (g)+ O2(g) = 2H2O (l) ΔH2
③ H2O(g) = H2O(l) ΔH3
写出气态甲醇完全燃烧生成CO2(g)和气态水的热化学方程式: (用ΔH1、ΔH2、ΔH3表示ΔH)。
(4)反应CO2(g)+ 3H2(g) CH3OH (g)+ H2O(g),它的有关数据如下图所示。
CH3OH (g)+ H2O(g),它的有关数据如下图所示。
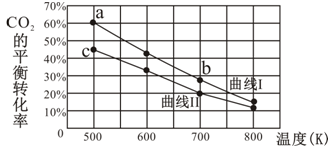
反应物起始的物质的量之比
下列说法正确的是 。
A.曲线Ⅰ对应的反应物起始物质的量之比为1.5
B.单位时间内消耗H2的物质的量与消耗H2O的物质的量之比为3∶1时,反应达到平衡状态
C.a点对应的H2的平衡转化率为90 %
D.b点对应的平衡常数K值大于c点
(5)反应CO2(g)+ 3H2(g) CH3OH (g)+ H2O(g) 在体积为2L的固定绝热的密闭容器中加入1 molCH3OH和1 molH2O ,第4 min达到平衡,反应中c(CO2)的变化情况如下图所示。在第5 min时向体系中再充入0.2molCO2和0.4molH2(其它条件不变),第8 min达到平衡,此时c(H2) =c(CH3OH)。请在下图中画出5到9 min的c(CO2)浓度示意曲线。
CH3OH (g)+ H2O(g) 在体积为2L的固定绝热的密闭容器中加入1 molCH3OH和1 molH2O ,第4 min达到平衡,反应中c(CO2)的变化情况如下图所示。在第5 min时向体系中再充入0.2molCO2和0.4molH2(其它条件不变),第8 min达到平衡,此时c(H2) =c(CH3OH)。请在下图中画出5到9 min的c(CO2)浓度示意曲线。
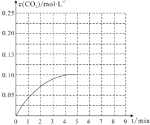
-
(12分)碱式碳酸铝镁[MgaAlb(OH)c(CO3)d·x H2O]常用作塑料阻燃剂。
(1)碱式碳酸铝镁具有阻燃作用,是由于其受热分解需吸收大量热量和 。
(2)MgaAlb(OH)c(CO3)d·x H2O中a、b、c、d的代数关系式为 。
(3)为确定碱式碳酸铝镁的组成,进行如下实验:
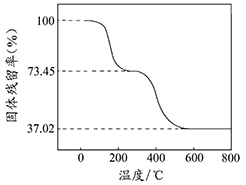
①准确称取3.390g样品与足量稀盐酸充分反应,生成CO20.560L(已换算成标准状况下)。②另取一定量样品在空气中加热,样品的固体残留率(固体样品的剩余质量/固体样品的起始质量×100%)随温度的变化如右图所示(样品在2700C时已完全失去结晶水,6000C以上残留固体为金属氧化物的混合物)。
根据以上实验数据计算碱式碳酸铝镁样品中的n(OH-): n(CO32-)(写出计算过程)。
-
碱式碳酸铝镁[MgaAlb(OH)c(CO3)d·x H2O]常用作塑料阻燃剂。
(1)碱式碳酸铝镁具有阻燃作用,是由于其受热分解需吸收大量热量和_________。
(2)MgaAlb(OH)c(CO3)d·x H2O中a、b、c、d的代数关系式为_________________。
(3)为确定碱式碳酸铝镁的组成,进行如下实验:
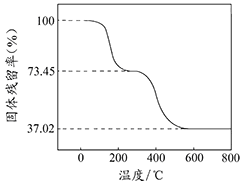
①准确称取3.390g样品与足量稀盐酸充分反应,生成CO20.560L(已换算成标准状况下)。②另取一定量样品在空气中加热,样品的固体残留率(固体样品的剩余质量/固体样品的起始质量×100%)随温度的变化如右图所示(样品在2700C时已完全失去结晶水,6000C以上残留固体为金属氧化物的混合物)。
根据以上实验数据计算碱式碳酸铝镁样品中的n(OH-): n(CO32-)(写出计算过程)________。
-
碱式碳酸铝镁[MgaAlb(OH)c(CO3)d·x H2O]常用作塑料阻燃剂。
(1)碱式碳酸铝镁具有阻燃作用,是由于其受热分解需吸收大量热量和 。
(2)MgaAlb(OH)c(CO3)d·x H2O中a、b、c、d的代数关系式为 。
(3)为确定碱式碳酸铝镁的组成,进行如下实验:
①准确称取3.390g样品与足量稀盐酸充分反应,生成CO20.560L(已换算成标准状况下)。②另取一定量样品在空气中加热,样品的固体残留率(固体样品的剩余质量/固体样品的起始质量×100%)随温度的变化如右图所示(样品在2700C时已完全失去结晶水,6000C以上残留固体为金属氧化物的混合物)。
根据以上实验数据计算碱式碳酸铝镁样品中的n(OH-): n(CO32-)(写出计算过程)。
-
碱式碳酸铝镁[MgaAlb(OH)c(CO3)d·xH2O]常用作塑料阻燃剂。
(1)碱式碳酸铝镁具有阻燃作用,是由于其受热分解需吸收大量热量和________。
(2)MgaAlb(OH)c(CO3)d·xH2O中a、b、c、d的代数关系式为________。
(3)为确定碱式碳酸铝镁的组成,进行如下实验:
①准确称取3.390 g样品与足量稀盐酸充分反应,生成CO2 0.560 L(已换算成标准状况下)。
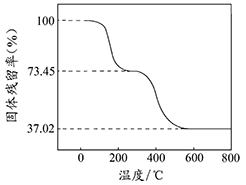
②另取一定量样品在空气中加热,样品的固体残留率(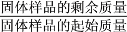 ×100%)随温度的变化如下图所示(样品在270 ℃时已完全失去结晶水,600 ℃以上残留固体为金属氧化物的混合物)。
×100%)随温度的变化如下图所示(样品在270 ℃时已完全失去结晶水,600 ℃以上残留固体为金属氧化物的混合物)。
根据以上实验数据计算碱式碳酸铝镁样品中的n(OH- )∶n(CO32- ) _________________ (写出计算过程)。
-
碱式碳酸铝镁[MgaAlb(OH)c(CO3)d·xH2O]常用作塑料阻燃剂。
(1)碱式碳酸铝镁具有阻燃作用,是由于其受热分解需吸收大量热量和________。
(2)MgaAlb(OH)c(CO3)d·xH2O中a、b、c、d的代数关系式为________。
(3)为确定碱式碳酸铝镁的组成,进行如下实验:
①准确称取3.390 g样品与足量稀盐酸充分反应,生成CO2 0.560 L(已换算成标准状况下)。
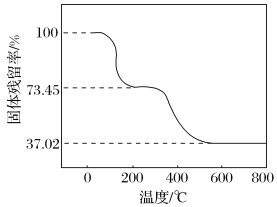
②另取一定量样品在空气中加热,样品的固体残留率(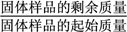 ×100%)随温度的变化如下图所示(样品在270 ℃时已完全失去结晶水,600 ℃以上残留固体为金属氧化物的混合物)。
×100%)随温度的变化如下图所示(样品在270 ℃时已完全失去结晶水,600 ℃以上残留固体为金属氧化物的混合物)。
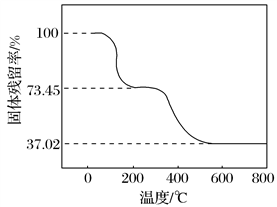
根据以上实验数据计算碱式碳酸铝镁样品中的n(OH- )∶n(CO )(写出计算过程)。_______
)(写出计算过程)。_______
-
Mg(OH)2可用作塑料的阻燃剂。现以某矿石(主要成分为3MgO·2SiO2·2H2O,还有少量Fe2O3、FeO、CaO和Al2O3)为原料生产,其工艺流程如下:
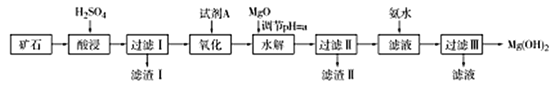
已知:
表1生成氢氧化物沉淀的pH
| 物质 | Fe(OH)2 | Fe(OH)3 | Al(OH)3 | Mg(OH)2 |
| 开始沉淀的pH | 7.6 | 1.9 | 3.4 | 9.1 |
| 完全沉淀的pH | 9.6 | 3.2 | 4.7 | 11.1 |
表2原料价格表
| 物质 | 价格(元•吨-1) |
| 漂液(含25.2% NaClO) | 450 |
| 双氧水(含30%H2O2) | 2400 |
回答下列问题:
(1)酸浸时,为提高矿石的浸出率可采取的措施为_________(任写一条)。该过程H2SO4适当过量的目的是_______________、_________________。
(2)工业生产要求生产成本较低,产品尽量不含杂质。试剂A的最佳选择是______,写出其发生反应的离子方程式_______________________。
(3)水解过程需调节溶液pH,a的取值范围为______,滤渣II的成分是______(填化学式)。
(4)向过滤II所得滤液中加入一定量氨水,写出镁离于沉淀的离子方程式____________,该过程温度不宜过高的原因是_____________________。
(5)实际生产中,可由Mg(OH)2为原料制备单质镁,简述制备方法_____________
-
氧化镁在易燃材料中常被用作阻燃剂,碳酸镁高温分解法是工业上制备轻质氧化镁的常用方法。镁硅矿主要成分为Mg3(Si2O5)(OH)4和还有少量的Fe2O3、Al2O3等。以镁硅矿为原料制备碳酸镁晶体(MgCO3•nH2O)的生产流程如下:
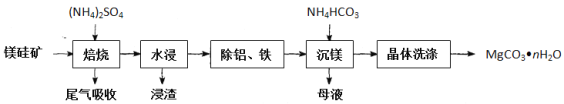
已知“焙烧”过程中的主要反应为:Mg3(Si2O5)(OH)4+5(NH4)2SO4 3MgSO4+10NH3↑+2SiO2+7H2O↑+2SO3↑
3MgSO4+10NH3↑+2SiO2+7H2O↑+2SO3↑
(1)Mg3(Si2O5)(OH)4用氧化物的形式表示为___,焙烧产物NH3的电子式为__。
(2)为提高水浸速率,可采取的措施为__(任写一种)。“浸渣”的主要成分为__。
(3)“除铝、铁”时,需将溶液pH调至8.0左右,适宜作调节剂的是__(填字母代号)。
a.Ca(OH)2 b.Mg(OH)2 c.NH3•H2O
(4)“沉镁”过程中反应的离子方程式为__。“沉镁”时若温度超过60℃,将会产生较多的碱式碳酸镁杂质,原因是___。
(5)流程中可以循环利用的物质是___(填化学式)。
(6)为测定产品MgCO3•nH2O中的n值,称取15.6g产品进行充分加热至恒重,冷却,称得固体质量为4g,则n=__。
-
硫酸亚铁是一种重要的化工原料,可以制备一系列物质。下列说法错误的是( )
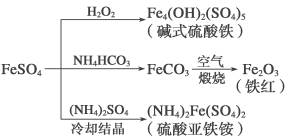
A.碱式硫酸铁水解能产生Fe(OH)3胶体,可用作净水剂
B.为防止NH4HCO3分解,生产FeCO3需在较低温度下进行
C.可用KSCN溶液检验(NH4)2Fe(SO4)2是否被氧化
D.常温下,(NH4)2Fe(SO4)2在水中的溶解度比FeSO4的大
-
硫酸亚铁是一种重要的化工原料,可以制备一系列物质(如下图),下列说法错误的是( )
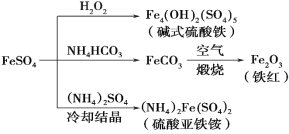
A. 碱式硫酸铁水解能产生Fe(OH)3胶体,可用做净水剂
B. 为防止NH4HCO3分解,生产FeCO3需在较低温度下进行,该反应的离子方程式为:Fe2++2HCO3-= FeCO3+ CO2↑+H2O
C. 可用KSCN溶液检验(NH4)2Fe(SO4)2是否被氧化
D. 该温度下,(NH4)2Fe(SO4)2在水中的溶解度比FeSO4的大
CH3OH (g)+ H2O(g) ΔH1
CH3OH (g)+ H2O(g),它的有关数据如下图所示。

CH3OH (g)+ H2O(g) 在体积为2L的固定绝热的密闭容器中加入1 molCH3OH和1 molH2O ,第4 min达到平衡,反应中c(CO2)的变化情况如下图所示。在第5 min时向体系中再充入0.2molCO2和0.4molH2(其它条件不变),第8 min达到平衡,此时c(H2) =c(CH3OH)。请在下图中画出5到9 min的c(CO2)浓度示意曲线。




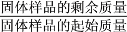 ×100%)随温度的变化如下图所示(样品在270 ℃时已完全失去结晶水,600 ℃以上残留固体为金属氧化物的混合物)。
×100%)随温度的变化如下图所示(样品在270 ℃时已完全失去结晶水,600 ℃以上残留固体为金属氧化物的混合物)。
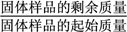 ×100%)随温度的变化如下图所示(样品在270 ℃时已完全失去结晶水,600 ℃以上残留固体为金属氧化物的混合物)。
×100%)随温度的变化如下图所示(样品在270 ℃时已完全失去结晶水,600 ℃以上残留固体为金属氧化物的混合物)。



