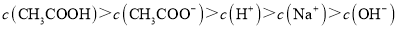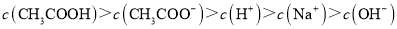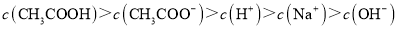-
常温下,用0.1000mol/LNaOH溶液分别滴定25.00mL0.1000mol/L盐酸溶液和
25.00mL0.1000mol/LCH3COOH溶液,滴定过程中pH变化曲线如下图所示。下列判断不正确的是
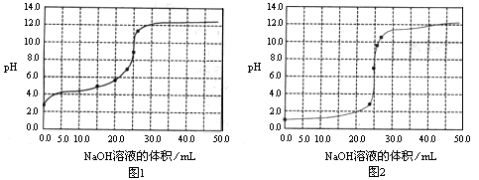
A.滴定盐酸的pH变化曲线为图2
B.在滴定CH3COOH溶液的过程中,始终都有c(Na+)+ c(H+)=c(CH3COO–)+c(OH–)
C.滴定CH3COOH溶液的过程中,当滴加12.5mLNaOH溶液时,溶液中离子浓度由大到小的顺序为c(CH3COO–)>c(Na+)>c(H+)>c(OH–)
D.当c(Na+)=c(CH3COO–)+ c(CH3COOH)时,溶液的pH<7
-
常温下,用0.1000mol/LNaOH溶液分别滴定20.00mL0.1000mol/LHCl溶液和20.00mL0.1000mol/LCH3COOH溶液,得到2条滴定曲线,如下图所示:
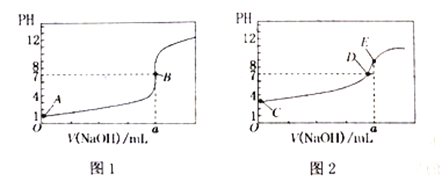
(1)由A、C点判断,滴定HCl溶液的曲线是__(填“图1”或“图2”)。
(2)a=___mL。
(3)c(Na+)=c(CH3COO-)的点是_______。
(4)E点对应离子浓度由大到小的顺序为________。
-
常温下,用0.1000mol/LNaOH溶液分别滴定20.00mL0.1000mol/LHCl溶液和20.00mL0.1000mol/LCH3COOH溶液,得到2条滴定曲线,如下图所示:
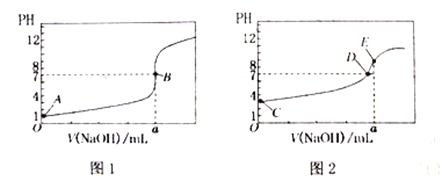
(1)由A、C点判断,滴定HCl溶液的曲线是__(填“图1”或“图2”)。
(2)a=___mL。
(3)c(Na+)=c(CH3COO-)的点是_______。
(4)E点对应离子浓度由大到小的顺序为________。
-
常温下,用 0.1000 mol·L NaOH溶液滴定 20.00mL0.1000 mol·L
NaOH溶液滴定 20.00mL0.1000 mol·L
 溶液所得滴定曲线如图。下列说法正确的是
溶液所得滴定曲线如图。下列说法正确的是
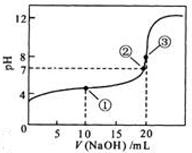
A.点①所示溶液中:
B.点②所示溶液中:
C.点③所示溶液中: 
D.滴定过程中可能出现:
-
常温下,用 0.1000 mol·L NaOH溶液滴定 20.00mL0.1000 mol·L
NaOH溶液滴定 20.00mL0.1000 mol·L
 溶液所得滴定曲线如图。下列说法正确的是
溶液所得滴定曲线如图。下列说法正确的是
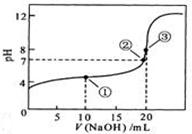
A.点①所示溶液中:
B.点②所示溶液中: 
C.点③所示溶液中:

D.滴定过程中可能出现:

-
常温下,用 0.1000 mol·L NaOH溶液滴定 20.00mL0.1000 mol·L
NaOH溶液滴定 20.00mL0.1000 mol·L
 溶液所得滴定曲线如图。下列说法正确的是
溶液所得滴定曲线如图。下列说法正确的是
A.点①所示溶液中:
B.点②所示溶液中:
C.点③所示溶液中:
D.滴定过程中可能出现:
-
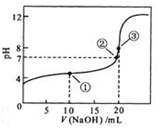
常温下,用 0.1000 mol·L NaOH溶液滴定 20.00mL0.1000 mol·L
NaOH溶液滴定 20.00mL0.1000 mol·L
 溶液所得滴定曲线如图。下列说法正确的是
溶液所得滴定曲线如图。下列说法正确的是
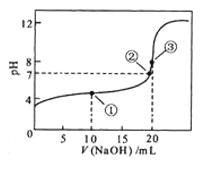
A.点①所示溶液中:
B.点②所示溶液中:
C.点③所示溶液中:
D.滴定过程中可能出现: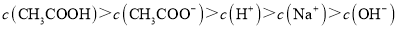
-
常温下,用 0.1000 mol·L NaOH溶液滴定 20.00mL0.1000 mol·L
NaOH溶液滴定 20.00mL0.1000 mol·L
 溶液所得滴定曲线如图。下列说法正确的是
溶液所得滴定曲线如图。下列说法正确的是
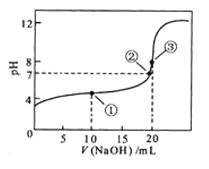
A.点①所示溶液中:
B.点②所示溶液中:
C.点③所示溶液中:
D.滴定过程中可能出现: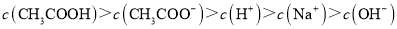
-
常温下,用 0.1000 mol·L NaOH溶液滴定 20.00mL0.1000 mol·L
NaOH溶液滴定 20.00mL0.1000 mol·L
 溶液所得滴定曲线如图。下列说法正确的是
溶液所得滴定曲线如图。下列说法正确的是
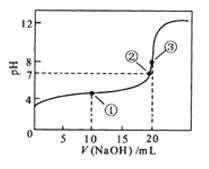
A.点①所示溶液中:
B.点②所示溶液中:
C.点③所示溶液中:
D.滴定过程中可能出现: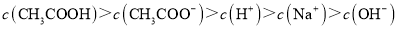
-
常温下,用 0.1000 mol·L NaOH溶液滴定 20.00mL0.1000 mol·L
NaOH溶液滴定 20.00mL0.1000 mol·L
 溶液所得滴定曲线如下图。下列说法正确的是
溶液所得滴定曲线如下图。下列说法正确的是
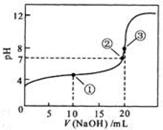
A、点①所示溶液中:
B、点②所示溶液中:
C、点③所示溶液中:
D、滴定过程中可能出现