-
阿司匹林(乙酰水杨酸, )是世界上应用最广泛的解热、镇痛和抗炎药。乙酰水杨酸受热易分解,分解温度为128℃~135℃。某学习小组在实验室以水杨酸(邻羟基苯甲酸)与醋酸酐[(CH3CO)2O]为主要原料合成阿司匹林,反应原理如下:
)是世界上应用最广泛的解热、镇痛和抗炎药。乙酰水杨酸受热易分解,分解温度为128℃~135℃。某学习小组在实验室以水杨酸(邻羟基苯甲酸)与醋酸酐[(CH3CO)2O]为主要原料合成阿司匹林,反应原理如下:

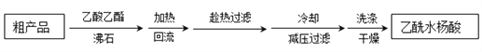
制备基本操作流程如下:
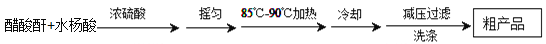
主要试剂和产品的物理常数如下表所示:
| 名称 | 相对分子质量 | 熔点或沸点(℃) | 水 |
| 水杨酸 | 138 | 158(熔点) | 微溶 |
| 醋酸酐 | 102 | 139.4(沸点) | 易水解 |
| 乙酰水杨酸 | 180 | 135(熔点) | 微溶 |
请根据以上信息回答下列问题:
(1)制备阿司匹林时,要使用干燥的仪器的原因是________________________________。
(2)合成阿司匹林时,最合适的加热方法是______________________。

(3)提纯粗产品流程如下,加热回流装置如图:

①沸石的作用是__________________________________;
②冷凝水的流出方向是________________(填“b”或“c”);
③使用温度计的目的是_____________________________________________________。
(4)在实验中原料用量:2.0g水杨酸、5.0mL醋酸酐( ),最终称得产品质量为2.2g,则所得乙酰水杨酸的产率为__________________(用百分数表示,小数点后一位)。
),最终称得产品质量为2.2g,则所得乙酰水杨酸的产率为__________________(用百分数表示,小数点后一位)。
-
阿司匹林(乙酰水杨酸,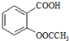 )是世界上应用最广泛的解热、镇痛和抗炎药。乙酰水杨酸受热易分解,分解温度为128℃~135℃.某学习小组在实验室以水杨酸(邻羟基苯甲酸)与醋酸酐[(CH3CO)2O]为主要原料合成阿司匹林,反应原理如下:
)是世界上应用最广泛的解热、镇痛和抗炎药。乙酰水杨酸受热易分解,分解温度为128℃~135℃.某学习小组在实验室以水杨酸(邻羟基苯甲酸)与醋酸酐[(CH3CO)2O]为主要原料合成阿司匹林,反应原理如下:

制备基本操作流程、装置示意图和有关数据如下(夹持和加热仪器已略去):

主要试剂和产品的物理常数
| 名称 | 相对分子质量 | 熔点或沸点(℃) | 水 |
| 水杨酸 | 138 | 158(熔点) | 微溶 |
| 醋酸 | 102 | 139.4(沸点) | 反应 |
| 乙酸水杨酸 | 180 | 135(熔点) | 微溶 |
请根据以上信息回答下列问题:
(1)制备备阿司匹林时,要使用干燥仪器的原因是________________________;
(2)合成阿司匹林时,最合适的加热方法是________________________;
(3)提纯粗产品流程如下,加热回流装置如图:
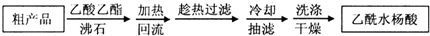
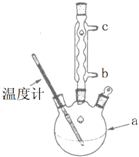
①使用温度计的目的是控制加热的温度,防止___________________________;
②冷凝水的流进方向是__________(填“a”或“b”)
③趁热过滤的原因是___________________________;
④下列说法正确的是__________(填选项字母)。
a.此种提纯方法中乙酸乙酯的作用是做溶剂
b.此种提纯产品的方法叫重结晶
c.根据以上提纯过程可以得出阿司匹林在乙酸乙酯中的溶解度低温时大
d.可以用紫色石蕊试液判断产品中是否含有未反应完的水杨酸
(4)该学习小组在实验中原料用量:2.0g水杨酸、5.0mL乙酸酐(ρ=1.08g•cm-3 ),最终称得产品质量m=2.2g,则所得乙酰水杨酸的产率为___________(用百分数表示,小数点后一位)。
-
阿司匹林(乙酰水杨酸,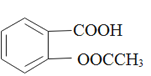 )是世界上应用最广泛的解热、镇痛和抗炎药。乙酰水杨酸受热易分解,分解温度为128℃~135℃。某学习小组在实验室以水杨酸(邻羟基苯甲酸)与醋酸酐[(CH3CO)2O]为主要原料合成阿司匹林,反应原理如下:
)是世界上应用最广泛的解热、镇痛和抗炎药。乙酰水杨酸受热易分解,分解温度为128℃~135℃。某学习小组在实验室以水杨酸(邻羟基苯甲酸)与醋酸酐[(CH3CO)2O]为主要原料合成阿司匹林,反应原理如下:

制备基本操作流程如下:
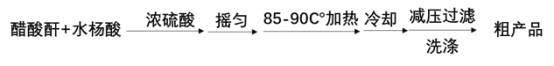
主要试剂和产品的物理常数如下表所示:
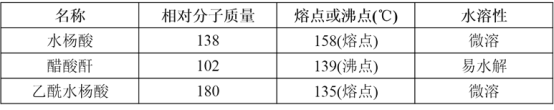
请根据以上信息回答下列问题:
(1)制备阿司匹林时,要使用干燥的仪器的原因是___。
(2)合成阿司匹林时,最合适的加热方法是___。
(3)提纯粗产品流程如下,加热回流装置如图:

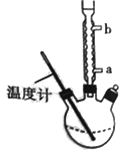
①使用温度计的目的是控制加热的温度,防止___。
②冷凝水的流进方向是___(填“a”或“b”)。
③趁热过滤的原因是___。
④下列说法不正确的是___(填字母)。
A.此种提纯方法中乙酸乙酯的作用是做溶剂
B.此种提纯粗产品的方法叫重结晶
C.根据以上提纯过程可以得出阿司匹林在乙酸乙酯中的溶解度低温时大
D.可以用紫色石蕊溶液判断产品中是否含有未反应完的水杨酸
(4)在实验中原料用量:2.0g水杨酸、5.0mL醋酸酐(ρ=1.08g/cm3),最终称得产品质量为2.2g,则所得乙酰水杨酸的产率为___%。
-
阿司匹林(乙酰水杨酸, )是世界上应用最广泛的解热、镇痛和抗炎药。乙酰水杨酸受热易分解,分解温度为128℃~135℃。某学习小组在实验室以水杨酸(邻羟基苯甲酸)与醋酸酐[(CH3CO)2O]为主要原料合成阿司匹林,反应原理如下:
)是世界上应用最广泛的解热、镇痛和抗炎药。乙酰水杨酸受热易分解,分解温度为128℃~135℃。某学习小组在实验室以水杨酸(邻羟基苯甲酸)与醋酸酐[(CH3CO)2O]为主要原料合成阿司匹林,反应原理如下:
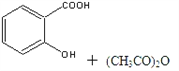
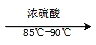
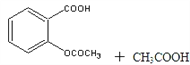
制备基本操作流程如下:
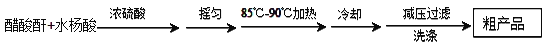
主要试剂和产品的物理常数如下表所示:
| 名称 | 相对分子质量 | 熔点或沸点(℃) | 水 |
| 水杨酸 | 138 | 158(熔点) | 微溶 |
| 醋酸酐 | 102 | 139.4(沸点) | 易水解 |
| 乙酰水杨酸 | 180 | 135(熔点) | 微溶 |
请根据以上信息回答下列问题:
(1)制备阿司匹林时,要使用干燥的仪器的原因是_____________________。
(2)合成阿司匹林时,最合适的加热方法是_________________________。
(3)提纯粗产品流程如下,加热回流装置如图:
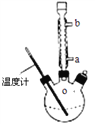
①使用温度计的目的是是控制加热的温度,防止_____________________________。
②冷凝水的流进方向是______________(填“a”或“b”);
③趁热过滤的原因是_________________________________________________。
④下列说法正确的是__________(填选项字母)。
a.此种提纯方法中乙酸乙酯的作用是做溶剂
b.此种提纯粗产品的方法叫重结晶
c.根据以上提纯过程可以得出阿司匹林在乙酸乙酯中的溶解度低温时大
d.可以用紫色石蕊溶液判断产品中是否含有未反应完的水杨酸
(4)在实验中原料用量:2.0g水杨酸、5.0mL醋酸酐( ),最终称得产品质量为2.2g,则所得乙酰水杨酸的产率为 ___________(用百分数表示,小数点后一位)。
),最终称得产品质量为2.2g,则所得乙酰水杨酸的产率为 ___________(用百分数表示,小数点后一位)。
-
(12分)(1)阿司匹林是世界上应用最广泛的解热、镇痛和抗炎药。乙酰水杨酸受热易分解,分解温度为128~135℃。某学习小组在实验室以水杨酸(邻羟基苯甲酸)与醋酸酐[(CH3CO)2O]为主要原料合成阿司匹林,制备基本操作流程(略)。
①写出制备阿司匹林的化学方程式________________。
可用重结晶提纯法提纯阿司匹林。方法如下:

加热回流的装置如图所示:
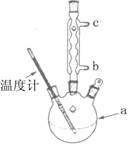
②使用温度计的目的是________________。
③冷凝水的流进方向是________________。(填“b”或“c”)。
④重结晶提纯法所得产品的有机杂质较少的原因________________。
检验产品中是否含有水杨酸的化学方法是________________。
(2)氯化苄(C6H5CH2Cl)也是一种重要的有机化工原料。工业上采用甲苯与干燥氯气在光照条件下反应合成氯化苄。为探索不同光强条件对合成产率的影响,需要对不同光强条件下的粗产品(含甲苯)进行纯度检测。每一组检测按照如下步骤进行:
A.称取0.300 g样品。
B.将样品与25 mL 4 mol·L-lNaOH溶液在三颈烧瓶中混合,水浴加热回流l小时后停止加热(发生的反应为:C6H5CH2Cl+NaOH→C6H5CH2OH+ NaCl)。
C.在三颈烧瓶中加入50 mL 2 mol·L-l HNO3,混合均匀。
D.将三颈烧瓶中溶液全部转移到100 mL容量瓶中,加水定容。
E.从容量瓶中取出25.00 mL溶液于锥形瓶中,加入6.00 mL 0.100 mol·L-1AgNO3溶液,振荡混合均匀。
F.在锥形瓶中滴入几滴NH4Fe(SO4)2溶液作为指示剂,用0.0250 mol·L-1 NH4SCN溶液滴定剩余的AgNO3。
G.重复E、F步骤三次,消耗0.0250 mol·L1NH4SCN溶液的平均值为4.00mL。
(已知:NH4SCN+ AgNO3= AgSCN↓+NH4NO3)根据以上实验信息回答下列相关问题:
①C步骤所加硝酸的目的是________。
②在F步骤操作中,判断达到滴定终点的现象是________。
③该产品的纯度为________。(请保留2位小数)
-
乙酰水杨酸即阿司匹林是最常用的解热镇痛药,其结构如图所示。关于它的描述中不正确的是( )
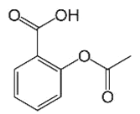
A.分子式为C9H8O4
B.1mol 乙酰水杨酸最多可以与2molNaOH反应
C.1mol乙酰水杨酸最多可以与3molH2反应
D.其在酸性条件下水解产物遇氯化铁溶液可以呈现紫色
-
乙酰水杨酸即阿司匹林是最常用的解热镇痛药,其结构如图所示。关于它的描述中不正确的是( )
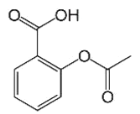
A.分子式为C9H8O4
B.1mol 乙酰水杨酸最多可以与2molNaOH反应
C.1mol乙酰水杨酸最多可以与3molH2反应
D.其在酸性条件下水解产物遇氯化铁溶液可以呈现紫色
-
乙酰水杨酸即阿司匹林是最常用的解热镇痛药,其结构如图所示。关于它的描述中不正确的是( )
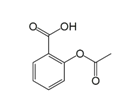
A.分子式为C9H8O4
B.其在酸性条件下水解产物遇氯化铁溶液可以呈现紫色
C.1mol 乙酰水杨酸最多可以与3molH2 反应
D.1mol 乙酰水杨酸最多可以与2molNaOH 反应
-
阿司匹林(Aspirin,乙酰水杨酸)是一种白色结晶或结晶性粉末,无臭或微带醋酸臭,微溶于水,易溶于乙醇,可溶于乙醚、氯仿,其水溶液呈酸性,是一种解热镇痛药,可用于治疗多种疾病。其结构如图所示,下列关于它的叙述正确的是( )

A.它的分子式为C9H7O4
B.它属于芳香烃
C.1mol它能与4molH2发生加成反应
D.它能发生加成反应、酯化反应、水解反应
-
邻羟基苯甲酸的结构简式为
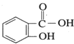 ,俗名为水杨酸,在医学上具有解热镇痛和抗炎、抗风湿作用,由于它易刺激胃肠道产生严重的反应,因此通常将它先转化为乙酰水杨酸(阿司匹林),服用后在人体内会缓慢反应生成水杨酸.
,俗名为水杨酸,在医学上具有解热镇痛和抗炎、抗风湿作用,由于它易刺激胃肠道产生严重的反应,因此通常将它先转化为乙酰水杨酸(阿司匹林),服用后在人体内会缓慢反应生成水杨酸.
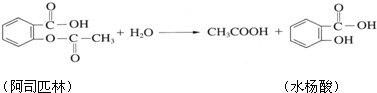
请回答下列问题:
(1)阿司匹林的分子式为______,其在人体内缓慢反应生成水杨酸的反应类型为______.
(2)在阿司匹林溶液中滴入紫色石蕊试液,溶液颜色变红,说明阿司匹林溶液具有______性.
(3)生产厂家将乙酰水杨酸制成其钠盐或钙盐,目的是______,以防止刺激胃黏膜.
 )是世界上应用最广泛的解热、镇痛和抗炎药。乙酰水杨酸受热易分解,分解温度为128℃~135℃.某学习小组在实验室以水杨酸(邻羟基苯甲酸)与醋酸酐[(CH3CO)2O]为主要原料合成阿司匹林,反应原理如下:
)是世界上应用最广泛的解热、镇痛和抗炎药。乙酰水杨酸受热易分解,分解温度为128℃~135℃.某学习小组在实验室以水杨酸(邻羟基苯甲酸)与醋酸酐[(CH3CO)2O]为主要原料合成阿司匹林,反应原理如下:

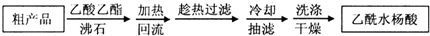


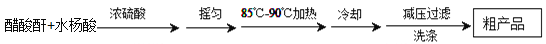


 )是世界上应用最广泛的解热、镇痛和抗炎药。乙酰水杨酸受热易分解,分解温度为128℃~135℃。某学习小组在实验室以水杨酸(邻羟基苯甲酸)与醋酸酐[(CH3CO)2O]为主要原料合成阿司匹林,反应原理如下:
)是世界上应用最广泛的解热、镇痛和抗炎药。乙酰水杨酸受热易分解,分解温度为128℃~135℃。某学习小组在实验室以水杨酸(邻羟基苯甲酸)与醋酸酐[(CH3CO)2O]为主要原料合成阿司匹林,反应原理如下:
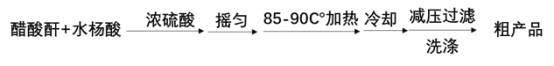




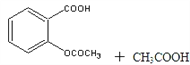
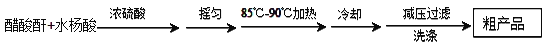







 ,俗名为水杨酸,在医学上具有解热镇痛和抗炎、抗风湿作用,由于它易刺激胃肠道产生严重的反应,因此通常将它先转化为乙酰水杨酸(阿司匹林),服用后在人体内会缓慢反应生成水杨酸.
,俗名为水杨酸,在医学上具有解热镇痛和抗炎、抗风湿作用,由于它易刺激胃肠道产生严重的反应,因此通常将它先转化为乙酰水杨酸(阿司匹林),服用后在人体内会缓慢反应生成水杨酸.